- 1.47 MB
- 2023-01-02 08:31:01 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
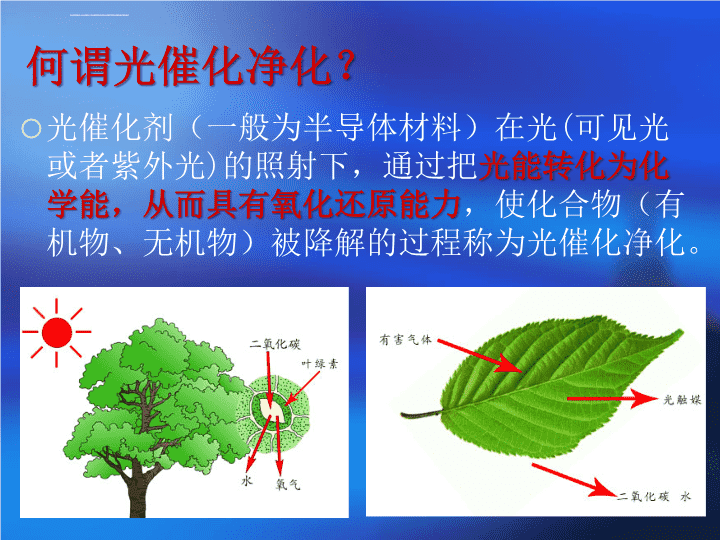
光催化净化方法及其在工业废水治理中的应用\n近年来,运用光催化氧化技术净化废水中的有机污染物,已经成功的得到了工业化应用,净化效果十分显著。\n何谓光催化净化?光催化剂(一般为半导体材料)在光(可见光或者紫外光)的照射下,通过把光能转化为化学能,从而具有氧化还原能力,使化合物(有机物、无机物)被降解的过程称为光催化净化。\n从光合作用这种最简单的光催化反应,总结下一个光催化反应发生的三个基本条件:叶绿素------光催化剂光------------特定波长范围(400-600nm之间最佳),非所有光都可以反应物------二氧化碳和水光催化剂------一般为半导体材料光------------也是特定波长范围,非所有光都可以,一般处于紫外线范围的光的效果最佳。反应物--------室内空气中的有机物光催化净化反应的三个基本条件:\n1972年,Fujishima和Honda首先报道利用二氧化钛(TiO2)做单晶电极用来分解水制备氢气以来,半导体多相光催化反应引起了各国研究者的关注(石油危机,对能源的巨大需求,但是该研究一直进展很小,原因是?)。1976年,加拿大科学家Carey等将TiO2光催化应用于废水中剧毒多氯联苯的降解研究,从而开创了将光催化氧化技术应用于污染物治理领域的先河。进入20世纪90年代以后,研究界发表了大量将光催化剂应用于环境中有害物质分解的报道。\n光催化氧化技术基础1)光的波长与能量光催化氧化反应,是从光催化剂吸收光子开始的。光化学反应需要具有一定能量的光子来诱发。一个光子的能量可以表示为:E=hv=hc/λ式中:h-普朗克常数,v-光的频率,c-光速光的波长越长,其具有的能量就越少,依次从紫外向红外递减。因此,紫外光的能量最高,红外光低,比如不同的车辆,一个车速快,冲击力大,一个车速慢,冲击力小。\n因此,紫外光光子的能量最高,红外光光子低,比如不同的车辆,一个车速快,冲击力大,一个车速慢,冲击力小。紫外光的化学效应如此强,以至于单纯的开紫外光,都有很好的杀菌效果,医院和食堂等场合。但是单纯的紫外光对有机物的杀灭效果是有一定限制的,不强。因此,要配合光催化剂使用。\n因此,我们可以初步设想一下光催化反应的发生过程:某光催化剂,处于某种室内空气环境中(室内空气中含有多种污染物),在光催化剂接触到某种波长光线以后,光子开始轰击光催化剂表面,其中,能量大于某一个阈值(或者说波长小于某一个阈值)的光子对表面的轰击使光催化剂表面发生了某种变化(分离出能够自由运动的电子),从而具有了氧化还原能力,这样,当气态污染物接触到光催化剂表面上时候,则被氧化还原。思考:哪些化合物具有光催化性能呢?(光催化剂和某一类物质有共同点)\n半导体是介于导体和绝缘体之间,电导率在(10-10~104-1cm-1)之间的物质。由于半导体具有特殊的光、电、磁等性质,从而在电子、化工、医药、航空和军事领域得到了广泛的应用。这种半导体的导电性质与其所处的温度、光照情况有关。利用此性质可以制的光敏元件和热敏元件。常见的半导体材料实际上可以分为两种,元素半导体、化合物半导体。常见的元素半导体材料包括鍺、硅、西、碲。化合物半导体有ZnS、TiO2、ZnO、CdS、SnO2和Fe3O4等。用作光催化氧化作用的半导体大多为金属的氧化物和硫化物。而TiO2材料制成的催化剂无毒、廉价、高效、性能稳定。\n以二氧化钛为例,为什么二氧化钛的表面在有和没有光照射的情况下,会从不具有氧化还原能力转化为具有氧化还原能力?从氧化还原能力的本质思考这个问题:氧化还原意味着电子的转移和交换。或者说,意味着光催化剂在有光照射的情况下,其表面具备了提供或者索取电子的能力。\n半导体的能带结构半导体存在一系列的满带,最下面的满带成为价带(valenceband,VB);存在一系列的空带,最上面的空带称为导带(conductionband,CB);价带和导带之间为禁带。当用能量等于或大于禁带宽度(Eg)的光照射时,半导体价带上的电子可被激发跃迁到导带,同时在价带上产生相应的空穴,这样就在半导体内部生成电子(e-)-空穴(h+)对。\n石榴籽:光致电子石榴籽留下的空洞:光致空穴\n光致电子:存在于导带中。光致空穴:存在于价带中。二者有复合的趋势,即在持续的光照射下,光子不断的轰击价带,导致光致电子和光致空穴不断产生,该分离过程以纳秒计算,然后,光致电子重新回到光致空穴中,二者复合。\nA/B/C/D为吸附在光催化剂表面的污染物分子\n因此,总结一下,对于某种光催化剂,用光子能量大于禁带宽度Eg的光来照射可以产生光致电子和光致空穴,他们在复合之前分别具有氧化和还原能力。由于光是持续照射的,因此宏观上总是在光催化剂表面上有固定数量的光致电子和光致空穴存在,因此表面具有持久的氧化还原能力。不同的半导体,Eg不同\n思考:禁带宽度Eg和光子的能量。\n二氧化钛的禁带宽度Eg为3.2eV,那么,如果想使那个二氧化钛来进行光催化反应,则要求照射到其分子上的光子所具有的能量大于这个数值,对照上表,可以看出,必须使得入射光子的波长小于等于387.5纳米。思考:如果一个光子的能量不够,能不能2个或者更多的光子共同照射一个固定位置,从而激发光致电子和光致空穴?在此,我们引出光化学反应中重要的两个定律:1)光化学定律1只有被分子有效吸收的光,才能有效引起分子的化学变化;2)光化学定律2发生光化学反应变化是由于分子吸收一个光量子的结果,在光化学反应发生的初期,被吸收的一个光子,只能激活一个分子。这两个定律是,决定光催化反应的根本规律。\n因此,对于已经选定的某种光催化剂,如果想促使其表面产生光致电子和光致空穴,必须保证照射到表面的光,其波长小于某个阈值,即单个光子能量要大于禁带宽度Eg,对于波长大于阈值的光,无论如何增大光的强度,都无法促使光催化剂表面产生光致电子和光致空穴,也无法促使其产生氧化还原能力。\n光致电子的标准氢电极电位为-1.5---0.5eV,,具有很强的还原性,可以使得半导体表面的电子受体被还原。而光致空穴的标准氢电极电位为1.0-3.5eV,具有很强的得电子能力,可以夺取粒子表面的有机物或者体系中的电子。由此可见,光致电子一旦和光致空穴分布到不同的位置,就有可能参与氧化和还原反应。\n二氧化钛表面光致电子和光致空穴的产生过程\n可以想象一下,在分子的周围,形成了大量的光致电子和光致空穴,在光的照射下,他们不断产生,又不断复合,但是从宏观的角度看,在某一时刻,总是有大量的来不及复合的电子和空穴的存在,他们不断的寻找自己的猎物。作为光致电子来说,他们的猎物是电子受体,这样光致电子就可以还原这个电子受体;而光致空穴迁移到表面后的猎物时哪些能够提供电子的物质,从而将这些物质氧化。\n实际上,科学家在对光催化反应的反应过程进行深入研究的基础上,发现在实际环境中的光催化反应不仅是光致电子和光致空穴的氧化还原反应。并且会发生其他反应,从而强化对污染物的氧化还原反应。主要是在过程中生成氢氧自由基,氢氧自由基的氧化能力是特别强的。\n当以波长小于385nm的光照射TiO2表面时,价带电子能够被激发产生光生电子空穴对,同时激发态的导带电子和价带空穴又能重新合并,使光能以热能或其他形式散发掉,如下式所示:当TiO2催化剂存在合适的俘获剂时(如H2O或O2),电子和空穴的重新复合得到抑制,在它们复合之前,就会在光催化剂表面发生氧化还原反应:光生电子与表面吸附的氧分子反应,分子氧不仅参与还原反应,还是表面羟基自由基的另外一个来源,具体的反应式如下所示:\n另外,Sclafani和Herraman通过对TiO2光电导率的测定,证实了在光催化反应中·O2-的存在,因此一个可能的反应是:在上式中,产生了非常活泼的羟基自由基(·OH),超氧离子自由基(·O2-)以及·HO2自由基,这些都是氧化性很强的活泼自由基,能够将各种有机物直接氧化为CO2,H2O等无机小分子。\n总结:光致电子和光致空穴的电位分别是-1.5-0.5eV和1.0-3.5eV氢氧自由基的电位E=2.8ev结论:两者都具有超强的氧化还原能力。\n光生电子—空穴对的氧化还原机理\n27导带价带\n28光催化材料UV灯(关)病原体有机物UV灯(开)REPLAY光催化降解有机物和病原体原理图\n表半导体光催化降解部分有机污染物