- 577.81 KB
- 2022-04-22 13:39:34 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中华人民共和国国家标准纸和纸板中无机填料和无机涂料的定性分析化学法GB/T2679.12一93Paperandboard-Qualitativeanalysisofmineralfillerandmineralcoating-Chemicalmethod1主题内容与适用范围本标准规定了测定纸和纸板中无机填料和无机涂料的化学定性分析方法。本标准适用于纸和纸板中无机填料的测定,也适用于涂布加工纸中无机涂料的测定。2引用标准GB45。纸和纸板试样的采取GB462纸和纸板水分的测定法GB463纸和纸板灰分的测定GB8943.4纸浆、纸和纸板钙、镁含量的测定法GB12658纸浆、纸和纸板中钾、钠含量的测定GB1291。纸和纸板二氧化钦含量的测定法3原理将纸样经575士25℃灼烧,由灰分的含量和外观大致可以确定填料和涂料中是否含无机物。如果填料和涂料中含有无机物,可以用原纸或由原样品烧成的灰进行化学鉴别,根据化学反应的现象或红外光谱的图形来推断出无机物的名称。然后按该无机物的定量测试法,测定其含量。4试剂分析时,必须使用分析纯试剂,水应符合4.1条的规定。4.1蒸馏水或去离子水。4.2浓盐酸:HCl(pznn=1.19).4.31:1(V/V)的盐酸。4.4稀盐酸:C(NCOz2mol/Lo将15mL的浓盐酸溶于75mL的水中,并用水稀释至100mLo4.5乙酸铅试纸浸溃滤纸于饱和的乙酸铅[Pb(CEH刀:)·3H20」的溶液中,取出风干后备用。4,6重铬酸钾(K2Cr207)溶液:4%(m/m),4.了饱和石灰水溶液溶解约0.2g的氢氧化钙[Ca(OH)2」于100mL的水中并过滤。4.8碘溶液。(1/212)-0.lmol/Lo4.9硫酸铁(NH4)2SO40国家技术监督局1993一08一07批准1994一03-01实施
GB/T2679.12一934.10浓硫酸:H,SO,(P-^1.84)04.11稀硫酸:5%(m/m)3mL的浓硫酸加到约75mL的水中,然后稀释至IOOmLo4.12过氧化氢溶液(HA):30%(m/m),4.13氯化钡溶液:looo(m/m)o4.14亚铁氰化钾溶液取15g的亚铁氰化钾[K,Fe(CN)s·3HM溶解于1OOOmL的水中。4.15二苯基硫卡巴腺(又称双硫踪dithizone)溶液溶解log的二苯基硫卡巴踪于100mL的四氯化碳(CCI,)中。4.16试镁灵溶解0.5g的对硝基苯偶氮间苯二酚[4-(nitrophenylazo)resorcinol〕于100mLl%的氢氧化钠溶液中。4.17氢氧化钾溶液:c(KOH)}2mol/L溶解11.2g的氢氧化钾于75mL的水中,冷却并稀释至100mL,4.18氢氧化钠溶液:c(NaOH)-2mol/L溶解8g的氢氧化钠于75mL水中,冷却并稀释至lOOmL,4.19乙酸:c(CH,COOH)z2mol/L4.20桑色素C3,5,7,2",4,一五9基黄烷酮(morin)J:桑色素溶于甲醇的饱和溶液。4.21固体碳酸钠。4.22氢氧化铁(NH,OH)溶液:15YO(m/M).4.23碳酸按溶液:c[(NH,)zCO,]-2mol/L,4.24草酸按L(NH4)2C2041溶液:5%(m/m).4.25磷酸氢二钠〔Na2HP04·12H20]溶液:20Yo(m/m)a4.26甲基红指示液:lg/L称取。.1g的甲基红,溶解于95%的乙醉中,并用乙醇稀释至100mL,4.27甲基橙指示液:lg/L称取。.lg的甲基橙,溶于100mL的蒸馏水中。5仪器5.1一般实验室仪器5.2高温炉:控温范围为室温至1000℃可调。5.3烘箱:能控温调节105士2"C。5.4具盖的铂增祸:30^-50mL,5.5瓷增涡:30-50mL.5.6白色的点滴盘一块。5.了黑色的点滴盘一块。5.8带环的铂丝一根。5.9红外分光光度计及其必要的附件。5.10原子吸收分光光度计及其相应的被检测元素的空心阴极灯。6试样的采取试样的采取应按照GB450的规定进行。6.1为了完成每一项的化学分析,从每一个测试单元中选取足量的试样,以便灼烧时所得到的灰分不
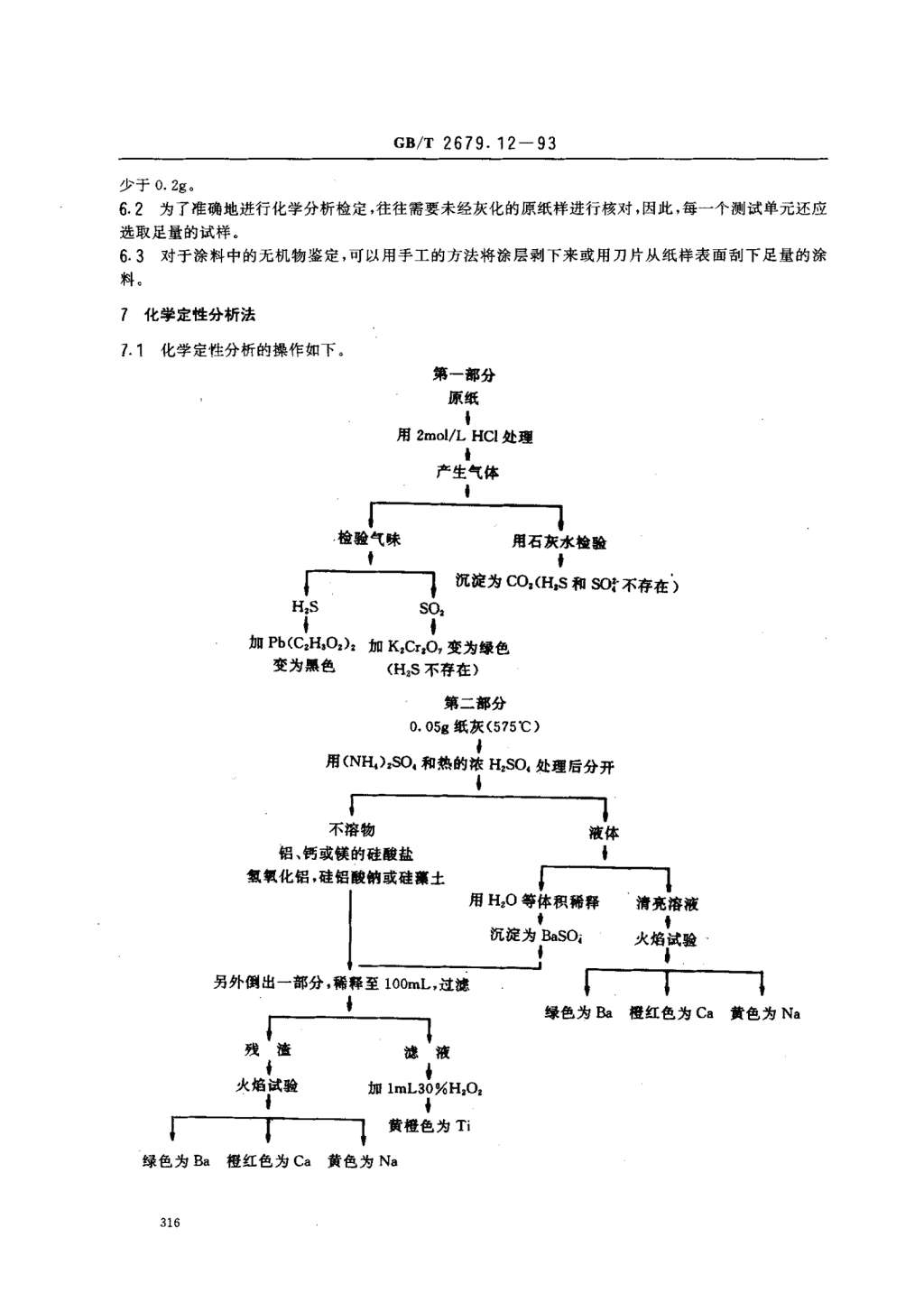
GB/T2679.12一93少于0.2g,6.2为了准确地进行化学分析检定,往往需要未经灰化的原纸样进行核对,因此,每一个测试单元还应选取足量的试样。6.3对于涂料中的无机物鉴定,可以用手工的方法将涂层剥下来或用刀片从纸样表面刮下足量的涂料。7化学定性分析法7.1化学定性分析的操作如下。第一部分原纸份用2mol/LHCl处理位产生气体口枪脸气味用石灰水检脸i沉淀为CO,(HS和SO;不存在’)加Pb(CA氏):加K,Cr,O,变为绿色变为黑色(H,S不存在)第二部分0.05g纸灰(575"C)口用(NH,),SO。和热的浓H,SO。处理后左‘不溶物液体铝、钙或镁的硅酸盐母氮氧化铝,硅铝酸钠或硅裁土{”’1用Hz0等体积稀释清亮溶液毋母沉淀为BaSOi口火竿-一-一~----一~-~---另外倒出一部分,稀释至100mL,过滤绿色为Ba橙红色为Ca黄色为Na火焰试验加1mL30^oH,认母黄橙色为Ti绿色为Ba橙红色为Ca黄色为Na
cB/T2679.12一93第兰部分。.lg纸祥灰舀用HCl处理并过逮4泌液不溶物分成6份(见第四部分)①②③④⑥⑥取约1/5,加Bact,取约1/10,加K,Cr2O,取约1/5,加K,Fe(CN)6毛番备绿色为S02沉淀为Znl沉淀为so全,加NH,OH和NH,CI往一滴滤液中加一滴取约1/10,加试模灵过诊取约2/5并过逮双硫惊,紫红色为滤液沉淀为酸溶性AI滤液天蓝色沉淀为Mg奋by(NH,),CO,奋备加KOH中和,乙陇玻化*沉淀为Ba或Ca备加桑色素‘加乙酸和K2Cr2O7备绿色荧光为Al滤液黄色沉淀为Ba杏加(NH,)2C,0,易白色沉淀为Ca各用火焰试验校对
GB/T2679.12一93第四部分HCI不溶物用Na,C氏烙融,再溶于HCI中并过撼滤液不溶物奋合烘干加HO加热,如果不溶.加H,SO,再溶于HCI过渔(NH,),SO‘加热排除SO,并一厂11逮液不溶物为Sio,倾入水中白色沉淀为Baso,沁液碑液取3/4,加NH,OH取1从,加BaCI,沉渔可为S心.加NaOH备加30%H.0.沉淀为SO;黄怪色为Ti沉淀为AI,Ti沉淀为Ti诊液用HO酸化加H,SO,.煮沸并过毖加NH,OH诱沉淀为AI沉淀为Ba撼液加NH,OH和(NH,),C,O,并过滤滤液加决酸盐沉淀为Ca毛沉淀为Mg
GB/T2679.12一93了.2亚硫酸盐、硫化物和碳酸盐(未灼烧的涂料或纸样)的鉴别7.2.1将部分未灼烧的涂料或纸样放在一个小烧杯中或在一支试管中,滴加2mol/L的盐酸(4.4),注意观察是否释出气泡或逸出有味的气体。若释出二氧化硫(SOS)或硫化氢(HAS)则表示有亚硫酸盐或硫化物存在。将烧杯或试管加热,并用湿的乙酸铅试纸(4.5)测试蒸汽,若出现一种金属的银灰色或黑色,证实有硫化物存在。如果不存在硫化物,可以继续向上述的烧杯或试管中加几粒结晶重铬酸钾或几滴4%的重铬酸钾溶液(4.6),若产生绿色表明存在还原剂。在这种情况下,多半是亚硫酸盐。在填料或涂料的纸中,同时使用亚硫酸盐和硫化物的混合物,一般不多见。7.2.2如果亚硫酸盐和硫化物都不存在,那么逸出气泡就是某种碳酸盐存在的最好证明。检验由碳酸盐分解出的二氧化碳,可以拿一支玻璃棒蘸一滴饱和的石灰水(4.7)于正在加热的装有用盐酸溶解试样的烧杯或试管溶液的正上方,若液滴出现混浊(牛奶样),则表明存在二氧化碳W02),这种沉淀后来会溶解。当有亚硫酸盐存在时,可以将亚硫酸盐氧化变成硫酸盐。即在试验的烧杯或试管中一滴一滴地加入碘溶液(4.8)一直到试液全部变成黄色,然后用一支玻璃棒蘸石灰水(4.7)按本段前面所述的方法测试,并验证是否有二氧化碳逸出。了.3烧灰与观察灰分鉴别取足量的试样于增锅中,低温炭化后,移入高温炉中经575士25℃灼烧(使用这祥低的温度是为了保护各种填料和涂料的成分,或将他们的变化减少到最低限度。如果按GB463法烧灰,温度为925士25‘C,那么碳酸钙就不存在了),测定其灰分含量和观察其灰分的外观来判断是否含有无机物。如果灰分含量小于1%或稍大于1肠,具有轻而蓬松的特点,可能没有加无机填料;如果灰分大于1%,呈现紧密而结实,似乎是加了填料;如果灰分100,也有可能掺用废纸,则要借助其他方法检定,如显微镜等的测定法。在试样炭化灼烧的过程中,某些无机填料或涂料会产生化学变化,例如:碳酸盐、硫化物和亚硫酸盐等。因此,对上述这些组分的检验应采用未灼烧的原纸样。7.4氢氧化铝、硅铝酸钠、铝、钙或镁的硅酸盐、钙或钡的硫酸盐、二氧化钦。7.4.1向约。.05g的灰(7.3)中,加人log的硫酸按和20mL的浓硫酸于一个250mL的烧杯中,盖上玻璃表面皿,煮沸至少3min。出现白色的烟雾系硫酸分解产生的三氧化硫。7.4.2在这么强的酸作用下,烧杯中的灰分不溶解物可能是:钙、铝或镁的硅酸盐,铝的氢氧化物或者硅藻土。如果热的溶液是清亮的,说明上述这些无机物是不存在的,而钙或/和钡的硫酸盐也能溶于热的浓硫酸中,若所取的灰分大于0.05g就可能不完全溶解。而二氧化钦是能溶于那种溶剂中。7.4.3倾出一些上层清液于一个小烧杯中,冷却后,小心地用一些冷水稀释它(稀释至原体积的5倍)。在稀释时若生成一种白色沉淀,表明有硫酸钡存在。因为硫酸钡相对地可溶于热的浓硫酸中,而不溶于稀硫酸中。7.4.4将7.4.2条的强酸处理物冷却后,也用水稀释至原体积的5倍与7.4.3条的试液混合并过滤,残渣留作7.4.5条的检验,向所得的滤液中加人1mL30%的过氧化氢溶液(4.12),这时溶液若出现黄色或橙色,表明含有钦。其颜色的深浅与钦的含量成正比,若仅产生微黄色,那可能是由高岭土中的钦或工厂的生产用水中溶有钦引起的。7.4.57.4.4条得到的残渣可以用下列的焰色试验来测定是否含有钙和钡。拿一根铂丝环蘸留在滤纸上的湿渣,并拿到酒精喷灯的火焰上,观察其火焰的颜色:绿色火焰:表明是钡的化合物;红色火焰:表明是钙的化合物;黄色火焰:表明是铝和/或镁的硅酸盐,铝的氢氧化物。7.4.6可以用焰色试验来检测由7.4.3条中得到的清液中可溶性的钙、钡和钠。其做法是用等体积的水小心地稀释少部分溶液,用铂金丝蘸此溶液,拿到酒精喷灯的火焰上观察其火焰的颜色:绿色火焰:表明是钡的化合物;红色火焰:表明是钙的化合物;强黄色火焰:表明是钠的化合物。7.5硫化物:亚硫酸盐和碳酸盐(利用试样经575士25℃灼烧的灰)的鉴别
GB/"r2679.12一937.5.1取灰分约。.1g(7.3)于一个小烧杯中,用少量的水润湿,加入1:1的盐酸(4.3)1OmL,与7.2.1条一样进行观察,若析出气泡,表明是一种碳酸盐的存在。取出1-2mI溶液加2滴4%重铬酸钾溶液(4.6),产生绿色表明有亚硫酸盐存在。7.5.2将上述的小烧杯中的内容物加热至沸,并用湿的乙酸铅试纸试烟气,若出现金属灰色或黑色表明有硫化物存在。7.5.1条和7.5.2条的这些试验应当用原纸作对比测试进行校核,因为灼烧时碳酸盐可能损失,碳酸盐可能被还原成亚硫酸盐或硫化物,或亚硫酸盐和硫化物被氧化成硫酸盐。这一切取决于灼烧时的温度和氧化条件。7.5.37.5.1条的小烧杯中的内容物若不完全溶解,将其煮沸5min,然后加人35mL的水,再次加热至沸,若这种溶液还不清亮,通过定量紧密滤纸进行过滤,用2倍于溶液的水洗涤,滤液用作酸溶部分(7.6)的分析。彻底地洗涤不溶残渣至无酸性反应[用甲基橙指示液(4.27)检验〕,弃掉洗涤液,保留滤纸上的酸不溶物,留作7.7条的试验用。76锌、镁、铝、钡、钙的硫酸盐7.6.,取7.5.3条得到的酸可溶滤液约1/5体积,加入氯化钡溶液(4.13)1mL后,若出现沉淀,或加热1Omin以后出现沉淀,表示有硫酸盐存在。另取约1/5体积的滤液,加入几毫升的亚铁氰化钾溶液(4.14),一种浓白色的沉淀出现,表明锌的存在。锌的存在可以用下一条的双硫踪试验还原成红色来证实。7.6.2取一滴由7.5.3条得到的酸溶解滤液于一个玻璃表面皿上,加1滴2mol/I的氢氧化钠溶液(4.18)和几滴双硫腺溶液(4.15)。当用玻璃棒搅拌时,四氯化碳挥发掉,而溶液若出现紫红色,证实锌的存在。沉淀的其他颜色可以不必考虑。7.6.3取保留下来的滤液(7-5-3)中的3/5体积加入1^-2滴试镁灵(4.16),并用氢氧化钠溶液(4.18)碱化,产生一种天蓝色的沉淀表明有镁的存在,然而普通纸中使用的其他无机物所得到的是紫色(与天蓝色不同)的溶液,小心不要加入过量的试剂,因为即使有镁的存在,过量可能掩蔽蓝色的沉淀。若有疑问的话,将溶液过滤,检查滤纸上是否有蓝色沉淀。7.6.4取1mL的酸溶滤液(7.5.3),加人2mol/L的氢氧化钾溶液(4.17)中和,并使之过量。取1滴这种溶液,用2mol/L的乙酸(4.19)在黑色的点滴盘上酸化,然后加1滴桑色素溶液(4.20)。若有铝存在时,这种混合物在晚上或紫外灯下检查时,会出现一种绿色的荧光。7.6.5向所保留的剩下的酸溶滤液(7.5.3)中一滴一滴地加人氢氧化铁溶液(4.22),中和至出现氨味,若铝以酸溶解的形式存在,这时就会产生出一种白色絮状沉淀。滤弃沉淀,滤液中加入碳酸按溶液(4.23),若出现一种白色沉淀,表明有钙和钡存在,不要过滤,将溶液用乙酸(4.19)酸化(乙酸会溶解沉淀),加入重铬酸钾溶液(4.6),若钡以酸溶解的形式存在,就会产生一种黄色沉淀,过滤弃黄色沉淀,加过量的碳酸钱溶液(4.23),出现白色沉淀,表明是钙(在操作过程中,钡已经除去),对于钙的检查,还可以按7.4.5条焰色试验,核验一下沉淀。7.了镁、铝的硅酸盐(滑石粉、高岭土)、氢氧化铝、硫酸盐7.7.1将7.5.3条中保留下来的酸不溶物的滤纸放到铂增祸中,干燥、炭化、灼烧去有机物,冷却并加人1-2g的无水碳酸钠拌和,放在925^1000℃的高温炉中熔融半小时,取出冷却,向增祸内加少量的水,以玻璃棒在熔块上轻轻地左右用力旋转使熔块脱落,连盖一并放入250mL盛有20mL水的烧杯中,盖上表面皿,慢慢地加人20mL1:1的盐酸溶液(4.3)使熔块溶解,待作用停止后,将钳塌和盖洗净取出,加热至沸,搅拌并过滤。保存残渣留作7.8条的分析用。7.7.2将7.7.1条获得的滤液在水浴上蒸发至干,加入5mL浓盐酸(4.2)及40mL水,加热,溶液中若出现一种明亮的不溶解的絮状物,这可能是由于硅酸盐中的硅脱水后析出。最好借助于黑色背影进行观察。稍置片刻后过滤。7.7.3取7.7.2条获得的滤液1/4体积,加人氯化钡溶液(4.13)5mL,若出现沉淀,表明硫酸盐的存320
GB/T2679.12一93在,将其余的3/4体积滤液慢慢滴加氢氧化钱溶液(4.22),若出现一种白色的凝胶状沉淀,表明铝的存在。加热并过滤沉淀,与7.7.1条合并保存,留作7.8条的分析用。在滤液中加入5%的硫酸(4.11)5mL,这时钡以硫酸钡的形式沉淀,然后煮沸并过滤,滤液用氨碱化至呈现出氨味,加草酸按溶液(4.24)至保证钙沉淀完全。若有钙沉淀,滤弃沉淀,然后加入5mL的氢氧化钱溶液(4.22)和过量(约5mL)的磷酸氢二钠溶液(4.25)或磷酸氢按溶液,搅拌均匀,在15min内出现沉淀表明有镁的化合物。当然对于镁的鉴别还可以按7.6.3条的方法用试镁灵进行测试。7.8二氧化硅、硫酸钡和二氧化钦将7.7.1条保存的残渣和7.7.3条检验氢氧化铝的沉淀用细水流喷洗沉淀返回原来的烧杯中,加入5mL的浓盐酸(4.2),若溶解不完全,加人10mL的浓硫酸(4.10),在通风柜内加热,一直到出现三氧化硫烟雾,冷却后,倾入盛有35mL的水中,若出现白色沉淀,这是硫酸钡,因为硫酸钡不会被碳酸钠熔融分解,并能溶于热的浓硫酸中,滤弃沉淀,滴2滴甲基红指示剂(4.26),用2mol/L的氢氧化钠溶液(4.18)中和,并再加入中和时所需要溶液等体积的氢氧化钠,加热至沸并冷却,若出现沉淀为氢氧化钦(关于钦的鉴别,也可以按7.4条的方法,用硫酸铰和硫酸处理上述残渣,向处理后的溶液中加过氧化氢溶液检验)过滤去氢氧化钦的沉淀物。滤液用1:1的盐酸(4.3)中和,加热至沸后,再用氢氧化按溶液(4.22)中和至显氨味(溶液中的甲基红变色后多加2-3滴),若有沉淀生成,其沉淀为氢氧化铝[Al(OH)31-了.9化学定性试验的现象观察与解释了.9.飞纸中的填料和涂料所含的无机成分可按下列指定的章条做判断实验碳酸钙:Ca(7.6.5),COp(7.2.2)碳酸钙中带有氢氧化镁或其他碳酸盐:Ca(7.6.5).Mg(7.6.3),COE(7.2.2)亚硫酸钙:Ca(7.6.5)1SO2(7.2.1)硫酸钙:Ca(7.6.5),SO专一(7.6.1)碳酸钡:Ba(7.6.5),COi(7.2.2)硫酸钡:Ba(7.4.3,7.8),S0乏一(7.7.3)锌钡白(lithopone)(立德粉、硫化物):硫化物(7.2.1),Zn(7.6.1,7.6.2),Ba(7.4.3,7.8),SO;(7.7.3)氧化锌:Zn(7.6.1,7.6.2)硫化锌:Zn(7.6.1,7.6.2),硫化物(7.2.1)二氧化钦一硫酸钡:Ti(7.4.4,7.8),Ba(7.4.3,7.8),S0;-(7.7.3)二氧化钦一硫酸钙:Ti(7.4.4,7.8),Ca(7.6.5),SOq-(7.6.1)缎白(涂料),AI(7.6.4,7.6.5),Ca(7.6.5),SO戈一(7.6.1)硅铝酸钠:Na(7.4.6),AI(7.6.4,7.6.5,7.7.3),SiO,(7.7.2)铝的氢氧化物:AI(7.6.4,7.6.5,7.7.3)高岭土:AI(7.7.3,7.8)硅藻土:Si02(7.7.2)滑石粉:Mg(7.6.3),SiOi(7.7.2)了9.2造纸工业中用硫化物作为填料或涂料,只限于单独使用硫化锌或与硫酸钡结合(锌钡白)使用。在不存在硫化物时,检出锌来,表明使用的是氧化锌。检出亚硫酸盐,一般所用的为亚硫酸钙。7.9.3大部分商业填料含有杂质,如缎白中可能含有碳酸钙;高岭土中(如:美国高岭土)可能含有少量的钦,还可能含有钙和镁;二氧化钦可能含有少量的铝和硫酸盐,钙填料可能含有镁;硫化物和亚硫酸盐填料通常含有硫酸盐,因此,在做出判断时要注意。7.9.4在普通的造纸过程中施用铝,因此,在不加填料时也会导致相当大量铝的化合物存在。在不含填料的纸中,也可以检验出含有少量的或痕量的硫酸钙和硫酸镁等,它来源于浆和工厂使用的硬水中。
GB/T2679.12一937.9.5碳酸盐通常与很多酸可溶性钙盐并存,如与白噩或缎白并存。若用盐酸可以溶解,有可能含有镁,显示出碳酸钙和碳酸镁的混合物。一种钡和碳酸盐的混合物,可能是以毒晶石的形式存在。在这种形式中,用盐酸处理灰分时,钡就能溶解并被检出,因为硫酸钡是不溶于稀盐酸的。了.9.6由试验证明,其无机物是一种酸溶性的硫酸盐,并检验出钙来,表明所用的是上等填料硫酸钙、石膏、缎白等。如果在涂料中有相当多的盐酸可溶的铝存在,那么所用的无机物可能是缎白或铝的氢氧化物。如果所用的是碳酸盐与硫化物相配合使用,没有硫酸盐,但在试验时有可能检出硫酸盐来。了.9.了试验证实有钙和亚硫酸盐,则表示用的是亚硫酸钙。7.98检定出有相当多的镁和硅酸盐存在,表明使用的是滑石粉、纤(维)滑石或微(滑)石棉。仅检出二氧化硅表明使用的是硅藻土,其硅藻土形状可以由显微镜检查辩认。7.9.9用浓硫酸处理灰分得到的部分残渣可能是高岭土、滑石粉、硅铝酸钠、硅酸钙、硅藻土、铝的氢氧化物或是这些物质的一种混合物,若确认试验有铝存在,表明所用的是高岭土,硅铝酸钠或铝的氢氧化物。7.9.10硫酸钡(重晶石或硫酸钡粉),检定时显示出能溶于热的浓硫酸中,而在稀硫酸中却生成沉淀。可以用残渣的焰色试验来证实。7.9.11钦一般以二氧化钦的形式存在,通常造纸中用的为钦钡颜料(BaS04-TiO2)和钦钙颜料(Ca-S04-TiO2),8红外光谱分析第7章中的化学定性分析法,检测的是无机离子,试验时不但能检测到组成填料和涂料的无机离子,有时还检测出杂质的无机物离子。这给鉴定带来了困难,分不清是填、涂进去的还是杂质,而且化学定性所用的药品多,步骤繁。如果能将红外光谱与化学定性法相结合,通常可以使鉴定工作简化。因为红外不仅检定的是分子中的基团,而且物质经稍微纯化后,其扫描光谱图代表了整个无机物的特征谱图。当杂质小于5%时,就检测不出来。根据特征谱图就能推断出填料和涂料的无机物名称,做到鉴定快速、准确。8.1按7.2条的方法将适量的纸样炭化,燃烧成灰,取少量的灰用澳化钾压片,然后用红外分光光度计扫描,根据扫描所得红外谱图与标准谱图比较。如果样品中的无机填料和涂料是单组分的,扫描得到的谱图与该组分的无机物标准图谱相同,这样就很容易得出该无机物的名称(各种单组分的无机物红外谱图附后,以供参考)。如果无机填料和涂料是由二至三种无机物组成的混合物,那么各种成分的无机物均会在红外谱图上出峰,这样可以由红外谱图的峰形和出峰位置,进行有目标的推断其无机物名称(图16是一个碳酸钙与高岭土的重叠红外光谱图,而图12是一个硫酸钡与二氧化钦重叠的红外光谱图)。8.2碳酸盐与二氧化钦混合红外扫描图若是碳酸钙与二氧化钦混合,这时可以取7.2条得到的灰约0.lg,加2mol/L的盐酸溶液(4.4)lOmL溶解,若出现大量气泡,证明是碳酸盐,加热使碳酸盐溶解。过滤,用热水洗至不呈酸性[用甲基橙指示液(4.27)检查〕。滤液按7.6.5条的方法用化学法做钙的证实试验。而滤纸上的酸不溶物放在增锅中干燥、炭化,925℃灼烧成灰。将灰再用澳化钾压片进行红外光谱扫描,所得的谱图应该是碳酸盐的峰消失,谱图应与二氧化钦谱图相同而得到证实。8.3硅酸盐(高岭土或滑石粉)与二氧化钦若灰分的扫描谱图是硅酸盐与二氧化钦时,可以用两种方法来证实:a.3.1取纸灰0.lg,加入log的硫酸按和20mL的浓硫酸,盖上表面皿煮沸至少3min,使二氧化钦溶解,冷却后小心地倾入200mL的蒸馏水中,冷却过滤,滤液加30%过氧化氢(4.12)5mL,若出现黄色,则表示有二氧化钦存在,滤纸上的残渣经彻底洗净,再次烘干,灼烧成灰,将灰做红外扫描,这时二氧化钦的峰应消失,只保留硅酸盐的峰,与标准图比较,鉴别出是高岭土或是滑石粉。
GB/T2679.12一938.3.2取。.1g的灰按7.7.1条的方法用碳酸钠进行熔融,用1:1盐酸溶解,其溶液分别按7.6.3和.6.4条做镁或铝离子的证实试验,其沉淀一定是二氧化硅和二氧化钦的混合物。.4钦钙颜料(CaSO,-TA)从样品灰的红外谱图上若观察到钦钙颜料时,可以再取7.2条处理的纸灰。.lg,加1,1的盐酸溶液(4.3)20mL,加热煮沸,再加20mL水稀释,并过滤。先用稀盐酸(4.4)洗,再用热水洗至无酸性反应[用甲基橙指示液(4.27)做检查试验〕,滤液按7.6.5,7.6.1条的方法分别做钙的硫酸根的证实试验,残渣烘干、灼烧,按上述方法做二氧化钦红外光谱的证实试验。8.5钦钡颜料(BaSO,-TA)从样品灰的谱图上若观察出是钦钡颜料时,这只能用下列方法来进一步证实:其做法是取7.2条中的灰。.lg,按7.4.1条的方法将灰用硫酸按一浓硫酸加热溶解,冷却后,倾人到200mL的水中,若出现白色沉淀,则为硫酸钡,上层清液加5mL30%的过氧化氢应出现黄色,其深浅与二氧化钦的含量成正比。若将沉淀的硫酸钡过滤,洗涤、烘干、灼烧,其灰再次进行红外扫描,将出现硫酸钡的光谱图。8.6锌钡白(ZnS-BaSO,)样品的灰分经扫描,若出现锌钡白的谱图时,可以另取7.2条的灰。.Ig,加1,1的盐酸溶解,过滤,滤液按7.6.1条的方法做锌的证实试验,而硫化物按7.2条的方法做证实试验,残渣再次烧灰做红外光谱图并与硫酸钡谱图相比较。总之,红外光谱就是通过原试样的灰分进行红外扫描,然后由谱图的峰形,初步判断最可能含有的无机物组分,然后用化学的方法进行有针对性的分离,将其中的一个组分溶解,用定性法鉴定,而另一个组分仍然是固体沉淀,经干燥后再次扫描鉴定。20泣t(cm,)图1滑石粉(未灼烧)红外光谱图20D谊t(cm,)图2滑石粉(600℃以下灼烧)红外光谱图
GB/"r2679.12一93200彼盆(cm-")图3双面胶版印刷纸中的滑石粉(900℃灼烧)红外光谱图200故盆(c口一,)图4氧化镁红外光谱图200故.(mti4图5高岭土红外光谱图2阅吐傲(c口协图6纸中高岭土(600℃以下灼烧)红外光谱图
Gs/T2679.12一93图7两个结晶水的硫酸钙红外光谱图2呱彼ft(-,)图8纸中硫酸钙(600℃以下灼烧)红外光谱图20彼盆(c口一,)图9氧化锌红外光谱图200彼ot(cm图10装饰纸中的二氧化钦红外光谱图
Gs/T2679.12一93200故R(cm,)图n硫酸钡红外光谱图2门胜R(cm-`)图12硫酸钡加二氧化钦红外光谱图200tta(c口一)图13硫酸钙(600℃以下灼烧)红外光谱图图14开源碳酸钙红外光谱图
Gs/T2679.12一932阅吐.(c一,)图15卷烟纸中碳酸钙(600℃以下灼烧)红外光谱图2叨健.cc口,)图16无碳复写纸中的碳酸钙加高岭土(600℃以下灼烧)红外光谱图9原子吸收分光光度法原子吸收分光光度法主要用于测定金属离子,只要对样品稍加处理,可以在两种或两种以上金属离子共存的情况下,不进行分离,就可以对金属离子在其要求的条件下进行定性或定量测定。由定量测定的结果推算出该无机物的含量。9.1样品的处理如下。
GB/T2679.12一93样品灰分硫化物、亚硫酸盐碳酸盐、硫酸盐Caz+、Mgz+,Zn0+,AI"+9.2称取5g的试样于增涡中,炭化,575士25℃灼烧后,慢慢加入1:1盐酸溶液(4.3)20mL,经热水浴加热溶解,若溶液是橙清的,则有可能是硫化物、亚硫酸盐、碳酸盐、可溶硫酸盐、氧化物(ZnO)等。然后定量地移入容量瓶,根据原子吸收分光光度法,测定无机阳离子:Ca,Mg,AI,Zn等含量。9.3如果定性确定纸中填的滑石粉、高岭土、二氧化钦等,按9.2条处理,盐酸不能溶解这些无机物。只能用7.7条的方法用碳酸钠熔融后再用盐酸溶解,过滤,滤液中的阳离子Ca,Mg,Al用原子吸收仪进行测定。过滤的残渣留作9.4条测试用。9.4将9.3条中的盐酸不溶物,用7.4条的方法处理,即用硫酸钱和浓硫酸作溶剂。加热过程中二氧化钦会溶解,溶液变成黄色(说明含TiOi),溶解液经稀释后过滤,滤液按GB1291。做二氧化钦的定量测定,残渣移人铂柑祸,烘干,灼烧称重,这些硫酸不溶残渣可能是硫酸钡和二氧化硅的混合物。
GB/T2679.12一939.5向9.4条中的铂增祸内加入。15-1.OmL水润湿后,加1-2滴浓硫酸,然后再加2-5mL氟化氢,在水浴上蒸干后,移入高温炉中赶三氧化硫,并灼烧到质量恒定。此质量则为硫酸钡。由硫酸钡和二氧化硅的质量减去硫酸钡的质量,便可算出二氧化硅的质量。10试验报告试验报告应包括下列项目:a.本国家标准的编号;b.试验的地点和参考资料,c.使用方法(化学定性、红外光谱或原子吸收);d.完整鉴定样品所需的一切资料;e试验结果应包括检定出的阴、阳离子和原子团,红外测定要附有红外扫描谱图,并指出其量的大小,如:痕迹、少量、大量,相当大量等。根据观察到的现象及阴阳离子,推断出填料和涂料中所用的无机物名称。原子吸收光度法,还应该算出百分含量;f.未按标准规定的操作和可能影响测试结果的其他环境。附加说明:本标准由中华人民共和国轻工业部提出。本标准由全国造纸工业标准化技术委员会归口。本标准由轻工业部造纸工业科学研究所负责起草。本标准的主要起草人魏鹏月、杨妍飞、陈曦、陈述。本标准参照采用TAPPIT421om83《纸中无机填料和涂料的定性分析(包括光学显微镜法)》。'
您可能关注的文档
- GBT26779-2011燃料电池电动汽车加氢口.pdf
- GBT26780-2011压缩天然气汽车燃料系统碰撞安全要求.pdf
- GBT26781-2011海区浮动助航标志配布导则.pdf
- GBT26782.1-2011卫星导航船舶监管信息系统系统组成与功能定义.pdf
- GBT26782.2-2011卫星导航船舶监管信息系统系统信息交换协议.pdf
- GBT26782.3-2011卫星导航船舶监管信息系统船载终端技术要求.pdf
- GBT26784-2011建筑构件耐火试验可供选择和附加的试验程序.pdf
- GBT2679.1-93纸透明度的测定法.pdf
- GBT2679.11-2008纸和纸板中无机填料和无机涂料的定性分析电子显微镜X射线能谱法.pdf
- GBT26792-2011高效液相色谱仪.pdf
- GBT26796.4-2011用于工业测量与控制系统的EPA规范功能块的技术规范.pdf
- GBT26799-2011点胶机通用技术条件.pdf
- GBT268-1987石油产品残炭测定法(康氏法).pdf
- GBT26800-2011电导电极.pdf
- GBT26802.1-2011工业控制计算机系统通用规范通用要求.pdf
- GBT26802.3-2011工业控制计算机系统通用规范设备用图形符号.pdf
- GBT26802.5-2011工业控制计算机系统通用规范场地安全要求.pdf
- GBT26803.1-2011工业控制计算机系统总线总论.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明