- 688.00 KB
- 2023-01-01 08:31:21 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
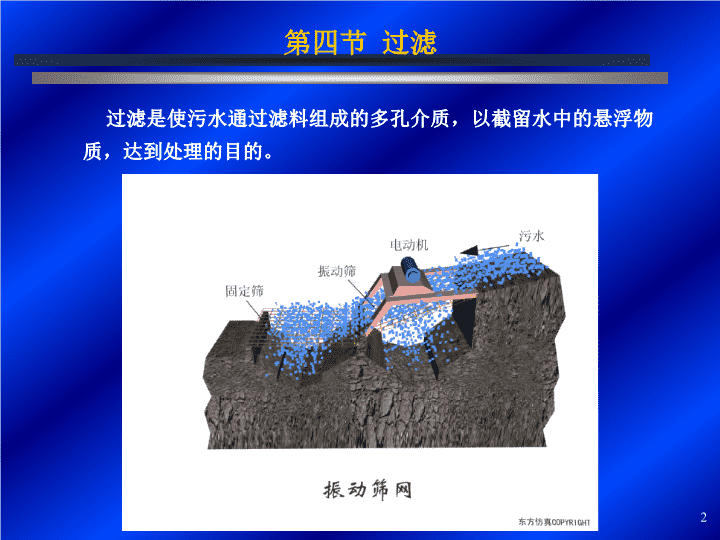
工业废水处理1\n第四节过滤过滤是使污水通过滤料组成的多孔介质,以截留水中的悬浮物质,达到处理的目的。2\n一、滤网滤网-污水中含有的细小悬浮物,不能用格栅去除,也难用沉淀去除,可采用小孔眼的滤网截留,回收。筛网通常用金属丝或化学纤维编制而成。其形式有转鼓式、转盘式、振动式、转帘带式和固定式倾斜筛多种。筛孔尺寸可根据需要,一般为0.15~1.0mm。常用旋转式滤网,污水从外侧流入内侧,悬浮物被截留,然后用刮刀刮下运走。优:效率高,可回收有用的物质。缺:易堵塞。3\n二、滤池滤池-去除微量悬浮物,深度处理。1.滤池过滤机理。1)机械筛滤作用-把滤料层作为筛子,某些粒径大于孔隙尺寸的杂质被截留,孔隙变小一些,于是后续的细小悬浮杂质也可被截留。2)沉淀作用-把滤料看作层层叠叠起来的多层沉淀池。利用巨大的沉淀面积截留水中微小粒子。3)絮凝作用-把滤料作为接触吸附介质,介质紧密排列,水在介质中流动时,杂质被吸附在介质表面并成长为大颗粒,巨大的表面积产生强烈的吸附能力。4\n2.截留杂质规律从接触絮凝作用考虑,杂质与滤料接触,被滤料表面分子间力吸附絮凝,同时水力冲刷可使絮凝杂质脱落向下层移动,被下层滤料截留。在过滤周期将终止时,表层滤料最细,吸附表面张力最大,截留的杂质最多,表层孔隙逐渐被杂质阻塞,尽管下层滤料还未发挥应有作用,但周期已终止,导致出现双层滤料,表层的滤料粒径大一些,截留的杂质多一些。二、滤池5\n3.构造-污水滤料和给水滤料有许多相同之处,与给水滤料的不同之处如下:滤料粒径大,强度高,耐腐蚀,成本低。抗冲击性负荷,出现双层滤料。运行周期长。运行方式分为正向流和反向流。4.滤料-石英砂、无烟煤、陶粒、聚丙烯球、炉灰渣、烟道灰、焦炭、电化学滤料。二、滤池6\n5.电化学滤料滤池原理-两种不同的金属直接接触,浸没在有传导性的电解质溶液里,可形成原电池,通过选用活性金属组成原电池可在它作用空间产生一个电场。电化学滤料滤池是利用污水中含有电解质物质,当铁屑浸没在含有电解质的污水中,铁屑晶体结构上的铁一碳之间形成了许多微小的腐蚀电池,产生电化学反应,在它的作用空间产生一个电场,铁一碳表面有电流流动,形成一种内部内电解反应,在电场作用下,铁阳极失去电子生成Fe2+进入污水中,碳阴极得到电子使碳表面的H+生成H2逸出,电极反应如下:二、滤池7\n阳极:2Fe—2Fe2++4e阴极:4H++4e—2H2(酸性溶液)O2+2H2O+4e—4OH-(中性溶液或碱性溶液)腐蚀电化学反应,在它的表面有电流流动,由于腐蚀原电池的作用,在电位较低的铁阳极上,金属铁失去电子变成铁离子进入溶液,电子流向阴极,在碳阴极附近,流来的电子被溶液中能够吸收电子的物质所接受,生成以氢氧根形式出现的阴离子,中和金属离子,形成一种内部电解反应。电极反应阴极新生成的H2能与污水中的许多污染组份发生氧化还原作用,阳极生成的Fe2+是良好的絮凝剂,能够捕集、裹挟污水中的污染物共沉。二、滤池8\n应用——采用铁屑和活性炭组成电池,由于电极电位不同,形成一组短路的电池,铁阳极失去电子生成Fe2+进入水中,电子流向阴极,在炭表面H+得到电子还原成H2,水中Fe2+与OH-结合形成Fe(OH)2絮凝体,电池不断反应,滤池强化工作作用。例如,将铁屑和碳粒浸没在ξ—电位为30mv的污水溶液中,铁屑和碳粒的电位差为1.2伏,粒料间的分离距离为0.1cm,可以得到5×10-3cm/s的分离速度,从理论上计算20s就完成沉积过程。特点:1)具有普通滤池的功能,2)具有原电池的电化学反应。3)起到电解反应的电氧化和电絮凝。二、滤池9\n三、微滤机可截留污水中微小的悬浮颗粒,滤布采用尼龙布和金属网,孔隙小于100μ,悬浮物去除率75-90%,滤后水中悬浮物小于5mg/L。10\n第五节中和定义:酸和碱反应生成盐和水称为中和反应11\n一、酸碱污水的产生1.酸性污水-化工厂、化纤厂、电镀厂,金属加工厂等酸性污水PH=1-4,腐蚀性强,改变水体的PH值,影响水生植物。2.碱性污水-印染厂、造纸厂、炼油厂的碱性污水PH=10-14,腐蚀危害小于酸性水,影响水生植物。酸碱污水在浓度高时3%-5%以上,应考虑回收和综合利用,制造硫酸亚铁、硫酸铁、在浓度不高时方可采用处理的方法。12\n二、中和剂1.酸性污水的中和剂苏打NaCO3和苛性钠NaOH具有组成均匀,易于贮存,反应迅速,易溶于水,但价格较高。石灰Ca(OH)2来源广泛,价格便宜。(但产生杂质多,浮渣多,难处理,一般用于水量较小的水厂)石灰石CaCO3,白云石CaCO3+MgCO3是开发的石料,在产地价格便宜,可以作为一种中和材料,主要用于滤床使用。2.碱性污水的中和剂-硫酸、盐酸、烟道气(含CO2,SO2)。13\n三、中和方法分类1.酸碱污水相互中和法电镀厂的酸性污水和印染厂的碱性污水相互混合,达到中和目的。根据化学反应等当量原理,Q1C1=Q2C2计算污水中酸碱的含量及污水量,使酸碱污水等当量混合,达到等当量中和并略偏于碱性。14\n2.药剂中和法用碱性、酸性物质为中和剂处理,常采用石灰处理酸性污水,石灰还是混凝剂,可凝聚水中的杂质,对于含杂质多的酸性污水有利。当污水中含有重金属离子时,加入石灰,碱性增大使水中重金属离子积大于溶度积产生沉淀。三、中和方法分类15\n药剂中和在混合池中进行,其后需设沉淀池和污泥干化,污水在混合反应池停留时间5分钟(给水反应池的停留时间是8-10分钟),在沉淀池停留时间1-2小时,污泥是污水的体积2%-5%,污泥需脱水干化。干投法-用机械将药剂粉碎,直径<0.5mm,然后直接投入水中。湿投法-将药剂溶解成液体,用计量设备控制投加量,可节省药剂。三、中和方法分类16\n3.过滤中和法(多用于原料所在地)使污水流经具有中和能力的滤池,例如石灰石、白云石、大理石等,产生中和作用。石灰石与硫酸反应白云石与硫酸反应白云石中含有,可生成溶解度较大的不会造成反应中滤池的堵塞,产生的是石灰石中和产生的50%,影响小一些,可以适当提高进水硫酸浓度。CaSO4三、中和方法分类17\n计算:石灰石与硫酸反应生成硫酸钙。9810013618生成硫酸钙微溶于水,18℃时溶解度为1.6g/L,采用石灰石能中和硫酸浓度为:1.6:136=x:98x=1.15g/L分析:1)当进水硫酸浓度大于1.15g/L,中和反应生成的CaSO4浓度大于1.6g/L,超过浓度积,会析出CaSO4沉淀。2)由于存在盐效应的过饱和现象,一般进水的硫酸浓度可提高到2.0-2.4g/L。3)应用中要注意进水的硫酸浓度,不使滤池堵塞。三、中和方法分类18\n4.碱性污水中和处理常用于酸性污水中和,或者采用投酸中和和烟道气中和碱性污水,碱性污水中和处理需具备采用方法的条件,投加酸中和方法简单,但是费用过高,烟道气体中和方便实用。烟道气中含有CO2和SO2,溶于水中形成H2CO3和H2SO4,使碱性污水被中和,烟道气体中和的方法有:1)将碱性污水作为湿法除尘的喷淋水。(给排水,暖通交叉)2)使烟道气通入碱性污水鼓泡中和。三、中和方法分类19\n第六节化学沉淀化学沉淀是向水中投加某种化学剂,使它与水中的溶解物质发生互换反应,生成难溶于水的沉淀物,降低污水中溶解物质的浓度。原理-根据化学沉淀的必要条件,一定温度下,难溶盐MmNn在饱和溶液下,沉淀和溶解反应如下。m、n-分别表示离子Mn+、Nm-的系数。根据质量作用原理,溶度积常数可表示为LMmNn20\n溶度积常数LMmNn的影响因素:1)同名离子效应-当沉淀溶解平衡后,如果向溶液中加入含有某一离子的试剂,则沉淀溶解度减少向沉淀方向移动→2)盐效应-在有强电解质存在状况下,溶解度随强电解质浓度的增大而增加,反应向溶解方向转移←。3)酸效应-溶液的PH值可影响沉淀物的溶解度,称为酸效应。4)络合效应-若溶液中存在可能与离子生成可溶性络合物的络合剂,则反应向相反方向进行,沉淀溶解,甚至不发生沉淀。应用:如果污水中含有大量的Mn+离子,要降低浓度,可向污水中投入化学物质,提高污水中Nm-浓度,使离子积大于溶度积L,结果MmNn从污水中沉淀折出,降低Mm+浓度。化学沉淀21\n一、氢氧化物沉淀法金属氢氧化物的溶解与污水的PH值关系很大。M(OH)n表示金属的氢氧化物,Mm+表示金属离子。则电离方程式其溶度积为同时水发生电离水的离子积为22\n代入上式将上式取对数将重金属离子的溶解度与PH值关系绘成曲线,从曲线中可以得到,重金属离子的浓度值。应用-采用氢氧化法处理污水,PH值是一个重要因素,处理污水中的Fe2+离子时,PH值大于9则可完全沉淀,而处理污水中AL3+离子时,PH值严格为5.5,否则AL(OH)3沉淀物又会溶解。一、氢氧化物沉淀法23\n二、硫化物沉淀法金属的硫化物溶解度一般比氢氧化物的溶解度小得多,可以采用硫化物沉淀法。电离方程式。采用硫化物沉淀法常用的药剂为硫化氢,硫化钠,硫化钾等。硫化氢在水中分两步电离。电离常数24\n由上二式可得总电离常数代入得在1大气压,25℃条件下,硫化氢在水中的饱和浓度为0.1M,则上式由上式可知,金属离子在水中溶解度与LMS和PH值有关二、硫化物沉淀法25\n三、钡盐沉淀法在处理含铬污水时,可用钡盐为沉淀剂,以碳酸钡为例,它与污水中铬酸进行反应,生成难溶的铬酸钡。碳酸钡是难溶的物质,但铬酸钡的溶度积更小一些,更难溶于水,象这样一种沉淀转化为另一种沉淀的过程为沉淀的转移。26\n四、分析1.沉淀和溶解是暂时的,有条件的。2.只要条件改变,沉淀和溶解就能相互转移。3.如果离子积大于溶度积就会发生沉淀。4.反之离子积小于溶度积就会溶解。27\n哈尔滨工业大学28