- 1001.50 KB
- 2022-04-22 11:34:10 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'琥珀课后资源网bbs.5hupo.com第二章饱和烃习题(P60)(一)用系统命名法命名下列各化合物,并指出这些化合物中的伯、仲、叔、季碳原子。(1)(2)3-甲基-3-乙基庚烷2,3-二甲基-3-乙基戊烷(3)(4)2,5-二甲基-3,4-二乙基己烷1,1-二甲基-4-异丙基环癸烷(5)(6)乙基环丙烷2-环丙基丁烷(7)(8)1,7-二甲基-4-异丙基双环[4.4.0]癸烷2-甲基螺[3.5]壬烷(9)(10)5-异丁基螺[2.4]庚烷新戊基(11)(12)2-甲基环丙基2-己基or(1-甲基)戊基(二)写出相当于下列名称的各化合物的构造式,如其名称与系统命名原则不符,予以改正。(1)2,3-二甲基-2-乙基丁烷(2)1,5,5-三甲基-3-乙基己烷(3)2-叔丁基-4,5-二甲基己烷
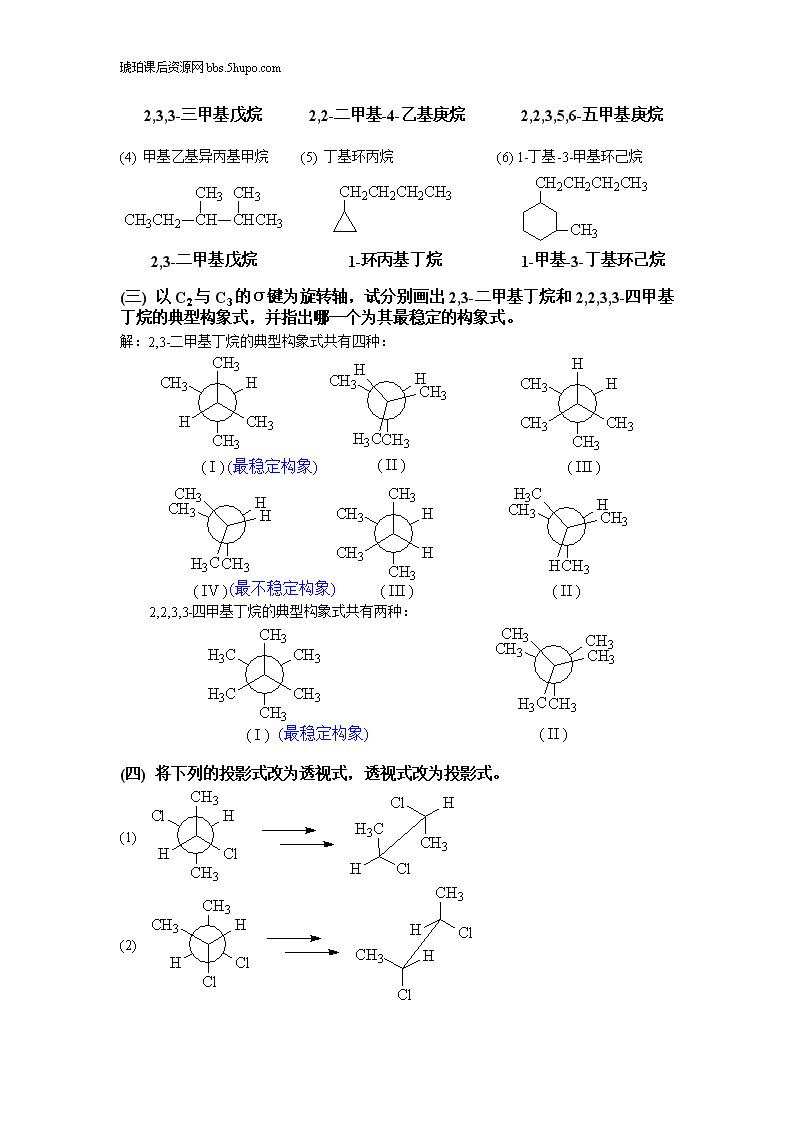
琥珀课后资源网bbs.5hupo.com2,3,3-三甲基戊烷2,2-二甲基-4-乙基庚烷2,2,3,5,6-五甲基庚烷(4)甲基乙基异丙基甲烷(5)丁基环丙烷(6)1-丁基-3-甲基环己烷2,3-二甲基戊烷1-环丙基丁烷1-甲基-3-丁基环己烷(三)以C2与C3的σ键为旋转轴,试分别画出2,3-二甲基丁烷和2,2,3,3-四甲基丁烷的典型构象式,并指出哪一个为其最稳定的构象式。解:2,3-二甲基丁烷的典型构象式共有四种:2,2,3,3-四甲基丁烷的典型构象式共有两种:(四)将下列的投影式改为透视式,透视式改为投影式。(1)(2)
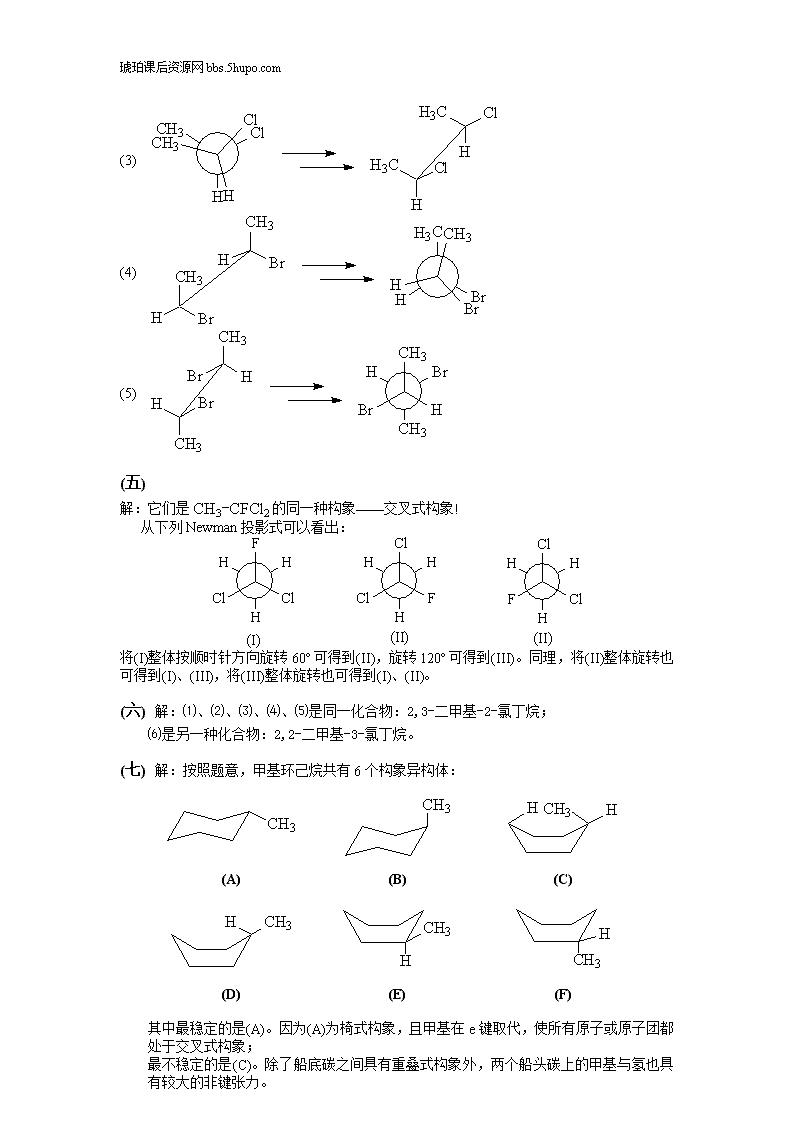
琥珀课后资源网bbs.5hupo.com(3)(4)(5)(五)解:它们是CH3-CFCl2的同一种构象——交叉式构象!从下列Newman投影式可以看出:将(I)整体按顺时针方向旋转60º可得到(II),旋转120º可得到(III)。同理,将(II)整体旋转也可得到(I)、(III),将(III)整体旋转也可得到(I)、(II)。(六)解:⑴、⑵、⑶、⑷、⑸是同一化合物:2,3-二甲基-2-氯丁烷;⑹是另一种化合物:2,2-二甲基-3-氯丁烷。(七)解:按照题意,甲基环己烷共有6个构象异构体:(A)(B)(C)(D)(E)(F)其中最稳定的是(A)。因为(A)为椅式构象,且甲基在e键取代,使所有原子或原子团都处于交叉式构象;最不稳定的是(C)。除了船底碳之间具有重叠式构象外,两个船头碳上的甲基与氢也具有较大的非键张力。
琥珀课后资源网bbs.5hupo.com(八)(1)解:沸点由高到低的顺序是:(2)(解:沸点由高到低的顺序是:F>G>E>H>D>C>B>A(3)解:沸点由高到低的顺序是:D>B>C>A(九)解:(1)(2)(3)(4)(十)解:(1)(2)(十一)解:设乙烷中伯氢的活性为1,新戊烷中伯氢的活性为x,则有:∴新戊烷中伯氢的活性是乙烷中伯氢活性的1.15倍。(十二)解:2,2,4-三甲基戊烷的构造式为:氯代时最多的一氯代物为;溴代时最多的一溴代物为这一结果说明自由基溴代的选择性高于氯代。即溴代时,产物主要取决于氢原子的活性;而氯代时,既与氢原子的活性有关,也与各种氢原子的个数有关。根据这一结果预测,异丁烷一氟代的主要产物为:FCH2CH2CH3(十三)解:自由基的稳定性顺序为:⑶>⑷>⑵>⑴(十四)解:反应机理:
琥珀课后资源网bbs.5hupo.com引发:增长:……终止:(十五)解:引发:增长:……终止:……第三章不饱和烃习题(P112)(一)用系统命名法命名下列各化合物:(1)(2)对称甲基异丙基乙烯3-甲基-2-乙基-1-丁烯4-甲基-2-戊烯(3)(4)2,2,5-三甲基-3-己炔3-异丁基-4-己烯-1-炔
琥珀课后资源网bbs.5hupo.com(一)用Z,E-标记法命名下列各化合物:(1)↓↑(2)↑↑(E)-2,3-二氯-2-丁烯(Z)-2-甲基-1-氟-1-氯-1-丁烯(3)↑↑(4)↑↑(Z)-1-氟-1-氯-2-溴-2-碘乙烯(Z)-3-异基-2-己烯(二)写出下列化合物的构造式,检查其命名是否正确,如有错误予以改正,并写出正确的系统名称。(1)顺-2-甲基-3-戊烯(2)反-1-丁烯顺-4-甲基-3-戊烯1-丁烯(无顺反异构)(3)1-溴异丁烯(4)(E)-3-乙基-3-戊烯2-甲基-1-溴丙烯3-乙基-2-戊烯(无顺反异构)(三)完成下列反应式:解:红色括号中为各小题所要求填充的内容。(1)(2)(3)(4)
琥珀课后资源网bbs.5hupo.com(硼氢化反应的特点:顺加、反马、不重排)(5)(6)(硼氢化反应的特点:顺加、反马、不重排)(7)(8)(9)(10)(11)(12)(13)(14)(五)用简便的化学方法鉴别下列各组化合物:(1)解:(2)
琥珀课后资源网bbs.5hupo.com解:(六)在下列各组化合物中,哪一个比较稳定?为什么?(1)(A),(B)解:(B)中甲基与异丙基的空间拥挤程度较小,更加稳定。(2)(A),(B)解:(A)中甲基与碳-碳双键有较好的σ-π超共轭,故(A)比较稳定。(3)(A),(B),(C)解:(C)的环张力较小,较稳定。(4)(A),(B)解:(A)的环张力较小,较稳定。(5)(A),(B),(C)解:(C)最稳定。(6)(A),(B)解:(A)的环张力很大,所以(B)较稳定。(七)将下列各组活性中间体按稳定性由大到小排列成序:(1)(2)解:(1)C>A>B(2)B>C>A(八)下列第一个碳正离子均倾向于重排成更稳定的碳正离子,试写出其重排后碳正离子的结构。解:题给碳正离子可经重排形成下列碳正离子:(1)(2)(3)(4)(九)解:可用Br2/CCl4或者KMnO4/H2O检验溶剂中有无不饱和烃杂质。若有,可用浓硫酸洗去不饱和烃。(十)写出下列各反应的机理:(1) 解:
琥珀课后资源网bbs.5hupo.com(2) 解:(3) 解:该反应为自由基加成反应:引发:增长:……终止:略。(4)解:(箭头所指方向为电子云的流动方向!)(十一)解:(1)双键中的碳原子采取sp2杂化,其电子云的s成分小于采取sp杂化的叁键碳,离核更远,流动性更大,更容易做为一个电子源。所以,亲电加成反应活性:>(2)解释:在进行催化加氢时,首先是H2及不饱和键被吸附在催化剂的活性中心上,而且,叁键的吸附速度大于双键。所以,催化加氢的反应活性:叁键>双键。(3)解释:叁键碳采取sp杂化,其电子云中的s成分更大,离核更近,导致其可以发生亲核加成。而双键碳采取sp2杂化,其电子云离核更远,不能发生亲核加成。(4)解释:双键上电子云密度更大,更有利于氧化反应的发生。(5)解释:氧化反应总是在电子云密度较大处。(6)解释:C+稳定性:3°C+>2°C+
琥珀课后资源网bbs.5hupo.com(十二)写出下列反应物的构造式:(1)(2)(3)(4)(5)(6)(十三)(1)所以,该反应能够发生。(2)所以,该反应不能发生。(3)所以,该反应不能发生。(4)所以,该反应不能发生。(十四)给出下列反应的试剂和反应条件:(1)1-戊炔→戊烷解:(2)3-己炔→顺-3-己烯解:(3)2–戊炔→反-2-戊烯解:
琥珀课后资源网bbs.5hupo.com(4)解:(十五)完成下列转变(不限一步):(1)解:(2)解:(3)解:(4)解:(十六)由指定原料合成下列各化合物(常用试剂任选):(1)由1-丁烯合成2-丁醇解:(2)由1-己烯合成1-己醇解:(3)解:(4)由乙炔合成3-己炔解:(5)由1-己炔合成正己醛 解:(6)由乙炔和丙炔合成丙基乙烯基醚解:
琥珀课后资源网bbs.5hupo.com(十七)解释下列事实:(1)1-丁炔、1-丁烯、丁烷的偶极矩依次减小,为什么?解:电负性:>>键的极性:>>分子的极性:1-丁炔>1-丁烯>丁烷(即:1-丁炔、1-丁烯、丁烷的偶极矩依次减小)(2)普通烯烃的顺式和反式异构体的能量差为4.18kJ•mol-1,但4,4-二甲基-2-戊烯顺式和反式的能量差为15.9kJ•mol-1,为什么?解:顺-4,4-二甲基-2-戊烯反-4,4-二甲基-2-戊烯由于叔丁基的体积大,空间效应强,导致在顺-4,4-二甲基-2-戊烯中,叔丁基与甲基处于双键同侧,空间障碍特别大,能量更高。(3)解:炔烃分子中的叁键碳采取sp杂化。与sp2、sp3杂化碳相比,sp杂化s成分更多,电子云离核更近,受核的束缚更强,电负性更大。由于sp杂化碳的电子云离核更近,使乙炔中的键键能增大、键长缩短;由于sp杂化碳的电负性更大,使中的电子云更偏向碳原子一边,导致乙炔分子中氢原子更容易以H+的形式掉下来,酸性增强。(4)解:烯烃、炔烃与卤素的加成反应是亲电加成,不饱和键上的电子云密度越大,越有利于亲电加成。由于炔烃中的叁键碳采取sp杂化,电负性较大。所以,炔烃与卤素加成时,比烯烃加卤素困难,反应速率也小于烯烃。(5)解:不矛盾。烯烃与Br2、Cl2、HCl的加成反应都是亲电加成。由于双键碳的电负性小于叁键碳,导致双键上的π电子受核的束缚程度更小,流动性更大,更有利于亲电加成反应。所以,与亲电试剂Br2、Cl2、HCl的加成反应,烯烃比炔烃活泼而、都是吸电子基,它们的引入,导致双键上电子云密度降低,不利于亲电加成反应的进行。所以,当炔烃用亲电试剂Br2、Cl2、HCl处理时,反应却很容易停止在烯烃阶段,生成卤代烯烃,需要更强烈的条件才能进行第二步加成(6)解:溴与乙烯的加成是亲电加成反应,首先生成活性中间体——环状溴翁正离子。后者可与硝酸根负离子结合得到硝酸-β-溴代乙酯(BrCH2CH2ONO2):
琥珀课后资源网bbs.5hupo.com(7)解:该实验现象与烯烃酸催化下的水合反应机理有关:(2°C+)(3°C+)与(C)相关的C+为(1°C+),能量高,不稳定,因此产物(C)不易生成。(8)解:以自由基聚合为例。若按头尾相接的方式,生成甲基交替排列的整齐聚合物,则与之相关的自由基都是二级自由基:二级自由基二级自由基二级自由基头尾相接、甲基交替排列的整齐聚合物反之,则会生成稳定性较差的一级自由基:二级自由基一级自由基丙烯在酸催化下进行聚合反应,其活性中间体为碳正离子,其稳定性顺序同样为:三级>二级>一级碳正离子。(十八)解:(A)(B)(C)或反应式略。(十九)分子式为C4H6的三个异构体(A)、(B)、(C),可以发生如下的化学反应:试写出化合物(A)、(B)和(C)的构造式,并写出有关的反应式。解:(A)(B)(C)有关的反应式略。
琥珀课后资源网bbs.5hupo.com(二十)解:(二十一)解:各步反应式:(二十二)解:C7H15Br的结构为:(A)~(E)的结构式:将(A)、(B)、(C)分别经臭氧化-还原水解后,测定氧化产物的结构,也可推断(A)、(B)、(C)的结构:
琥珀课后资源网bbs.5hupo.com(二十三)解:各步反应式:(二十四)解:(二十五)解:各步反应式:第四章二烯烃和共轭体系习题(P147)(一)用系统命名法命名下列化合物:(1)(2)
琥珀课后资源网bbs.5hupo.com4-甲基-1,3-戊二烯2-甲基-2,3-戊二烯(3)(4)2-甲基-1,3,5-己三烯(3Z)-1,3-戊二烯(二)下列化合物有无顺反异构现象:若有,写出其顺反异构体并用Z,E-命名法命名。解:(1)无;(2)有;(3E)-1,3-戊二烯,(3Z)-1,3-戊二烯;(3)有;(3Z,5Z)-3,5-辛二烯,(3Z,5E)-3,5-辛二烯,(3E,5E)-3,5-辛二烯;(4)有;(3E)-1,3,5-己三烯,(3Z)-1,3,5-己三烯;(5)无(三)完成下列反应式:解:红色括号中为各小题所要求填充的内容。(1)(2)(3)(4)(5)(6)(7)(8)
琥珀课后资源网bbs.5hupo.com(9)(10)(四)给出下列化合物或离子的极限结构式,并指出哪个贡献最大?(2)(3)(4)(5)(6)解:(1)贡献最大(非电荷分离)(2)结构相似,二者贡献一样大(3)结构相似,二者贡献一样大(4)各共振结构式结构相似,能量相同,对真实结构的贡献相同。(5)贡献最大(与电负性预计相同)(6)贡献最大(共价键最多)(五)解:的真实结构可用共振论表示如下:其中(II)对真实结构的贡献就是使C=C双键带部分正电荷,电子云密度降低。
琥珀课后资源网bbs.5hupo.com的真实结构可用共振论表示如下:其中(II)对真实结构的贡献就是使C=C双键带部分负电荷,电子云密度升高。(六)解释下列反应:解:(1)(2)……(七)解:该二烯烃的构造式为:2,4-己二烯各步反应式略。(八)解:由于C+稳定性:所以,只有与相关的产物生成:
琥珀课后资源网bbs.5hupo.com(九)解:(十)下列各组化合物分别与HBr进行亲电加成反应,哪个更容易?试按反应活性大小排列顺序。解:(1)反应活性顺序:>>>(考虑C+稳定性!)(2)反应活性顺序为:1,3-丁二烯>2-丁烯>2-丁炔(考虑C+稳定性!)(十一)解:反应活性:(1)B>C>A; (2)A>B>C(C难以形成s-顺式构型,不反应)(十二)试用简单的化学方法鉴别下列各组化合物:(1)己烷,1-己烯,1-己炔,2,4-己二烯(2)庚烷,1-庚炔,1,3-庚二烯,1,5-庚二烯解:(1)(2)(十三)选用适当原料,通过Diels-Alder反应合成下列化合物。解:(1)
琥珀课后资源网bbs.5hupo.com(2)(3)(4)(5)(6)(十四)解:(A)(B)or(C)(十五)根据以上事实,试推测该二聚体的构造式,并写出各步反应式。解:该二聚体的构造式为:各步反应式略。第五章芳烃芳香性(一)写出分子式为C9H12的单环芳烃的所有同分异构体并命名。解:
琥珀课后资源网bbs.5hupo.com(二)命名下列化合物:解:(1)3-对甲苯基戊烷(2)(Z)-1-苯基-2-丁烯(3)4-硝基-2-氯甲苯(4)1,4-二甲基萘(5)8-氯-1-萘甲酸(6)1-甲基蒽(7)2-甲基-4-氯苯胺(8)3-甲基-4羟基苯乙酮(9)4-羟基-5-溴-1,3-苯二磺酸(三)完成下列各反应式:解:红色括号中为各小题所要求填充的内容。(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)(11)(12)
琥珀课后资源网bbs.5hupo.com(13)(14)(15)(16)(四)用化学方法区别下列各组化合物:(1)环己烷、环己烯和苯(2)苯和1,3,5-己三烯解:(1)(2)(五)写出下列各反应的机理:解:(2)解:(3)解:
琥珀课后资源网bbs.5hupo.com(4)(六)解:由于氧和氮的电负性均大于碳,在亚硝基苯中存在下列电动去的转移:所以亚硝基苯(Ph—NO)进行亲电取代反应时,其活性比苯小,—NO是第二类定位基。(七)写出下列各化合物一次硝化的主要产物:解:蓝色箭头指向为硝基将要进入的位置:(1)(2)(3)(4)(5)(6)(7)(8)(9)(10)(11)(12)
琥珀课后资源网bbs.5hupo.com(13)(14)(15)(16)(17)(18)讨论:A.(10)的一元硝化产物为而不是,因为与前者相关的σ-络合物中正电荷分散程度更大,反应活化能更低:B.(13)的一元硝化产物为而不是,是因为前者的空间障碍小,热力学稳定。(八)利用什么二取代苯,经亲电取代反应制备纯的下列化合物?解:可用下列二取代苯分别制备题给的各化合物:(1)(2)(3)(4)(九)将下列各组化合物,按其进行硝化反应的难易次序排列:(1)苯、间二甲苯、甲苯 (2)乙酰苯胺、苯乙酮、氯苯
琥珀课后资源网bbs.5hupo.com解:(1) 间二甲苯>甲苯>苯 解释:苯环上甲基越多,对苯环致活作用越强,越易进行硝化反应。 (2)乙酰苯胺>氯苯>苯乙酮解释:连有致活基团的苯环较连有致钝集团的苯环易进行硝化反应。对苯环起致活作用的基团为:—NH2,—NHCOCH3且致活作用依次减小。对苯环起致钝作用基团为:—Cl,—COCH3且致钝作用依次增强。(十)比较下列各组化合物进行一元溴化反应的相对速率,按由大到小排列。解:(1)一元溴化相对速率:甲苯>苯>溴苯>苯甲酸>硝基苯解释:致活基团为—CH3;致钝集团为—Br,—COOH,—NO2,且致钝作用依次增强。(2)间二甲苯>对二甲苯>甲苯>对甲基苯甲酸>对苯二甲酸解释:—CH3对苯环有活化作用且连接越多活化作用越强。两个甲基处于间位的致活效应有协同效应,强于处于对位的致活效应;—COOH有致钝作用。(十一)解:这是-F、-Cl、-Br的吸电子效应与苄基中―CH2―的给电子效应共同作用的结果。电负性:F>Cl>Br>H邻、对位电子云密度:甲苯>苄基溴>苄基氯>苄基氟新引入硝基上邻、对位比例:甲苯>苄基溴>苄基氯>苄基氟新引入硝基上间位比例:甲苯<苄基溴<苄基氯<苄基氟(十二)解:硝基是强的吸电子基(-I、-C),它使苯环上电子云密度大大降低,新引入基上间位。(十三)甲苯中的甲基是邻对位定位基,然而三氟甲苯中的三氟甲基是间位定位基。试解释之。解:由于氟的电负性特别大,导致F3C-是吸电子基,对苯环只有吸电子效应,而无供电子效应,具有间位定位效应。(十四)在AlCl3催化下苯与过量氯甲烷作用在0℃时产物为1,2,4-三甲苯,而在100℃时反应,产物却是1,3,5-三甲苯。为什么?解:前者是动力学控制反应,生成1,2,4-三甲苯时反应的活化能较低;后者是热力学控制反应,得到的1,3,5-三甲苯空间障碍小,更加稳定。(十五)解:高温条件下反应,有利于热力学稳定的产物(间甲苯磺酸)生成。(十六)将下列化合物按酸性由大到小排列成序:(1)(2)(3)(4)(5)解:(3)>(1)>(5)>(2)>(4)
琥珀课后资源网bbs.5hupo.com各化合物失去H+后得到的碳负离子稳定性顺序为:(3)>(1)>(5)>(2)>(4)。碳负离子越稳定,H+越易离去,化合物酸性越强。(十七)下列反应有无错误?若有,请予以改正。(1)解:错。右边苯环由于硝基的引入而致钝,第二个硝基应该进入电子云密度较大的、左边的苯环,且进入亚甲基的对位。(2)解:错。FCH2CH2CH2+在反应中要重排,形成更加稳定的2º或3º碳正离子,产物会异构化。即主要产物应该是:若用BF3作催化剂,主要产物为应为(3)解:错。①硝基是致钝基,硝基苯不会发生傅-克酰基化反应;②用Zn-Hg/HCl还原间硝基苯乙酮时,不仅羰基还原为亚甲基,而且还会将硝基还原为氨基。(4)解:错。CH2=CHCl分子中-Cl和C=C形成多电子p—π共轭体系,使C—Cl具有部分双键性质,不易断裂。所以该反应的产物是PhCH(Cl)CH3。(十八)用苯、甲苯或萘等有机化合物为主要原料合成下列各化合物:解:(1)(2)(3)(4)
琥珀课后资源网bbs.5hupo.com(5)(6)(7)(8)(9)(10)(十九)解:乙酰苯胺溴化时,溴原子引入2-或4-所形成的活性中间体σ-络合物的稳定性大于上3-时:
琥珀课后资源网bbs.5hupo.com2,6-二甲基乙酰苯胺溴化时,溴原子引入3-所形成的活性中间体σ-络合物的稳定性更强:(二十)解:(二十一)解:由实验式及相对分子质量知,该烃的分子式为C16H16,不饱和度为9,故该烃分子中可能含有2个苯环和一个双键。由氧化产物知,该烃的结构为:
琥珀课后资源网bbs.5hupo.com(二十二)解:C9H12的构造式为:各步反应式:(C)的一对对映体:(二十三)解:各步反应式略。(二十四)解:(1)、(3)、(6)、(8)有芳香性。(1)、(3)、(8)中的π电子数分别为:6、10、6,符合Huckel规则,有芳香性;(6)分子中的3个苯环(π电子数为6)及环丙烯正离子(π电子数为2)都有芳香性,所以整个分子也有芳香性;(2)、(4)、(7)中的π电子数分别为:8、12、4,不符合Huckel规则,没有芳香性;(5)分子中有一个C是sp3杂化,整个分子不是环状的离域体系,也没有芳香性。(二十五)下列各烃经铂重整会生成那些芳烃?(1)正庚烷(2)2,5-二甲基乙烷解:(1)(2)第六章立体化学(一)在氯丁烷和氯戊烷的所有异构体中,哪些有手性碳原子?解:氯丁烷有四种构造异构体,其中2-氯丁烷中有手性碳:氯戊烷有八种构造异构体,其中2-氯戊烷(C2*),2-甲基-1-氯丁烷(C2*),2-甲基-3-氯丁烷(C3*)有手性碳原子:
琥珀课后资源网bbs.5hupo.com(二)各写出一个能满足下列条件的开链化合物:解:(1)(2)(三)解:和和(四)解:不饱和烃是或,生成的饱和烃无旋光性。(五)比较左旋仲丁醇和右旋仲丁醇的下列各项:(1)沸点(2)熔点(3)相对密度(4)比旋光度(5)折射率(6)溶解度(7)构型解:(1)、(2)、(3)、(5)、(6)相同;(4)大小相同,方向相反;(7)构型互为对映异构体。(六)解:(1)、(3)、(4)和题中所给的乳酸相同,均为R-型;(2)为S-型。提示:①在Fischer投影式中,任意两个基团对调,构型改变,对调两次,构型复原;任意三个基团轮换,构型不变。②在Fischer投影式中,如果最小的基团在竖键上,其余三个基团从大到小的顺序为顺时针时,手性碳的构型为R-型,反之,为S-型;如果最小的基团在横键上,其余三个基团从大到小的顺序为顺时针时,手性碳的构型为S-型,反之,为R-型;(七)解:S-型。(2)、(3)、(4)和它是同一化合物。(八)解:3-甲基戊烷进行氯化,可以得到四种一氯代物。其中:3-甲基-1-氯戊烷有一对对映体:3-甲基-2-氯戊烷有两对对映体:
琥珀课后资源网bbs.5hupo.com(1)(2)(3)(4)(1)和(2)是对映体,(3)和(4)是对映体;(1)和(3)、(2)和(3)、(1)和(4)、(2)和(4)、是非对映体。(九)解:第二次观察说明,第一次观察到的α是+2.30°,而不是-357.7°。(十)解:(1)(A)(B)(C)(D)(E)(2)以上各产物都有旋光性。(3)全部都有同样的构型关系。(4)都不能预测。(十一)解:(1)四种:(2)八种;(3)八种(十二)解:(1)Yes(2)No(3)No(4)Yes(5)No(6)No,四种立体异构体等量混合物无旋光性(十三)解:有四种立体异构体:(A)(B)(C)(D)
琥珀课后资源网bbs.5hupo.com(A)和(C),(B)和(D)是对映异构体;(A)和(D)或(B),(B)和(C)或(A)是非对映异构体;(A)和(B),(C)和(D)是顺反异构体。(十四)解:分子中有两处可产生构型异,一处为双键,可产生顺反异构,另一处为手性碳,可产生旋光异构。其中:(I)和(II)、(II)和(IV)是对映体;(I)和(III)、(I)和(IV)、(II)和(III)、(II)和(IV)是非对映体;(I)和(III)、(II)和(IV)是顺反异构体。(十五)解:(十六)某烃分子式为C10H14,有一个手性碳原子,氧化生成苯甲酸。试写出其结构式。解:C10H14的结构式为:(十七)解:
琥珀课后资源网bbs.5hupo.com(十八)解:(A)(B)(十九)解:(A)(B)(C)第七章(一)写出下列分子式所代表的所有同分异构体,并用系统命名法命名。(1)C5H11Cl(并指出1°,2°,3°卤代烷)(2)C4H8Br2(3)C8H10Cl解:(1)C5H11Cl共有8个同分异构体:(2)C4H8Br2共有9个同分异构体:
琥珀课后资源网bbs.5hupo.com(3)C8H10Cl共有14个同分异构体:(二)用系统命名法命名下列化合物。(1)(2)(3)(4)(5)(6)
琥珀课后资源网bbs.5hupo.com(三) 1,2-二氯乙烯的(Z)-和(E)-异构体,哪一个熔点较高?哪一个沸点较高?为什么?解:熔点:沸点:原因:顺式异构体具有弱极性,分子间偶极-偶极相互作用力增加,故沸点高;而反式异构体比顺式异构体分子的对称性好,它在晶格中的排列比顺式异构体紧密,故熔点较高。(四)解:(1)(A)>(B)>(D)>(C)(C)为对称烯烃,偶极矩为0(2)(B)>(C)>(A)。(五)解:(六)完成下列反应式:解:红色括号中为各小题所要求填充的内容。(1)(2)(3)(4)(5)
琥珀课后资源网bbs.5hupo.com(6)(7)解释:(8)(9)(10)(11)(12)(13)(14)
琥珀课后资源网bbs.5hupo.com(15)(16)(七)在下列每一对反应中,预测哪一个更快,为什么?(1)解:B>A。I-的离去能力大于Cl-。(2)解:B>A。中β-C上空间障碍大,反应速度慢。(3)解:A>B。C+稳定性:CH3CH=CHCH2+ > CH2=CHCH2CH2+(4)解:A>B 。反应A的C+具有特殊的稳定性:(5)解:A>B。亲核性:SH->OH-。(6)解:B>A。极性非质子溶剂有利于SN2。(P263)(八)将下列各组化合物按照对指定试剂的反映活性从大到小排列成序。(1)在2%AgNO3-乙醇溶液中反应:(A)1-溴丁烷(B)1-氯丁烷(C)1-碘丁烷(C)>(A)>(B)(2)在NaI-丙酮溶液中反应:(A)3-溴丙烯(B)溴乙烯(C)1-溴乙烷(D)2-溴丁烷(A)>(C)>(D)>(B)(3)在KOH-醇溶液中反应:(A)>(B)>(C)(九)用化学方法区别下列化合物(1)解
琥珀课后资源网bbs.5hupo.com(2)解:(3)(A)(B)(C)解:(1)1-氯丁烷,1-碘丁烷,己烷,环己烯解:(5)(A)2-氯丙烯(B)3-氯丙烯(C)苄基氯(D)间氯甲苯(E)氯代环己烷解:(十)完成下列转变[(2)、(3)题的其它有机原料可任选]:(1)解:(2)解:
琥珀课后资源网bbs.5hupo.com或:(3)解:(4)解:(5)解:(6)解:(十一)在下列各组化合物中,选择能满足各题具体要求者,并说明理由。(1)下解:(B)。-NO2的吸电子共轭效应使对位氟的活性大增。(2)下列哪一个化合物在乙醇水溶液中放置,能形成酸性溶液?(A)(B)解:(A)。苄基型C-X键活性远远大于苯基型(苄基型C+具有特殊的稳定性)。(3)下列哪一个与KNH2在液氨中反应,生成两种产物?(A)(B)(C)解:(B)。
琥珀课后资源网bbs.5hupo.com(十二)由1-溴丙烷制备下列化合物:(1)异丙醇解:(2)1,1,2,2-四溴丙烷解:(3)2-溴丙烯解:由(2)题得到的(4)2-己炔解:[参见(2)](5)2-溴-2-碘丙烷解:[参见(2)](十三)由指定原料合成:(1)解:(2)
琥珀课后资源网bbs.5hupo.com解:(3)解:(4)解:(十四)由苯和/或甲苯为原料合成下列化合物(其他试剂任选):(1)解:(2)解:或者:(3)解:
琥珀课后资源网bbs.5hupo.com(4)解:(十五)解:(十六) 解:(1)由苯和乙烯合成:(1)由甲苯合成:(十七)回答下列问题:(1)解:CH3Br和C2H5Br是伯卤代烷,进行碱性水解按SN2机理进行。增加水的含量,可使溶剂的极性增大,不利于SN2;(CH3)3CCl是叔卤代烷,水解按SN1机理进行。,增加水的含量,使溶剂的极性增大,有利于SN1;(2)解:(CH3)3CCH2X在进行SN1反应时,C-X键断裂得到不稳定的1ºC+:(CH3)3CC+H2,所以SN1反应速度很慢;(CH3)3CCH2X在进行SN2反应时,α-C上有空间障碍特别大的叔丁基,不利于亲核试剂从背面进攻α-C,所以SN2速度也很慢。(3)解:在浓的乙醇钠的乙醇溶液中,反应均按SN2机理进行,无C+,无重排;在乙醇溶液中加热,反应是按照SN1机理进行的,有C+,有重排:
琥珀课后资源网bbs.5hupo.com(4)解:几种烯丙基氯在含少量水的甲酸(HCOOH)中的溶剂解反应教都是按照SN1机理进行的。各自对应的C+为:稳定性:(II)’>(IV)’>(I)’>(III)’(5)解:亲核性:(B)>(C)>(A)原因:三种亲核试剂的中心原子均是氧,故其亲核性顺序与碱性一致。(6)解:I-是一个强的亲核试剂和好的离去基团:亲核性:I->OH-;离去能力:I->Cl-(7)解:增加水的含量,减少碱的浓度。(8)解:1,2-二苯基-1-氯丙烷的构造:苏型的反应:赤型的反应:以上的结果说明,E2反应的立体化学是离去基团与β-H处于反式共平面。(9)解:顺式较快。因为其过渡态能量较低:
琥珀课后资源网bbs.5hupo.com(10)解:因为二者可生成相同的苯炔中间体:(十八)解:(十九)解:(二十)解:(二十一)解:
琥珀课后资源网bbs.5hupo.com两步反应均按SN2机理进行,中心碳原子发生两次构型翻转,最终仍保持R-型。(二十二)解:(二十三)解:(二十四)解:'
您可能关注的文档
- 结构和性质相关分析与功能》第三版_课本答案全_主编傅建熙_.doc
- 《有机化学》 习题答案.doc
- 《有机化学》中国农业出版社 课后习题答案.doc
- 《有机化学》习题及思考题答案.pdf
- 《有机化学》习题答案(汪小兰主编).pdf
- 《有机化学》习题答案.doc
- 《有机化学》第四版(高鸿宾)课后习题答案 高等教育出版社.doc
- 《有机化学》第四版(高鸿宾)课后习题答案.doc
- 《有机化学》第四版. 高鸿宾版 课后练习答案.doc
- 》第四版._高鸿宾版_课后练习答案.doc
- 》第四版[1]._高鸿宾版_课后练习答案(新).doc
- 》第四版[1]._高鸿宾版_课后练习答案.doc
- 》第四版_习题答案_高等教育出版社[1].doc
- 《期货投资分析》习题集附答案.doc
- 《机械制图》习题集整理(答案和题目已分开).doc
- 《机械制图习题集》(第四版)N2(一)答案.pdf
- 《机械制造工艺学》试题库及答案.doc
- 《机械制造技术基础》习题与解答.doc
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明