- 1.70 MB
- 2022-04-22 13:34:49 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
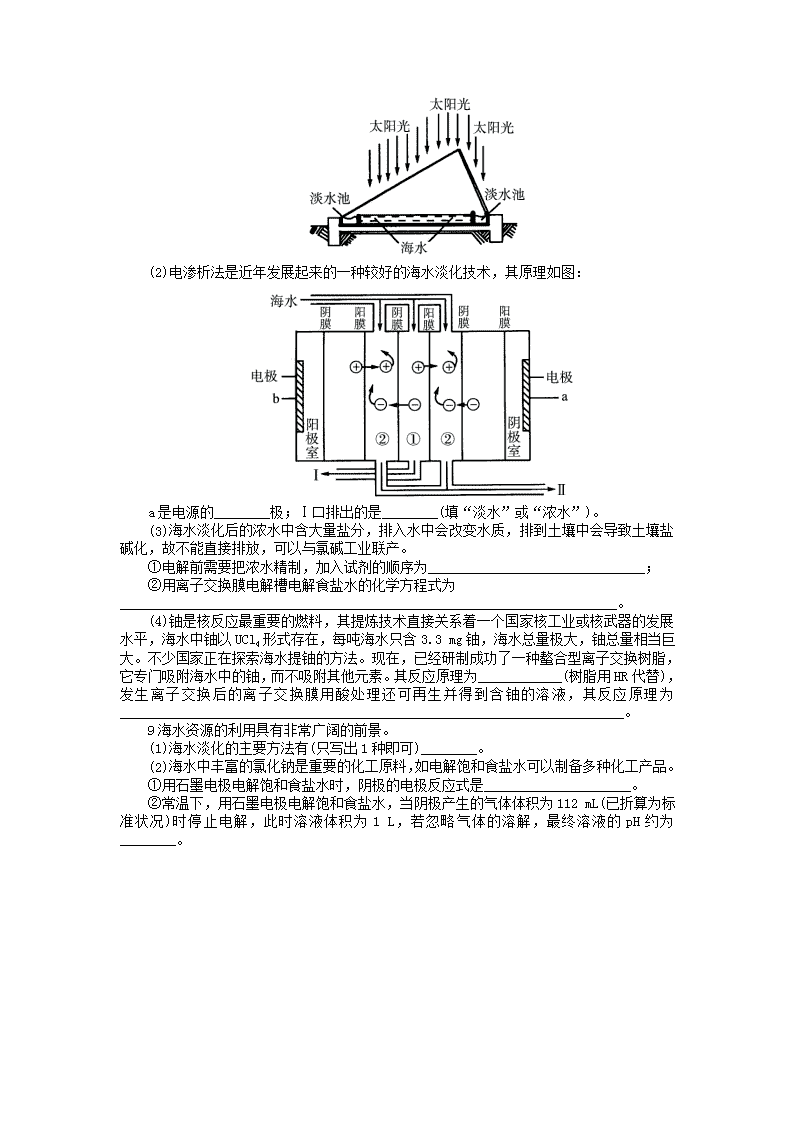
'2019-2020年高中化学专题一多样化的水处理技术第三单元海水淡化课后训练苏教版选修1化学与科技、社会、生产密切结合,下列有关说法不正确的是( )。A.“乙醇汽油”的广泛使用能有效减少有害气体的排放B.“无磷洗涤剂”的推广使用,能有效减少水体富营养化的发生C.“无氟冰箱”取代“含氟冰箱”,对人类的保护伞——臭氧层起到保护作用D.“海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化2若实行海水淡化供应饮用水,下列方法在原理上完全不可行的是( )。A.用明矾使海水中的盐分沉淀而淡化B.利用太阳能使海水蒸馏而淡化C.将海水缓慢凝固以获取淡化的饮用水D.将海水通过离子交换树脂,以除去所含盐分的离子3下列关于水的说法正确的是( )。A.电解水实验用的是交流电B.水是由氢气和氧气组成的C.水是由氢元素和氧元素组成的D.海水是蓝色的,湖水是绿色的,所以水具有多种颜色4下列说法中,不正确的是( )。A.蒸馏法淡化海水是将水加热至105℃蒸发汽化,然后将蒸气冷凝而得到蒸馏水的方法B.天然水里一般溶有Ca2+、Mg2+等金属阳离子,我们把溶有较多量Ca2+、Mg2+的水称为硬水C.阳离子交换树脂中的H+可与水中的金属阳离子Mn+交换D.阴离子交换树脂中既含有阳离子,又含有阴离子,因此既能与水中的阳离子交换,又能与水中的阴离子交换5生产、生活离不开各种化学物质,下列说法不正确的是( )。A.不需要通过化学反应就能从海水中获得食盐和淡水B.潜水艇在紧急情况下可用过氧化钠供氧C.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂D.工业上常用硅制造光导纤维6《科学》评出2004年10大科技突破,其中“火星上‘找’到水的影子”名列第一。下列关于水的说法中错误的是( )。A.用膜分离的方法可以使海水淡化B.高效催化剂可使水分解,同时释放能量C.密度小于1g·cm-3的溶液,浓度越大,密度越小D.金属的电化学腐蚀中,水参与了正极反应7下列说法不正确的是( )。A.海水淡化的主要方法有蒸馏法、电渗析法、离子交换法、反渗透法B.海水中溶解的主要无机盐有NaCl、MgCl2、KCl、MgSO4等物质C.海水综合利用,可将海水淡化与制食盐及氯碱工业、镁工业、钾工业、溴工业等形成联合工业体D.海水淡化因能耗大,成本高,不能形成规模化生产8地球的海水总量约有1.4×1018t,是人类最大的资源库。(1)如图利用海水得到淡水的方法为________。
(2)电渗析法是近年发展起来的一种较好的海水淡化技术,其原理如图:a是电源的________极;Ⅰ口排出的是________(填“淡水”或“浓水”)。(3)海水淡化后的浓水中含大量盐分,排入水中会改变水质,排到土壤中会导致土壤盐碱化,故不能直接排放,可以与氯碱工业联产。①电解前需要把浓水精制,加入试剂的顺序为_______________________________;②用离子交换膜电解槽电解食盐水的化学方程式为_______________________________________________________________________。(4)铀是核反应最重要的燃料,其提炼技术直接关系着一个国家核工业或核武器的发展水平,海水中铀以UCl4形式存在,每吨海水只含3.3mg铀,海水总量极大,铀总量相当巨大。不少国家正在探索海水提铀的方法。现在,已经研制成功了一种螯合型离子交换树脂,它专门吸附海水中的铀,而不吸附其他元素。其反应原理为____________(树脂用HR代替),发生离子交换后的离子交换膜用酸处理还可再生并得到含铀的溶液,其反应原理为________________________________________________________________________。9海水资源的利用具有非常广阔的前景。(1)海水淡化的主要方法有(只写出1种即可)________。(2)海水中丰富的氯化钠是重要的化工原料,如电解饱和食盐水可以制备多种化工产品。①用石墨电极电解饱和食盐水时,阴极的电极反应式是_____________________。②常温下,用石墨电极电解饱和食盐水,当阴极产生的气体体积为112mL(已折算为标准状况)时停止电解,此时溶液体积为1L,若忽略气体的溶解,最终溶液的pH约为________。
参考答案1.解析:海水淡化可以解决淡水供应危机,但向海水中加入明矾不能使海水淡化。答案:D2.解析:海水淡化的方法:蒸馏法、电渗析法、离子交换法等。选项A,加明矾,明矾的主要成分是KAl(SO4)2·12H2O,不能使海水中的盐沉淀出来,所以不能使海水淡化。答案:A3.解析:电解水使用的是直流电。虽然水通电后能分解生成两种气体,但不能认为水是由氢气和氧气组成的,否则水就不是纯净物,而是混合物了。纯净的水是无色液体,海水和湖水呈现不同的颜色是因为它们都不是纯净的水,且水层厚度大。当纯水的厚度不超过2m时,都是无色透明的。答案:C4.解析:在进行水处理时,阳离子交换树脂中的H+只能和水中的金属阳离子Mn+交换,阴离子交换树脂中的OH-只能和水中的阴离子Ym-交换。答案:D5.解析:A选项,蒸发海水可以得到淡水和食盐,属于物理变化;B选项,2Na2O2+2CO2===2Na2CO3+O2,2Na2O2+2H2O===4NaOH+O2↑;C选项,Cl2+2NaOH===NaCl+NaClO+H2O,NaClO是84消毒液的有效成分,2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O,Ca(ClO)2是漂白粉的有效成分,它们都能漂白、杀菌消毒;D选项,工业上制造光导纤维的应是SiO2,所以D选项错误。答案:D6.解析:膜分离法是海水淡化的一种方法,A项正确;催化剂可以加快化学反应速率,但不能改变反应的方向和热效应,B项错误;C项正确,如常见的氨水、乙醇溶液等均如此;金属的电化学腐蚀主要是吸氧腐蚀,正极的电极反应式为2H2O+O2+4e-===4OH-,D项正确。答案:B7.解析:A项中涉及海水淡化的几种主要方法,正确;B项中海水含有Na+、Mg2+、K+、Ca2+、、Cl―、Br―等,因此可以从海水中得到NaCl、MgCl2、KCl、MgSO4、CaSO4、MgBr2等物质;C项中海水淡化的同时,得到了含盐分较多的浓水,为氯碱工业、镁工业、钾工业、溴工业等提供了较好的原料,可以降低成本,C项正确;D项中最初海水淡化能耗大,成本高,但随着技术的进步,使用规模的扩大,成本已大大降低,故错误。答案:D8.解析:(1)海水经过蒸发和冷凝得到淡水,原理与蒸馏相同,故方法可归类为蒸馏法。(2)从阴极接电源负极,阳极接电源正极以及图中阴、阳离子移动方向可知a是电源的负极;利用电场作用,使海水中阴、阳离子分别向阳、阴极定向移动,但在阳膜和阴膜的离子选择性透过作用下,使有的间隔内离子浓度变大(如②间隔),有的间隔内离子浓度变小(如①间隔),故得出Ⅰ口排出的是淡水。(3)浓水需精制后才能电解,精制时一般先加烧碱除去Mg2+、Fe3+等,再加氯化钡除去,再加碳酸钠除去Ca2+和过量的Ba2+,过滤出沉淀后加盐酸调节pH。(4)根据离子交换树脂交换溶液中阳离子的离子方程式,迁移到交换铀离子的离子方程式,一定要注意铀离子带4个单位的正电荷,用酸处理交换后的树脂又得到铀离子和树脂。答案:(1)蒸馏法(2)负 淡水(3)①NaOH、BaCl2(NaOH和BaCl2位置可互换)、Na2CO3、盐酸 ②2NaCl+2H2O2NaOH+H2↑+Cl2↑(4)4HR+U4+===UR4+4H+ UR4+4H+===4HR+U4+9.解析:本题考查了海水的综合利用。海洋是个大宝库,里面有许多资源。(1)在淡水资源日益紧张的今天,海水淡化显得非常重要,常用的方法有蒸馏法(或电渗析法或离子交换法)。(2)用石墨电极电解饱和食盐水,阳极发生的反应:2Cl--2e-===Cl2↑,阴极发生的反应:2H++2e-===H2↑。当阴极产生112mL气体时,此时消耗H+为0.01mol,所以生成0.01molOH-,pH=12。
答案:(1)蒸馏法(或电渗析法、离子交换法)(2)①2H++2e-===H2↑ ②12'
您可能关注的文档
- 15种我国农村生活污水处理技术详细讲解
- 生活污水处理技术规范选编
- 《污水处理技术》术语英语词汇大全
- 一体化地埋式生活污水处理技术方案设计
- 锅炉水处理技术培训资料2012年度
- 工业锅炉水处理技术_10
- 国内外水处理技术的现状发展趋势
- 高浓度氨氮废水处理技术最新进展
- 2019-2020年高中化学专题一多样化的水处理技术第一单元水的净化与污水处理课后训练苏教版选修2
- 常见工业废水处理技术精选范文
- 东北地区农村生活污水处理技术指南精选范本
- 景观水处理技术之物理方式精品word
- 光伏行业超纯水水处理技术实施方案
- 环保型水处理技术设施建设项目投资立项申报投资建议
- 烟台污水处理技术
- 东南地区农村生活污水处理技术指南.pdf
- 以糖蜜为原料的酵母废水处理技术.pdf
- 宜州荣发缫丝厂废水处理技术方案.pdf