- 267.10 KB
- 2022-04-22 13:32:09 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'TiO2纳米管的制备及应用研究进展毕业论文目录摘要1Abstract2前言3第一章TiO2纳米管的概况41.1TiO2纳米管的晶型和形貌41.2TiO2纳米管的化学组成5第二章TiO2纳米管的制备及改性方法62.1模板法62.2阳极氧化法62.3水热合成法72.4浓碱处理法82.5TiO2纳米管的改性方法82.5.1非金属掺杂92.5.2金属掺杂92.5.3半导体复合10第三章TiO2纳米管的应用领域113.1降解污染物113.2染料敏化太阳能电池123.3光解水制氢133.4气敏传感器材料133.5其他方面应用14第四章TiO2纳米管发展趋势及应用的展望15参考文献17致谢20
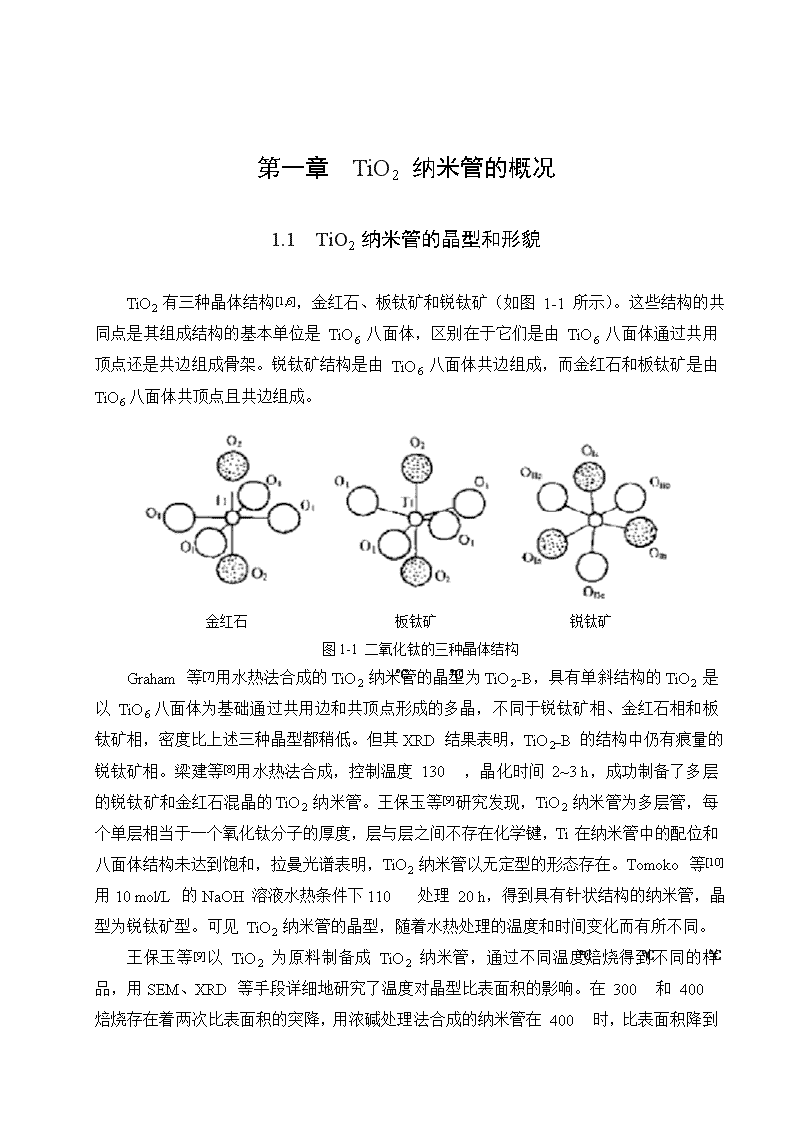
第一章TiO2纳米管的概况1.1TiO2纳米管的晶型和形貌TiO2有三种晶体结构[1,6],金红石、板钛矿和锐钛矿(如图1-1所示)。这些结构的共同点是其组成结构的基本单位是TiO6八面体,区别在于它们是由TiO6八面体通过共用顶点还是共边组成骨架。锐钛矿结构是由TiO6八面体共边组成,而金红石和板钛矿是由TiO6八面体共顶点且共边组成。金红石板钛矿锐钛矿图1-1二氧化钛的三种晶体结构Graham等[7]用水热法合成的TiO2纳米管的晶型为TiO2-B,具有单斜结构的TiO2是以TiO6八面体为基础通过共用边和共顶点形成的多晶,不同于锐钛矿相、金红石相和板钛矿相,密度比上述三种晶型都稍低。但其XRD结果表明,TiO2_B的结构中仍有痕量的锐钛矿相。梁建等[8]用水热法合成,控制温度130℃,晶化时间2~3h,成功制备了多层的锐钛矿和金红石混晶的TiO2纳米管。王保玉等[9]研究发现,TiO2纳米管为多层管,每个单层相当于一个氧化钛分子的厚度,层与层之间不存在化学键,Ti在纳米管中的配位和八面体结构未达到饱和,拉曼光谱表明,TiO2纳米管以无定型的形态存在。Tomoko等[10]用10mol/L的NaOH溶液水热条件下110℃处理20h,得到具有针状结构的纳米管,晶型为锐钛矿型。可见TiO2纳米管的晶型,随着水热处理的温度和时间变化而有所不同。王保玉等[9]以TiO2为原料制备成TiO2纳米管,通过不同温度焙烧得到不同的样品,用SEM、XRD等手段详细地研究了温度对晶型比表面积的影响。在300℃和400℃焙烧存在着两次比表面积的突降,用浓碱处理法合成的纳米管在400
℃时,比表面积降到很小,管的结构被严重破坏。用浓碱处理法合成的TiO2纳米管是无定型的,而模板法制备的纳米管为锐钛矿型。这可能是因为浓碱处理法制备的纳米管为多层,层与层之间不能形成三维空间的点阵结构。而王芹等[11]研究则发现钛纳米管经过400℃热处理后能保持其纳米管的形貌,600℃有纳米管间烧结的现象,800℃时管的形状被完全破坏。可见合成方法不同,氧化钛纳米管的热稳定性也有很大的差异。TiO2纳米管的特征:(1)大多数纳米管是非对称的;(2)大部分纳米管是卷曲型的;(3)几乎所有的纳米管是顶端开口或是两端开口的;(4)所有纳米管为多层纳米管。在水热处理的过程中,除了生成纳米管本身的一级结构外,还存在纳米管之间的聚集,因而产生了TiO2纳米管的二级结构。Bavykin等[12]研究发现,纳米管的二级结构取决于前驱体TiO2的量和所用NaOH的体积,其比例越小,生成的TiO2纳米管越倾向聚集成球状。这可能是由于在水热条件下生成纳米管的过程是一个比较缓慢的过程,影响因素较复杂。1.2TiO2纳米管的化学组成人们对TiO2纳米管本身的化学组成存在不同看法,比如:到底是二氧化钛、钛酸盐还是钛酸?近年来大家对这些方面都进行了一些探讨,彭练矛等对此做出了一系列工作[13,14,15],他们通过用HCl溶液处理和不用HCl溶液处理的纳米管的对比发现,酸处理并没有促进纳米管的生成,而是在纳米管中引入更多的缺陷。用XRD和能量损失谱研究孤立纳米管的成分,发现氧和钛的原子比为不定值,化学分析和红外光谱表明材料中含有成键的氢,这也就是说目前所认为的TiO2纳米管都是由钛酸盐或钛酸组成。王芹等[11]将酸性溶液处理所得的H2TiO3纳米管于400℃热处理,失水而成锐钛矿型氧化钛,并能保持其纳米管形貌显示出纳米管具有较好的热稳定性,这一观点与Wang等[16]一致。兰英等[17]以金红石相TiO2为原料,将所制得的质子钛酸盐纳米管于500℃煅烧后,该纳米管逐渐转变为锐钛矿相四方结构的纳米柱。Yang等[18]认为以锐钛矿为原料所得的纳米管Na2Ti2O4(OH)2和H2Ti2O4(OH)2均为单斜晶系。
第二章TiO2纳米管的制备及改性方法2.1模板法模板合成法[19,20]是把纳米结构基元组装到模板孔洞中而形成纳米管或纳米丝的方法,如图2-1所示。通过合成适宜尺寸和结构的模板为主体,利用物理或化学方法向其中填充各种金属、非金属或半导体材料。常用的模板主要有两种:一种是有序孔洞阵列氧化铝模板(PPA),另一种是含有孔洞无序分布的高分子模板。其他材料的模板还有纳米孔洞玻璃、介孔沸石、蛋白、多孔Si模板、表面活性剂及金属模板。目前在模板合成法制备TiO2纳米管过程中,常采用纳米阵列孔洞厚膜(如氧化铝模板)、有机聚合物或表面活性剂作模板,然后通过电化学沉积法、溶胶-凝胶法等技术来获得TiO2纳米管。通过模板法制备TiO2纳米管,一般制备工艺复杂,生成纳米管的大小和形状取决于模板孔的尺寸和形状,而且模板和纳米管的分离往往会破坏纳米管的形貌,表面粗糙,如图2-2所示。因此重现性比较差。图2-1模板合成TiO2纳米管示意图图2-2模板法制备的TiO2纳米管2.2阳极氧化法阳极氧化法是指将经过预处理的钛片放入含有氟化物电解液中作为阳极,以镍等作为阴极,通过阳极氧化将阳极腐蚀制得TiO2管状结构。TiO2纳米管的形貌和性质取决于电解液的组成配比、电解液的pH、外加电压、温度、反应时间等。Varghese等[21]
采用阳极氧化法制备TiO2纳米管,通过实验得出:当外加电压为20V时制得的纳米管内径为76nm,管壁厚为27nm,而当负载电压减小为12V时制得的纳米管内径减小为46nm,管壁厚也下降到17nm。Zhao等[18]在HF电解液中,加入乙二醇和少量的水,通过合适的外加电压,得到了形貌规则排列整齐的TiO2纳米管,制得的纳米管的形貌随外加电压、电解液配比浓度和反应时间的改变而改变。并且,该种方法制得的纳米管稳定性很高,通过改变阳极氧化电压、电解液成分、电解液pH和电解时间,可以控制纳米管的直径、管长、管壁厚度及其形态。J.M.Macak[22]等采用阳极氧化法制备TiO2纳米管,电解液采用的是含有少量氟化物的中性硫酸盐溶液,取代了传统的HF溶液,制备出了微米级TiO2纳米管。阳极氧化法的优点是成本低廉、效果明显的TiO2纳米管的制备方法。采用阳极氧化法,可通过改变其反应参数可以实现TiO2纳米管的可控生长,但应用阳极氧化法制备纳米管的最佳条件至今仍有争议。2.3水热合成法水热合成法,又称为化学法,传统的水热合成法是将TiO2纳米粒子在高温下与碱溶液混合进行反应,然后经过离子交换工艺后进行煅烧,制成TiO2纳米管。近年来,在传统方法的基础上又研发出了两种新的方法:超声碱溶法和微波水热法。超声碱溶法是将TiO2纳米颗粒加入到碱性溶液中,直接放入超声仪中进行超声振荡,然后得到TiO2纳米管。微波水热法是将TiO2粉末加到碱溶液后,经微波加热制得纳米管。Kasuga等[22]将溶胶凝胶法得的TiO2纳米粉体放入到5~10mol/LNaOH水溶液中,加热温度至110℃,时间持续20h,最终得到针状TiO2纳米管,管长长约100nm、管径约8nm,形貌良好。研究者利用超声碱溶法制备TiO2纳米管,将TiO2颗粒放入一定浓度的NaOH水溶液中,进行超声振荡,再经水洗和稀硝酸处理,最后合成了长度可达200~300nm的TiO2纳米,这种纳米管管径5nm,壁厚约1.3nm,完全符合应用条件。DmitryVB等[13]借助高分辨率的透射电镜和低温氮吸收系统,研究了在碱性水热合成法中,制备条件对TiO2纳米管形态的影响。通过研究发现,纳米管的平均管径随水热处理温度的升高而有所增加,增大TiO2与NaOH的摩尔比虽然同样也能使纳米管的平均管径有所增加,但会导致纳米管比表面积的下降,从而影响纳米管的性能。水热合成法相对于其它几种方法的特点是:
可直接生成氧化物,无需煅烧,避免了硬团聚的形成。产物晶粒分布均匀,发育完整,而且该法可以控制粒度,颗粒之间的团聚少,原料较为便宜,可以得到理想的化学计量组成材料。水热合成TiO2纳米管的关键问题是设备要经历高温和高压,因而对材质和安全要求较严格而且成本较高。2.4浓碱处理法一般用四氯化钛、有机钛或商品化的TiO2为钛源,先用浓NaOH水热处理后,再用稀HCl处理,最后得到二氧化钛纳米管。Tomoko等[10]用金红石型的氧化钛为前驱物,加入浓NaOH溶液,油浴控温110℃,反应20h,经用0.1mol/LHCl处理得到样品,并指出水洗和进一步用稀HCl处理是得到氧化钛纳米管的必要条件。浓碱处理后得到含有TiONa的样品,经过酸处理后,形成了片状的纳米粒子,这些片状的纳米粒子卷曲成纳米管。Sun等[23]报道了与Tomoko等[10]相同的结果。但是Chen等[24]在后续处理中分别用水、乙醇、丙酮来洗涤,由于后两种非水溶剂的酸性比较弱,H+难以取代晶格中的Na+,结果表明洗涤对纳米管的产率没有什么影响,由此认为高浓度的Na+和较强的碱性条件的是形成纳米管所必需的,这与王芹等[11]和Yao等[25]的研究结果是一致的。张青红等[26]用浓碱处理不同粒径的锐钛矿相和金红石相TiO2纳米粉体得到了不同形貌的纳米管,发现金红石相超细纳米晶型有利于形成均一形貌的纳米管。而Seo等[27]的研究结果表明,用粒径25nm的球状金红石相纳米TiO2在100℃,反应12h,并没有发生粒子的形状和大小的变化,锐钛矿相TiO2在形成纳米管时更有利,这是因为在浓NaOH溶液处理过程中,锐钛矿型的结构有助于纳米管在某一特定的方向连续不断地生长。Lan等[28]用粒径120~128nm金红石相纳米TiO2在碱性条件下通过控制水热反应的温度和时间来控制产物的形状、大小和晶型。结果表明在相对低温的条件下,锐钛矿型比金红石型在碱性溶液中更容易反应生成纳米管。2.5TiO2纳米管的改性方法由于TiO2带隙较宽,对大部分可见光不能进行有效地吸收利用,同时又因光生电子与空穴容易复合而表现出较低的光量子效率。通过对其掺杂改性,可在一定程度上解决这些问题。特别是若能在纳米管中掺杂部分金属、非金属元素等制成复合纳米材料,那么TiO2纳米管的光电转化效率和光催化性能将得到大大的改善。目前国内外已有不少TiO2纳米管掺杂金属和非金属、半导体复合等改性的报道,下面主要由以下几个方面介绍。
2.5.1非金属掺杂非金属元素的掺杂一般是用非金属元素取代TiO2中的部分氧,形成TiO2-xAx(A代表非金属元素)晶体,由于O的2p轨道和非金属中能级与其能量接近的p轨道杂化后使价带宽化,禁带宽度会相应减小,从而拓宽了TiO2的光响应范围[29,30]。以S、N为例,掺杂后N或者S取代了TiO2的晶格氧进入晶格,通过其p轨道和O的2p轨道杂化混合形成新的能带,进而降低带隙,使得改性后的TiO2光响应范围扩展至可见光区[31]。Tokudome等[32]以自制的TiO2纳米管为原料,用0.5mol/L的HNO3作为表面质子化试剂,然后与氨水溶液反应,在673K煅烧得到了淡黄色的粉末N_TiO2纳米管,实验表明该纳米管可以吸收400nm以上的可见光,并且对异丙醇具有可见光催化活性,其催化活性在空气中和水中在紫外光辐照后没有减弱,与未掺杂的氧化钛纳米管相比较,其光催化活性得到了提高。Schmuki等[33]和Bard等[34]分别制得了氮掺杂和碳掺杂的TiO2纳米管。非金属元素掺杂TiO2纳米管的改性方法可以有效地将TiO2光谱响应范围从紫外光区拓展至可见光区,从而使其具有可见光光催化活性。但是对于非金属元素掺杂TiO2纳米管,无论是理论基础方面还是应用方面,都有许多问题需要解决和深入研究。2.5.2金属掺杂金属掺杂包括贵金属修饰和金属离子掺杂,贵金属修饰TiO2可以改变体系的电子分布,形成Schottky能垒,进一步抑制光生电子和空穴的复合。金属离子掺杂是利用物理或化学的方法,将金属离子引入到TiO2晶格结构内部,改变晶格的结构类型,引入新的电荷,使光生电子和空穴的运动状况发生改变,能带结构产生变化,从而使TiO2的光催化活性发生改变,达到提高光催化活性的目的。目前对氧化钛纳米管的金属掺杂报道主要集中在金、银和铂等贵金属。由于金对负载介质的粒子大小和结构很灵敏,用金比较适合对其负载型氧化钛纳米管的催化活性进行评价。Tomoki等[35]研究了氧化钛纳米管掺杂金后性质的变化,其高分辨电镜和电子衍射结果表明,TiO2纳米管的晶体构型不同于锐钛矿相,也不同于金红石相。Au/TiO2纳米管和参照标准的Au/TiO2催化剂相比,具有较低的CO氧化活性和中等强度H2的氧化活性。宋旭春等[36]采用温和的水热方法合成了掺杂铁的纳米管,并发现以金红石掺杂铁的TiO2纳米粉体为前驱体得到长约200nm、管径10nm左右的掺铁纳米管,但对其应用性质没有进一步研究。
2.5.3半导体复合半导体复合主要是通过纳米粒子间的相互耦合作用形成半导体复合体,利用两种半导体的导带、价带、禁带宽度不一致的特点,使光生载流子在复合后在能隙不同的两种半导体之间发生传输与分离,由于两种半导体的的导带、价带、禁带宽度不一致,在复合后,光生载流子在能隙不同的两种半导体之间发生传输与分离,从而降低了光生电子-空穴对的复合率。复合半导体多为采用浸渍法或混合溶胶制备的TiO2二元或多元复合半导体,常见的半导体复合体系有TiO2/ZnO、TiO2/MnO2、TiO2/CdS等,迄今对TiO2纳米管阵列进行半导体复合的有关报道较少。利用电沉积的方法在TiO2纳米管阵列表面沉积了粒径约为10~20nm的CdS颗粒膜,修饰后的TiO2纳米管阵列禁带宽度为2.53eV,N2气氛下350℃热处理后禁带宽度为2.41eV,光谱响应范围发生了明显的红移,光电性质也有了较为明显的改善。SiHua-Yan等[37]以CdSe纳米粒子为敏化剂,将经过一系列预处理的TiO2纳米管阵列放在含CdSe纳米粒子的溶液中浸渍,制得敏化的TiO2纳米管阵列,该阵列具有较强的可见光响应。综上所述,采用不同的方法对TiO2纳米管阵列进行改性,可使其具有可见光响应,光催化活性得以明显改善,为今后进一步研究改性方法、控制掺杂或复合第二物种的量以及探索第二物种的作用机理提供了重要的研究基础。
第三章TiO2纳米管的应用领域3.1降解污染物TiO2纳米材料可以光催化处理难降解的有机污染物。目前纳米TiO2光催化研究方向主要集中在两个方面:一个是实现可见光响应,另一个是提高光量子效率。TiO2纳米管的管状结构使光生电子空穴逃逸到纳米管表面参与氧化还原反应只需要皮秒的时间,降低了电子与空穴的复合几率,从而能够提高光量子效率。科学家通过将乙酰丙酮锌盐与TiO2纳米管按照Zn/Ti原子比为0.12的比例进行配体交换制备得到Zn2+掺杂TiO2纳米管,与纳米管较大的比表面积协同作用显示出很好的光催化效果。与纳米TiO2颗粒膜相比,TiO2纳米管阵列具有比表面积和量子阱效应更高,纳米管尺寸、形貌和结构可控,阵列层与基体结合强度高等优点,表现出更强的光催化活性。科学家以偶氮染料AO7及亚甲基蓝为目标污染物对纳米TiO2颗粒膜与TiO2纳米管阵列、不同长度以及不同晶型的TiO2纳米管阵列光催化活性分别进行了比较,发现TiO2纳米管阵列的光催化活性优于纳米TiO2颗粒膜,而且管长越长光催化活性越好,锐钛矿晶型的光催化活性优于无定型及混晶型的TiO2纳米管阵列。利用甲醇和溴水混合水溶液将钛基底溶掉得到一端封闭的TiO2纳米管阵列,然后用氢氟酸蒸气除去阻挡层,得到两端通透的TiO2纳米管阵列,该阵列具有良好的渗透性和光催化性能。科学家针对TiO2纳米管阵列在光催化方面的应用开展了一些研究工作,首先,以0.5%HF为电解质,20V电压下阳极氧化20min得到TiO2纳米管阵列,与溶胶凝胶法制备的纳米TiO2颗粒膜进行比较,发现前者对苯酚的光催化降解效率提高了近1倍,且稳定性较好。其次,制备了不同孔径和长度的TiO2纳米管阵列,研究表明,热处理温度对TiO2纳米管阵列的结晶度和形貌有较大的影响,其中,450℃热处理后的TiO2纳米管阵列具有较好的锐钛矿型结构并能够很好的保持阵列形貌[38]。对不同管长的TiO2纳米管阵列的光催化性能进行了综合考察,TiO2纳米管阵列光催化性能明显优于纳米TiO2颗粒膜,且作为光催化剂能使偶氮染料甲基橙迅速脱色,最终降解为无机小分子;TiO2纳米管阵列的光催化活性与其自身的结构和晶型密切相关,纳米管阵列膜的厚度存在一个最佳值,使其具有最高的光催化降解速率,但在膜厚一致的前提下,纳米管的管径对光催化降解速率影响不大。
3.2染料敏化太阳能电池太阳的辐射对地球所提供的能量是巨大的,约为3×1024焦耳/每年,比人类每年所消费的能源多一万倍。所以说,只要在全球0.1%的面积上具有10%转换效率的太阳能电池,就能够满足全球的能量供应。目前,利用太阳能的主要途径是通过光电化学太阳能电池,将太阳能转换为电能加以利用。在过去的几十年中,各式太阳能电池应运而生,得到了长足的发展。当前发展较为成熟、应用较为广泛的是硅系太阳能电池,但由于硅系太阳能电池使用的材料成本居高不下,使其不能得到广泛的应用。Grimes等[39]合成了透明的TiO2纳米管太阳能电池,并报道了把这种透明的排列紧密的纳米管阵列制成染料敏化太阳能电池(DSC)中的负电极的初步结果。人们发现,这种纳米管具有非常好的渗透电子的性质,从效果上说,它就像是一种电子高速公路,能引导光致电子做有用功。这种纳米管阵列长度达到几个微米时就能制成单电子理想光电转化效率高达31%的太阳能电池,如果在紫外光照射下,这种材料对光能的转化率可达到13.1%,简单地说就是每个光子入射进来都能产生很多氢气。如果能够把这种TiO2纳米管的能隙调整到可见光波段,就能够制造出一种可以实际应用的太阳能制备氢气装置。科学家利用离子植入结合煅烧法,得到了氮掺杂的TiO2纳米管,实验证实这种锐钛矿型的TiO2纳米管在紫外光区和可见光区都有很大程度光电流响应的增强,这是因为具有较大的比表面积和同时氮掺杂所带来的可见光响应所致。Bard[34]等的研究结果表明,可以用化学的方法降低带隙宽度,同时可以调控碳掺杂TiO2纳米管的形貌,使太阳能的利用效率得以提高。Wang[16]研究了管长220nm~2μmTiO2纳米管阵列的光电转化效率,发现随着管长的增加光电转化效率从0.1%增至0.62%,此外,经适当的热处理后短路电流可达3.28mA·cm 。Grimes以含8%(C4H9)4NF的甲酰胺为电解质溶液制备出管长220μm的TiO2纳米管阵列,经过处理染料敏化后光电转化效率为6.89%、开路电位为0.817V、短路电流密度为12.27mA·cm-2,其光电转化效率相对于6μm长的纳米管阵列提高了62%[40]。TiO2纳米管阵列的光电转换受多种因素的影响,其光电转换机理是今后研究的重要内容,提高光电转换效率是必须解决的根本问题。3.3光解水制氢
早在1972年Fujishima和Honda[41]就报道了利用n型半导体TiO2光解水制氢,此后这一领域的研究始终倍受关注。TiO2的能级与水的氧化还原电位相匹配,是光解水制氢的理想材料,近年来TiO2纳米管阵列材料随着其制备技术的成熟而成为光解水制氢的理想材料。据报道TiO2纳米管阵列材料为光阳极制备的光电池氢气生成速率为7.6mL·(hW)-1,光电转化效率高达12.25%,与纳米TiO2粉末相比,产氢效率大幅度提高。Grimes[39]考察了不同温度下制备的TiO2纳米管阵列的产氢效率,发现温度越低,管壁越厚,产氢速率越大,5℃下制备的TiO2纳米管阵列具有较厚的管壁,产氢速率为24mL·(hW)-1。后又以室温下制备的长达6μm的TiO2纳米管阵列为光阳极,可见光为光源,其产氢速率为175μL·(hW)-1,光电转化效率为0.6%。目前,由于TiO2禁带宽度的限制大都以紫外光为光源,对太阳光的利用较少,这也是光解水制氢亟待解决的问题之一。3.4气敏传感器材料纳米管还可用于传感器材料的制备,用于检测H2、CO、O2等。比较常用的是作为汽车尾气传感器,通过检测汽车尾气中的氧气含量来控制和减少尾气中的二氧化碳和氮氧化物的污染。Varghese[21]等用TiO2纳米管制备的传感器来检测H2含量,发现此种传感器对H2敏感度很高。利用阳极化技术成功制备了负载Pd的阵列TiO2纳米管,将该纳米管作为氢气传感器,延长了传感器的使用寿命。TiO2纳米管阵列气敏材料具有工作温度范围广、灵敏度高、制备方法简单等优点。科学家以不同形貌的TiO2纳米管阵列为探测氢气的气敏传感器,发现管径越小,灵敏度越高,内径22nm的TiO2纳米管阵列对氢气的灵敏度比之前报导的最高值还要高10倍;290℃下,氢气浓度从0增加到500mg·L-1,内径22nmTiO2纳米管阵列的电阻变化达4个数量级,这种材料不仅灵敏度高,而且工作温度低。TiO2纳米管阵列表面修饰约10nm厚的Pd后制得的氢敏传感材料在室温下氢敏活性高达107,是目前报道的最高氢敏活性的材料之一[37]。TiO2纳米管阵列的高气敏活性源于其特殊的形貌结构及纳米尺度上的高度对称性。目前,对TiO2纳米管阵列气敏传感性能的研究还相对较少,深入探究影响其性能的各种因素及其气敏传感机制是非常必要的。3.5其他方面应用作为新型的绿色环保型纳米材料,TiO2
纳米管阵列各方面潜在的优越性能正一步步展现出来。以该材料为模板还可以合成出的其他纳米材料,如钛酸钡和钛酸锶钡纳米管,这些材料具有新颖的物化特性。在TiO2纳米管阵列上电沉积钙磷盐经热碱处理形成的羟基磷灰石涂层在模拟人体液中的电化学性能优于纯钛,TiO2纳米管阵列能阻止体液对基体钛的侵蚀及金属离子向基体的游离。以钛板为基底的TiO2纳米管阵列,在1.5SBF模拟体液中诱导形成磷灰石层,表现出良好的生物活性,具有在生物材料领域上应用的可行性,经过NaOH溶液处理的TiO2纳米管阵列具有良好的生物活性,加快了羟基磷灰石在模拟体液中的生长速度,有望在外科和牙科得到广泛应用。
第四章TiO2纳米管发展趋势及应用的展望TiO2纳米管的制备和应用研究涉及化学、物理、材料、工程等学科。虽然近年来人们对TiO2纳米管进行了诸多研究,但无论是基础研究还是应用研究都还有许多问题尚待解决。如在基础研究方面,对TiO2纳米管的生成机理和化学组成,有必要采用新的表征手段进行表征,因为到目前为止TiO2纳米管的机理和组成还存在分歧。就合成方法而言,模板法、阳极氧化法、水热合成法、浓碱处理法各有优点和不足,争取探索更好的合成方法,从而对TiO2纳米管阵列的管径、管长和壁厚等参数进行有效控制,达到对TiO2纳米管的形态和纳米尺寸的精准调控,定向合成出功能更强大的纳米元器件。例如在气敏传感器中,高气敏活性源于TiO2纳米管阵列的特殊形貌结构及纳米尺度上的高度对称性,在光催化剂方面,TiO2纳米管的管长及阵列膜的厚度都对TiO2纳米管的光催化效率有决定性的影响。因此怎样可以精准的制备TiO2纳米管阵列是今后的研究目标之一。作为一种新型的纳米材料,TiO2纳米管阵列已经在光催化降解污染物、染料敏化太阳能电池、光解水制氢、气敏传感器以及生物材料等领域显示出广阔的应用前景。然而与传统TiO2一样,TiO2纳米管阵列也存在固有缺陷,成为其实际应用的“瓶颈”。由于TiO2带隙较宽,对大部分可见光不能进行有效地吸收利用,同时又因光生电子与空穴容易复合而表现出较低的光量子效率。通过对其掺杂改性,可在一定程度上解决这些问题。特别是若能在纳米管中掺杂部分金属、非金属元素等制成复合纳米材料,则TiO2纳米管的光电转化效率和光催化性能将得到大大的改善。当前的TiO2纳米管的掺杂主要是金属掺杂、非金属掺杂和半导体复合。通过在TiO2纳米管阵列的管内自组装非金属、金属或磁性材料纳米粒子,改善了TiO2纳米管阵列的表面对其可见光的吸收,进一步改善TiO2纳米管阵列的光、电、磁等特性。但是从目前的研究结果来看,可见光催化或能量转换效率还较低,因此可见光响应TiO2纳米管阵列的可见光催化和光电转换效率研制仍将是今后的研究热点之一。TiO2纳米管的应用研究目前还处于实验阶段,实际应用还需要进一步研究。例如,TiO2纳米管在涂料和化妆品中的应用要解决好TiO2在体系中的相容性。对于在光催化领域中应用时,要选择好金属掺杂剂,采用合适的掺杂量,目的是减少电子与空穴的复合,提高光催化性能。制造染料敏化太阳能电池的研究方面,电池光电转换效率还较低,可能原因有两个方面,一方面是由于所制备的TiO2
纳米管长度较短的原因,另一方面也和电解质、染料、电池的封装等外在因素相关。在之后的研究中,首要任务是探寻如何制备长度更长、排列规则有序的TiO2纳米管阵列;同时,对于电解质、染料、电池封装等因素也需要进行研究,以求得到最佳组合结果,从而获得较好的光电转换效率。最重要的是TiO2纳米管阵列的制备条件与工业化生产还有一定的差距,要向大规模工业化过渡及完全投入实际应用还需要做很多的工作。此外,深入开发TiO2纳米管阵列在生物材料领域的应用也具有重要的现实意义。TiO2纳米管自身的优异性能正日益的被挖掘出来,虽然其中有许多尚待解决的问题,但无数的工作者们正努力的改善和改进其性质和制备方法,相信有一天TiO2纳米管会成为人们的优异帮手,给人们的生活带来一定的方便。
参考文献[1]高濂,郑珊,张青红,纳米氧化钛光催化材料及应用[M].北京:化学工业出版社.2002.14:3160-3163.[2]刘吉平,廖莉玲,无机纳米材料[M].北京:科学出版社.2003.16(11):997-1002[3]O’ReganB.GratezelM,Alow-cost,high-efficiencysolarcellbasedondye-sensitizedcolloidalTiO2films[J].Nature.2010,353:737-740.[4]AdachiM.MurataY.HaradaM.etal.Formationoftitaniananotubeswithhighphoto-catalyticactivity[J].ChemistryLetters.2010,(8):942-943.[5]VargheseO.K.GongD.W.PauloseM.etal.ExtremeChangesintheElectricalResistanceofTitaniaNanotubeswithHydrogenExposure[J].AdvancedMaterials.2010,15(7-8):624-627.[6]付敏,原鲜霞,马紫峰.TiO2纳米管制备及其应用研究进展[J].化工进展.2005,24(1):42-43.[7]AGraham,AARobert,JCanalesetal.Chem.Commun.ARoom-temperatureTiO2-nanotubeHydrogenSensorAbletoSelf-cleanPhotoactivelyfromEnviron-mentalContamination[J].JMaterRes,2011,5(19):2454~2456[8]梁建,马淑芳,韩培德等.阳极氧化TiN薄膜制备N掺杂纳米TiO2薄膜及其可见光活性[J]物理化学学报,2005,34(2):287~290[9]王保玉,郭新勇,张治军等.合成温度对二氧化钛纳米管的影响[J].高等学校化报,2003,24:1838~1841[10]KTomoko,HMasayoshi,Langmuir,PreparationofAnataseTiO2/TiNanotube-likeElectrodesandTheirHighPhotoelectrocatalyticActivityfortheDegradationofPCPinAqueousSolution[J].AppliedCatalysisA:General.2011,14:3160~3163[11]王芹,陶杰,翁履谦等.钐离子掺杂二氧化钛光催化降解甲基橙研究[J].材料开发与用,2004,19:9~12[12]DVBavykin,VNParmon,AALapkinetal.J.Mater.Chem.ColloidsandSurfacesA:Pysicochem.[J]Eng.Aspects,2004,14:3370~3377[13]QChen,WZZhou,DmitryVB.EffectsofF-dopingonthePhotocatalyticActivi-tyandMicrostructuresofNanocrystallineTiO2Powders[J].ChemMater,2002,14(17):1208~1211[14]QChen,GHDu,LMPeng.PreparationandCharacterizationofTiO2NanotubeArraysandResearchofProperties[D].Xiamen:XiamenUni-versity,2002,21(3):265~269[15]SZhang,LMPeng,QChenetal.Phys.Rev.Lett..EnhancedPhotocleavageofWaterUs-ingTitaniaNanotubeArrays[J].NanoLett,2010,1218~1221_1~4[16]WZWang,OKVarghese,MPauloseetal.EffectsofDissolvedOxygen,pH,andAnionsonthe2,3-dichlorophenolDegradationbyPhotocatalyticReactionwithAnodicTiO2NanotubeFilms[J].Chemosphere,2004,19(2):417~422[17]兰英,刘建文,掺杂二氧化钛纳米管的光催化性能[J]高学平等.电化学,2004,10(2):133~136[18]JJYang,ZSJin,zhao.PhotoelectrocatalyticDegradationofPentachlorophenolinAqueousSolutionUsingaTiO2NanotubeFilmElec-trode[J].EnvironPollut,,2011,3898~3901[19]付敏,原鲜霞,马紫峰.TiO2纳米管制备及其应用研究进展[J].化工进展.2005,24(1):44-46.
[20]郭孟狮,杨靖华,周心艳.TiO2纳米管的研究进展[J].材料导报.2010,20(z2):108-110.[21]DGong,CAGrimes,OKVargheseetal.Pho-tocatalyticpropertyofCe-dopedTiO2nanotube[J].MaterialforMechanicalEngineering,2001,16(12):3331~3334[22]MacakJ.M,TsuchiyaH,KasugaP,High-Aspect-RatioTiO2NanotubesbyAnodizationofTitanium[J].AngewandteChemieInternationalEdition2010,44(14):2100-210[23]XMSun,YDLi.Chem.Eur.J.UseofHighly-orderedTiO2Nan-otubeArraysinDye-sensitizedSolarCells[J].NanoLett,2010,9:2229~2238[24]QChen,WZZhou,Fabricationofhighlyorderedtitaniumdioxidenanotubearrayandinvestigationofitsphotocatalyticactivity[J].ActaChimicaSinica,2011,14(17):1208~1211[25]BDYao,YFChan,Photo-catalyticpropertyandsynthesisoftitaniananotubes[J].JournaloftheChineseCeramicSociety,2010,82(2):281~283[26]张青红,高濂,郑珊等.氧化钦纳米管的合成机理与表征[J].材料开发与应用,2002,60(8):1439~1444[27]DSSeo,JKLee,Adsorp-tionandphotocatalyticdegradationofdimethomorphonnano-Ag/TiO2cataly[J].ChineseJournalofRareMetals,2010,229:428~432[28]YLan,XPGao,AlkalineearthmetaldopednanoporousTiO2forenhancedphotocatalyticmineralisationofbisphenol-A[J].CatalysisCommunications,2010,15:1310~1318[29]刘淑芝,刘先军,徐胜利等.提高TiO2可见光分解水制氢活性的研究进展[J].应用化工,2008,37(12):1491-1495.[30]曹沛森,许璞,王玉宝等.纳米TiO2光催化剂的改性及应用研究进展[J].纳米材料与结构,2008,45(3):145-152.[31]肖羽堂,李志花,许双双.非金属元素掺杂二氧化钛纳米管的研究进展[J].化工进展,2010,29(7):1235~1240[32]HTokudome,Reviewonoptoelec-tronicpropertiesandapplicationsofTiO2filmsTiO2[J].Chi-neseJournalofRareMetals,2011,33(9):1108~1109[33]AGhicov,JM.Macak,HTsuchiyaetal.Synthesisofvisible-lightre-sponsivenitrogen/carbondopedtitaniaphotocatalystbymechano-chemicaldoping[J].Mater.Sci,2010,6(5):1080~1082[34]JHPark,SKim,Visiblelightphotoelectrochemicalresponseofnitrogen-dopedTiO2thinfilmspreparedbyanodicoxidationoftitaniumnitridefilms[J].2006,6(1):24~28[35]ATomoki,AnelectrochemicalstrategytoincorporatenitrogeninnanostructuredTiO2thinfilms:modifica-tionofbandgapandphotoelectrochemicalproperties[J].J.Phys,2011,37:265~269[36]宋旭春,岳林海,徐铸德等.利用微波法合成二氧化钛纳米管[J].无机化学学报,2003,19(8):899~901[37]孙岚,李静,庄惠芳,赖跃坤,王成林/林昌健.TiO2纳米管阵列的制备、改性及其应用研究进展[J].无机化学学报,2007,11(23):1846~1847[38]陈晓娟,彭芳光.TiO2纳米管的制备、改性及应用研究[J].铁道建筑技术,2008(B12):296-299.[39]GK.Mor,KShankar,Theinfluenceofsynthesistemperatureontheti-tania[J].J.Phys,2010,25:135~142[40]
李欢欢,陈润锋,马琮,张胜兰,安众福,黄维.阳极氧化法制备二氧化钛纳米管及其在太阳能电池中的应用[J],物理化学学报.2011,27(5),1017-1025[41]张雪峰,李会容,闫珉,等.TiO2可见光光催化的研究进展[J].电子元件与材料,2010,27(9):40-44.
致谢本论文是在姜艳丽导师的悉心指导下完成的,首先在此表示衷心的感谢。在完成本论文过程中,姜艳丽导师那严谨的治学态度,科学的思维方式,强烈的创新精神,丰富的科研经验,使我受益匪浅,更是我学习的榜样。最后感谢我的家人与朋友,感谢他们给予了我无私的爱和大力支持。'
您可能关注的文档
- pH测试仪三电极测量系统设计毕业论文.doc
- PLC交通灯毕业论文.doc
- PLC交通灯设计毕业论文.doc
- PLC控制系统的可靠性分析及其关键技术研究毕业论文.doc
- QAM传输系统的设计与实现毕业设计.doc
- RPG游戏设计与实现毕业论文.doc
- SVD与KFDA相结合人脸识别设计毕业论文.doc
- SZL7.0-1.011570-AI热水锅炉毕业设计.doc
- TD-SCDMA移动通信系统毕业论文.doc
- TPS在江淮汽车的应用分析毕业论文.doc
- VB课堂点名回答问题系统的设计与实现.doc
- WCDMA移动通信室内分布系统毕业设计.doc
- WCDMA网络切换专题优化毕业设计.doc
- web服务器网站建设与管理服务器的搭建毕业论文.doc
- WLAN安全覆盖设计毕业论文.doc
- Word 2007 编辑技巧毕业论文.doc
- XXX铜矿开发毕业设计.doc
- XX办公楼建筑毕业设计.doc
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明