- 500.25 KB
- 2022-04-22 13:44:22 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中国科技论文在线http://www.paper.edu.cn基于活性的格尔德霉素探针的设计及其抗#肿瘤靶点的研究1222222**孙延龙,王成,张秀丽,王聪,李海花,王毓,徐雪莲5(1.潍坊医学院,山东省潍坊市261053;2.中国海洋大学海洋药物教育部重点实验室,医药学院,山东省青岛市266003)摘要:[目的]设计合成源自格尔德霉素,具有抗肿瘤活性的探针,在点击化学条件下,标记肿瘤细胞内的靶点蛋白.[方法]采用MTT法对设计合成的格尔德霉素小分子探针的抗肿瘤活10性进行评价;在细胞蛋白标记实验中,采用FTC-133肿瘤细胞株,将探针作用于靶点蛋白,后加入含有荧光标记功能的报告基团罗丹明B,在点击化学条件下,使报告基团与格尔德霉素化学小分子探针共价链接,以此来标记靶点蛋白。[结果]设计合成的格尔德霉素化学小分子探针与格尔德霉素具有相似的抗肿瘤细胞增殖抑制作用,同时能够标记肿瘤细胞中的靶点蛋白HSP90.[结论]本课题设计合成的化学小分子探针,根据点击化学理论,可以用于标记肿瘤15细胞中的靶点蛋白.关键词:格尔德霉素;HSP90抑制剂;基于活性的探针Designoftheactivity-basedGeldanamycinprobesandstudyontheirantitumortargetingbioactivity1222220SUNYanlong,WANGCheng,ZHANGXiuli,WANGCong,LIHaihua,WANG22Yu,XUXuelian(1.WeifangMedicalUniversity,Weifang,Shandong261053;2.KeyLaboratoryofMarineDrugs,ChineseMinistryofEducation,SchoolofMedicineandPharmacy,OceanUniversityofChina,Qingdao,Shandong266003)25Abstract:ThisstudyisbasedontheantitumorstructureandbioavailabilityrelationshipofGeldanamycin.17-azideand17-alkyneGAweredesignedandsynthesized,whichwereusedasactivity-basedprobesofGA.Rhodamine-alkyne(RB1)wasalsodesignedandsynthesizedasreportedgroup(tag).ThetargetingproteinsofGAwerelabledbyRhodaminereportedgroupthroughclickchemistry.Totally3GAactivity-basedprobesweredesignedandsynthesized,G2withdifferent30concentrationsweredirectlyaddedtothecellculturemedium,eitheraloneorinthepresentofthecompetingGA.TheresultsindicatethatG2couldtargetHSP90,whichmakesthisapproachsuitabletolabelandidentifythetargetingproteins.Keywords:Geldanamycin;HSP90inhibitor;activity-basedprobes350引言新药研发是一个漫长而又耗时的过程,通常包括如下几个阶段:靶点的鉴别、先导化合物的发现、小分子化合物的结构优化、临床前药效学和毒性评价及临床试验等。其中靶点鉴[1]别是药物发现过程的开始,也是最为关键的阶段之一。利用化学小分子的多样性,选择适当的活性小分子,设计合成能够高选择性地作用于靶点蛋白,同时探测蛋白质的功能、结构40以及与活性小分子作用模式的探针——化学小分子探针,可以为重大疾病的诊断和防治提供[2]新的标记物、新的药物作用靶点和新的先导结构,从而为创新药物的发现奠定基础。基金项目:高等学校博士学科点专项科研基金新教师类资助课题(20130132120005)作者简介:孙延龙(1976-),男,讲师,主要研究方向:化学探针的设计与合成通信联系人:徐雪莲(1975-),讲师,主要研究方向:化学探针的设计合成及抗肿瘤靶点的确证.E-mail:xuelianx@ouc.edu.cn-1-
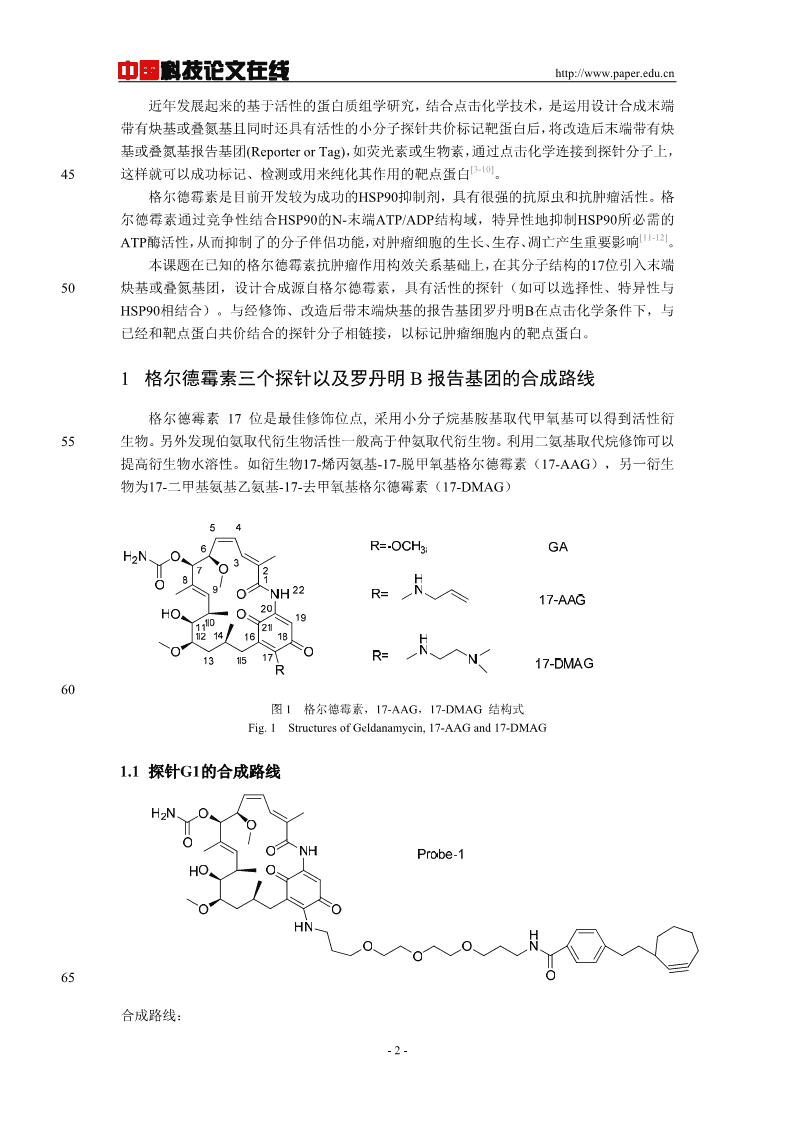
中国科技论文在线http://www.paper.edu.cn近年发展起来的基于活性的蛋白质组学研究,结合点击化学技术,是运用设计合成末端带有炔基或叠氮基且同时还具有活性的小分子探针共价标记靶蛋白后,将改造后末端带有炔基或叠氮基报告基团(ReporterorTag),如荧光素或生物素,通过点击化学连接到探针分子上,[3-10]45这样就可以成功标记、检测或用来纯化其作用的靶点蛋白。格尔德霉素是目前开发较为成功的HSP90抑制剂,具有很强的抗原虫和抗肿瘤活性。格尔德霉素通过竞争性结合HSP90的N-末端ATP/ADP结构域,特异性地抑制HSP90所必需的[11-12]ATP酶活性,从而抑制了的分子伴侣功能,对肿瘤细胞的生长、生存、凋亡产生重要影响。本课题在已知的格尔德霉素抗肿瘤作用构效关系基础上,在其分子结构的17位引入末端50炔基或叠氮基团,设计合成源自格尔德霉素,具有活性的探针(如可以选择性、特异性与HSP90相结合)。与经修饰、改造后带末端炔基的报告基团罗丹明B在点击化学条件下,与已经和靶点蛋白共价结合的探针分子相链接,以标记肿瘤细胞内的靶点蛋白。1格尔德霉素三个探针以及罗丹明B报告基团的合成路线格尔德霉素17位是最佳修饰位点,采用小分子烷基胺基取代甲氧基可以得到活性衍55生物。另外发现伯氨取代衍生物活性一般高于仲氨取代衍生物。利用二氨基取代烷修饰可以提高衍生物水溶性。如衍生物17-烯丙氨基-17-脱甲氧基格尔德霉素(17-AAG),另一衍生物为17-二甲基氨基乙氨基-17-去甲氧基格尔德霉素(17-DMAG)60图1格尔德霉素,17-AAG,17-DMAG结构式Fig.1StructuresofGeldanamycin,17-AAGand17-DMAG1.1探针G1的合成路线65合成路线:-2-
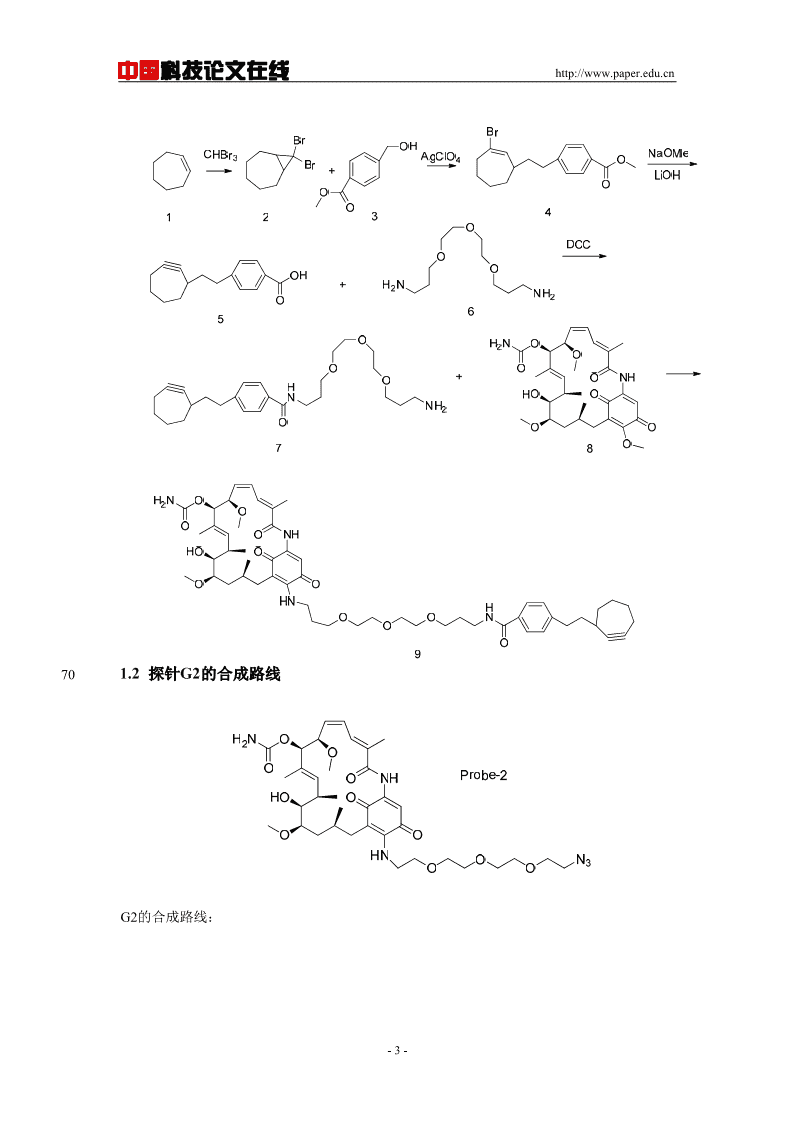
中国科技论文在线http://www.paper.edu.cn701.2探针G2的合成路线G2的合成路线:-3-
中国科技论文在线http://www.paper.edu.cn751.3探针G3的合成路线H2NOOOONHProbe-3HOOOOHHNOONOO80合成路线设计:85-4-
中国科技论文在线http://www.paper.edu.cn1.4报告基团RB1的合成路线90本课题通过改造罗丹明B使之成为可以应用的报告基团。已知罗丹明B改造的构效关系,如果在其羧基引入伯胺会使其在pH为中性时分子内部形成5元环,而失去荧光特性。为了保持其荧光特性,因此引入哌嗪基。95报告基团RB1的合成路线:100本课题设计合成的RB1最大吸收波长在586nm以上,激发后的发射波长在600nm以上,接下来的点击化学标记实验证明了该报告基团具有很好的应用价值。-5-
中国科技论文在线http://www.paper.edu.cn2G1、G2、G3与GM-FITC竞争结合Hsp90α实验用来对本课题设计合成的上述三个探针进行Hsp90亲和实验里用到的已知荧光报告基[13]团(GM-FITC,KDs=33.8±1.2nM)按文献报导合成。105图2GM-FITCFig.2StructureofGM-FITC110荧光偏振分析法(FluorescencePolarizationAssay,FPA)是一种定量分析技术,其基本原理是带有荧光基团的物质经偏振光照射(485nm),荧光吸收进入激发状态,并能再次回复到基本状态,同时发出偏振光在525nm。其荧光偏振的强弱取决于荧光分子的大小,与激发状态的荧光转动速度呈反比。FPA采用竞争反应的原理,在缺乏未标记分析物(通常是待测样品)时荧光信号最强;115加入未标记分析物后,在已标记和未标记样品之间的竞争将减弱荧光信号。荧光信号强度与游离的分析物的浓度成正比,与待测样品中未标记分析物的浓度成反比。通过测定一系列已知浓度的标准晶,绘制竞争结合抑制标准曲线。经与标准反应曲线比较而得到定量值。以测定半抗原药物的浓度为例,反应体系出了分子探针之外,还需要加入荧光标记物质,通过与大分子抗体的竞争结合作用。当药物探针分子浓度增高时,与大部分抗体发生竞争结合作用,120标记药物分子成游离状态,在系统中高速转动,荧光强度很低。如果待测药物浓度降低时,标记药物与抗体发生特异性结合,形成大分子复合物,在液相中转动速度较慢,此时检测到的偏振荧光强度也较高。为了测定G1、G2、G3与Hsp90α结合程度,将不同浓度的G1、G2、G3加入到特定浓度的GM-FITC(5nM)与Hsp90α(30nM)之中,测定FP的变化。(见图3)-6-
中国科技论文在线http://www.paper.edu.cn125图3G1、G2、G3与Hsp90α结合程度Fig.3CompetitionassayusingG1,G2,G3todisplaceGM-FITCbindingtoHsp90α通过与GM-FITC竞争性结合Hsp90α实验,可以看到G2表现出很强的竞争结合Hsp90α130能力(EC50=13nM)。这与格尔德霉素C-17取代构效关系结论一致,即取代碳链越短其与Hsp90亲和越容易。HSP90受体蛋白与信号转导、细胞周期调控和凋亡路径有关,即HSP90通过其受体多环节多途径影响癌细胞生长和或存活。HSP90与凋亡的关系日益引起人们的重视,当细胞受到外界刺激,HSP90在引导肿瘤细胞存活,或诱导肿瘤细胞发生凋亡,起到重要的作用。135HSP90具有重要的生理功能,决定细胞生存或凋亡。在凋亡发生过程中,HSP90可以通过阻止procaspase-9与凋亡蛋白酶活化因子1凋亡体的结合而抑制凋亡的发生。格尔德霉素衍生物的生物活性与结合Hsp90的能力紧密相关。在之前的竞争G2与GM-FITC竞争结合Hsp90α实验中发现G2与Hsp90α具有很强的亲和作用,因此本部分实验利用G2-RB1-Hsp90α建立了适用于高通量筛选的模型。140我们通过监测G2(2nM)与Hsp90α(30nM)亲和反应3小时后加入RB1(2nM)和CuI(1nM)发现点击化学的反应效率极高,加入后30秒后mp就几乎保持恒定。证明使用G2与Hsp90α亲和反应后,利用RB1进行点击化学测定荧光强度变化是可以用来建立高通量筛选模型的。恒定浓度G2(2nM)与不同浓度的Hsp90α(0-125nM)在不同作用时间下mP荧光强度(总荧光减去未加Hsp90α的荧光强度)。见图4-7-
中国科技论文在线http://www.paper.edu.cn145图4恒定浓度G2与不同浓度的Hsp90α在不同作用时间下mP荧光强度图Fig.4FluorescenceintensityofcertainconcentrationG2actedwithdifferentconcentrationHsp90αatdifferenttimepoints由上图可以看出,FP强度变化范围0-125mP(G2与Hsp90α亲和饱和状态),通过Prime150软件计算得出Kd=5.1±1.1nM,比之前文献报导的格尔德霉素Hsp90α亲和能力(200nM)高出很多。同时发现Hsp90α浓度超过30nM后mP变化不大,因此选择使用Hsp90α(30nM)进行高通量筛选就可以。恒定浓度G2(2nM)与不同浓度的Hsp90α(0-125nM)在不同作用时间下总荧光强度见图5.155图5恒定浓度G2与不同浓度的Hsp90α在不同作用时间下总荧光强度Fig.5TotalfluorescenceintensityofcertainconcentrationG2actedwithdifferentconcentrationHsp90αatdifferenttimepoints160通过上述2个实验发现,G2(2nM)与不同浓度的Hsp90α(0-125nM)结合后荧光变化占总荧光比重(大于80%)。说明G2与Hsp90α结合后用RB1点击结合后,比空白游离的G2-RB1荧光强度有显著改变,同时反应进行3h后进行高通量筛选为较佳时间。-8-
中国科技论文在线http://www.paper.edu.cn为了得到作为高通量筛选的合适G2浓度,将不同浓度的G2(0-160nM)单独、G2和格尔德霉素(GA,0.5)与Hsp90α(30nM)、G2-RB1空白测定mP。见图6,165可以看出G2在2nM时与Hsp90α(30nM)结合荧光强度最大。图6不同浓度的G2、G2和格尔德霉素与Hsp90α、G2-RB1空白测定mPFig.6FluorescenceintensityofdifferentconcentrationG2,G2andGeldanamycinactedwithHsp90αandG2-RB1atdifferenttimepoints170为了测定DMSO含量对mP的影响,用不同含量的DMSO加入到G2(2nM)与Hsp90α(30nM)亲和反应3小时,加入RB1(2nM)和CuI(1nM)。结果见图7。175图7DMSO含量对mP的影响Fig.7TheeffectsofDMSOcontentonFluorescenceintensity从结果可知,DMSO(v/v)含量不超过4%为佳。最后优化的条件为G2(2nM)与Hsp90α(30nM)亲和反应3小时,加入加入RB1(5nM)和CuI(1nM),DMSO(v/v)含量不超过4%为佳。180通过该条件对已知的Hsp90抑制剂格尔德霉素、TPR2A、ATP、ADP进行了EC50测定。结-9-
中国科技论文在线http://www.paper.edu.cn果分别为104±3.1,31±3.9,43.0±2.2,190±11.0nM。3细胞增殖抑制实验(MTT)采用FTC-133、FTC-236和FTC-238细胞株,分别加入20μL浓度为50,20,10、1uM的G2或GA。实验结果显示,在三组实验中,G2均表现出与GA相似的抗肿瘤活性。在浓185度为50uM时,抗肿瘤活性最佳,对肿瘤细胞增殖的抑制率都在80%以上,且抗肿瘤活性呈现出明显的剂量依赖性,随着药物浓度的降低,其对肿瘤细胞增殖的抑制率逐渐下降。在浓度为10uM时,对肿瘤细胞增殖的抑制率达50%以上;在浓度为1uM时,抗肿瘤活性最差。具体结果详见表1和图8.190表1GA和G2对FTC-133、FTC-236和FTC-238肿瘤细胞增殖抑制作用(n=3)Tab.1ProliferationinhibitionofGAandG2onFTC-133、FTC-236和FTC-238(n=3)FTC-133FTC-236FTC-238浓度(uM)GAG2GAG2GAG25093.0290.2395.0890.5489.0480.082090.5080.3289.3275.4185.4676.971056.0850.5471.9669.3671.4565.02133.0910.1548.1933.2560.3222.97图8GA和G2对三种肿瘤细胞增殖抑制作用(n=3)195Fig.8ProliferationinhibitionofGAandG2onFTC-133、FTC-236和FTC-238(n=3)4细胞蛋白标记分析采用设计合成的格尔德霉素化学小分子G2探针与罗丹明B荧光报告基团,在点击化学条件下,对FTC-133肿瘤细胞进行蛋白标记分析,经SDS-PAGE分离,采用凝胶荧光扫描成像系统对结果进行分析,实验结果如图9。-10-
中国科技论文在线http://www.paper.edu.cn200结果显示:(1)通过点击化学反应,格尔德霉素化学小分子探针与罗丹明荧光报告基团成功链接,并标记靶点蛋白(见荧光条带);(2)从荧光条带呈现的颜色深浅变化可以看出,靶点蛋白标记荧光强弱于探针浓度高低密切相关;当药物浓度从50,20,10,5uM依次递减时,荧光条带从深至浅渐变;(3)由格尔德霉素化学小分子探针G2标记位于72kDa,56kDa,23kDa蛋白,经高浓度(100)底物GA的竞争抑制作用后,这三条蛋白荧光条带消205失或明显变弱;因此,这三条蛋白条带极有可能是GA的靶点蛋白,其中72kDa蛋白与HSP90AB1分子量相近,56kDa和23kDa蛋白则有可能是GA新的靶点蛋白。图9G2细胞蛋白标记图Fig.9G2proteomelabelingandanalysis2105结论本研究共设计合成了格尔德霉素化学小分子探针3个。通过与GA-FITC竞争结合HSP90α实验,发现G2与HSP90α具有较强的亲和作用(EC50=13nM)。同时设计合成了适用于点击化学带末端炔基功能性罗丹明B。通过细胞靶点蛋白标记实验,取得了良好的标记效果。建立了G2-RB1-HSP90α用作高通量筛选(HTS)模型的,并通过该条件对已知的Hsp90215抑制剂格尔德霉素、TPR、TPR2A、ATP、ADP进行了EC50测定。其结果表明利用ABPP-CC建立高通量筛选(HTS)模型优于先前报道的GA-FITC-HSP90α并采用MTT法对G2抗肿瘤活性进行评价;通过对比发现,设计合成的格尔德霉素G2化学小分子探针与格尔德霉素具有相似的抗肿瘤细胞增殖抑制作用;在细胞蛋白标记实验中,均采用FTC-133肿瘤细胞株;第一组给以不同浓度的探针G2,第二组给以不同浓度的-11-
中国科技论文在线http://www.paper.edu.cn220探针G2和高浓度的格尔德霉素原药;当探针于靶点蛋白结合后,加入含有荧光标记物RB1的点击化学配方,使荧光标记物与格尔德霉素化学小分子探针点击链接,以此来标记靶点蛋白;过量的格尔德霉素将通过竞争结合靶点蛋白与探针组进行对照;随后采用SDS-PAGE对蛋白进行分离,采用凝胶荧光扫描成像仪对结果进行分析,通过对两组荧光条带进行对比,验证了本课题设计合成的化学小分子探针与格尔德霉素具有至少3个共同作用的靶点蛋白。225[参考文献](References)[1]COOKJ,HUNTERG,VERNONJ.TheFutureCosts,RisksandRewardsofDrugDevelopment[J].Pharmacoeconomics,2009,27(5):355-363.[2]CHIOSISG,TIMAULM,LUCASB,AsmallmoleculedesignedtobindtotheademinenucleotidepocketofHsp90causesHer2degradationandthegrowtharrestanddifferentiationofbreastcancercells[J],ChemBiol,2001,2308(3):289-299.[3]HEINC,LIUX,WANGD,Clickchemistry,apowerfultoolforpharmaceuticalsciences[J].PharmRes,2008,25(10):2216-2230.[4]LEDROURNAGUETB,VELONIAK.Macromol,Clickchemistry:apowerfultooltocreatepolymer-basedmacromolecularchimeras[J].RapidCommun,2008,29(12/13):1073-1089.235[5]BINDERW,SACHSENHOFERR.Macromol."Click"chemistryinpolymerandmaterialscience:anupdate[J].RapidCommun,2008,29(12/13):952-981.[6]GOLASP,MATYJASZEWSKIK.ClickchemistryandATRP:abeneficialunionforthepreparationoffunctionalmaterials[J].QSARCombSci,2007,26(11-12):1116-1134.[7]BaskinJM,PrescherJA,LaughlinST,AgardNJ,ChangPV,MILLERI,LOA,CODELLIJ,BertozziC240R.Copper-freeclickchemistryfordynamicinvivoimaging[J].ProcNatlAcadSci,USA,2007,104(43):16793-16797.[8]TORNOEC,CHRISTENSENC,MELDALM.PeptidotriazolesonSolidPhase:[1,2,3]-TriazolesbyRegiospecificCopper(I)-Catalyzed1,3-DipolarCycloadditionsofTerminalAlkynestoAzides[J].JOrgChem,2002,67(9):3057-3064.245[9]KALSSHK,YANGP,SrinivasanR,etal.Clickchemistryasahigh-throughputamenableplatforminCatalomics[J].QSARCombSci,2007,26(11/12):1135-1144.[10]SALISBURYC,CRAVATTB.Clickchemistry-ledadvancesinhighcontentfunctionalproteomics[J].QSARCombSci,2007,26(11/12):1229-1238.[11]ROESMP,OBRIENR,StructuralbasisforinhibitionoftheHsp90molecularchaperonebytheantitumor250antibioticsradicicolandgeldanamycin[J],JMedChem,1999,42(2):260-266.[12]SCHULTET,AKINAGAS,SOGAS,AntibioticradicicolbindstotheN-terminaldomainofHsp90andsharesimportantbiologicactivitieswithgeldanamycin[J],CellStressChaperones,1998,3(2):100-108.[13]LAURAL,SARAJ.SynthesisofNovelFluorescentProbesfortheMolecularChaperoneHsp90[J].BoorgMedChemLett,2003;13:3975-3978.255-12-'
您可能关注的文档
- 基于SIFT的图像复制粘贴篡改检测.pdf
- 基于分层技术的快速最大方差展开算法及其在过程监测中的应用.pdf
- 基于区域映射与全概率模型的多示例图像检索方法.pdf
- 基于卫星测高回波波形的南极海域重力异常研究.pdf
- 基于异丙醇锆阴极修饰层的高效聚合物太阳能电池.pdf
- 基于机器学习的信号测向方法.pdf
- 基于格兰杰因果关系磁刺激穴位对亚健康失眠的脑功能网络分析.pdf
- 基于正弦波波形的电网电压监测.pdf
- 基于毛细管结构的热式风速传感器设计.pdf
- 基于生态原理的亚热带可持续农林复合经营评价.pdf
- 基于移动设备多传感器融合的室内定位系统.pdf
- 基于组氨酸的药物基因载体在癌症诊疗中的应用.pdf
- 基于能量峰值检测的UWB导频模式估计算法.pdf
- 基于负载均衡的VANET跨层贪婪路由算法.pdf
- 基于逆向技术的采煤机导向滑靴设计优化.pdf
- 多功能高强度水凝胶的构建及其生物医学应用.pdf
- 多小区协作上行链路系统中一种以用户为中心的动态分簇算法.pdf
- 大豆花叶病毒抗性鉴定及抗病种质筛选.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明