- 398.64 KB
- 2022-04-22 13:43:11 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中国科技论文在线http://www.paper.edu.cn基于Fe3O4和Man-CQDs纳米探针双标记#模式定量检测沙门氏菌12**赵斌,徐溢5(1.重庆大学化学化工学院,重庆400044;2.重庆大学光电工程学院微系统研究中心,重庆400044)摘要:沙门氏菌是常见的肠道致病菌,一直威胁着人类的生命安全,建立一种快速、高灵敏的沙门氏菌检测方法,对于国家食品安全具有重要的意义。本文以柠檬酸为碳源,通过水热10法制备得到荧光碳量子点(CQDs),基于其表面丰富的羧基将氨基化甘露糖以酰胺键的形式修饰在其表面制备得到Man-CQDs纳米探针,并以相同的方式将氨基化甘露糖修饰在商品化的Fe3O4表面,制备得到Man-Fe3O4纳米探针。在混菌溶液中Man-Fe3O4探针选择性地识别捕获沙门氏菌,在外加磁场的作用下,分离得到Bacteria-Man-Fe3O4复合物,再利用Man-CQDs对捕获的沙门氏菌进行荧光标记,利用荧光光谱仪对双标记的沙门氏菌进行荧光15测试。结果显示沙门氏菌的浓度的对数与对应荧光值存在良好的线性关系,线性方程为-1-1IFL=217.2Log(c)-758.8(R2=0.9578),线性范围为104cfu•mL-107cfu•mL,检测限为5×103-1cfu•mL。本文所建立的基于磁性纳米探针的双标记模式检测沙门氏菌的方法,具有快速、高选择性和高灵敏的优点。关键词:沙门氏菌;双标记;荧光光谱法20中图分类号:Q93-332QuantitativedetectionofSalmonellabyDualrecognitionwithMan-Fe3O4andMan-CQDsprobes12ZHAOBin,XUYi25(1.Collegeofchemistryandchemicalengineering,ChongqingUniversity,Chongqing400044;2.MicrosystemResearchCenter,SchoolofOptoelectronicEngineering,ChongqingUniversity,Chongqing400044)Abstract:Salmonellaisacommonintestinalpathogenicbacteria,whichhasbeenthreateningthesafetyofhumanlife.Itisimportanttoestablisharapidandsensitivemethodforthedetectionof30salmonella.Inthepaper,citricacidwasusedascarbonsourceforpreparingfluorescentCQDs.DuetotheobtainedCQDswasrichincarboxylgrouponthesurface,Man-CQDswassynthesizedbyimmobilizing4-Aminopheny-l-α-D-mannopyanosideonsurfaceofCQDsviacovalentbond.Man-Fe3O4wasobtainbythesameway.Inthemixedsolution,Salmonellawasselectivelycaptured,andSalmonella-Man-Fe3O4complexeswasisolatedbyexertingexternalmagneticfield.35Morever,thecapturedSalmonellawaslabeldbyMan-CQDs,Salmonellalabeleddoublerecognitionwastestbyfluorescencespectroscopy.TheresultsshowthatthereisagoodlinearrelationshipbetweenthelogarithmoftheconcentrationofSalmonellaandthecorrespondingfluorescencevalue,linearequationIFL=217.2Log(c)-758.8(R2=0.9578),thelinearrangeis104cfu-mL-1-107cfu-mL-1,thedetectionlimitis5×103CFU-mL-1.AmethodfordetectionofSalmonellabacteriabasedonthe40magneticnano-probeswasdeveloped.Keywords:Salmonella;dualrecnogtion;Fluorescencespectrometry基金项目:重庆市科学技术委员会社会民生科技创新一般项目[cstc2015shmszx00014]和重庆市科学技术委员科技惠民计划项目【cstc2015jcsf8001】等资助作者简介:赵斌(1990-),男,硕士研究生,主要研究方向:新型纳米粒子的制备及其用于微生物的定量检测通信联系人:徐溢(1966-),教授,博士生导师,主要从事分析化学、应用化学和微型集成生化分析系统等领域研究工作.E-mail:1804366887@qq.com-1-
中国科技论文在线http://www.paper.edu.cn0引言45细菌的定量检测直接关系着国家的食品安全。目前传统的细菌检测方法主要有平板计数法、多管发酵法、滤膜法等,这些检测方法都存在操作复杂、耗时长,难以实现快速检测,且检测过程中常常遇到样品成分较为复杂,背景干扰物质较多,影响检测结果,需要检测对[1]样本繁琐的预处理,这就要求建立一种快速、高灵敏的检测方法。基于纳米探针的细菌检测方法是目前细菌检测研究的热点,磁性纳米探针具有良好的磁性,可实现在复杂样本中选50择性捕获目标菌,荧光纳米探针具有良好的荧光性能,可实现对细菌高效地荧光标记,从而实现高灵敏地检测。将两者纳米探针的性能结合,发挥两者捕获和荧光标记的协同作用,可[2][3]实现混合菌液中目标菌的快速、高选择性和高灵敏度地定量检测。ÜzeyirDogan等在Fe3O4@Au纳米粒子表面修饰了大肠杆菌的抗体得到磁性纳米探针,同时在壳聚糖包裹的QDs表面也修饰了同种大肠杆菌的抗体,制备得到荧光纳米探针,采用磁性纳米探针和荧55光纳米探针在溶液中对大肠杆菌进行双标记,实现了对细菌的磁捕获和荧光标记。结果表明28-1大肠杆菌细菌的浓度与检测荧光值在10-10cfu•mL存在良好的线性关系,检测限为30-1cfu•mL,极大地降低了检测限。将磁性纳米粒子和荧光纳米粒子结合,用于复杂样本中对目标菌的捕获和荧光标记,建立一种在复杂溶液中快速检测目标菌的荧光检测方法。基于磁性纳米粒子良好的磁性和碳量子点高的荧光量子产率特性,本文拟在Fe3O4纳米60粒子和CQDs表面修饰上甘露糖,制备得到Man-Fe3O4的磁性纳米糖探针和Man-CQDs的荧光纳米糖探针。实验首先在合成的混菌样本溶液中采用Man-Fe3O4纳米探针选择性地识别捕获沙门氏菌,再结合Man-CQDs纳米探针对捕获的沙门氏菌进行荧光标记,最后采用荧光光谱仪检测双标记的细菌的荧光信号,基于这种双标记的模式实现在混合菌液中对沙门氏菌的定量检测。651实验试剂及仪器RF-5301荧光光谱仪、UV-2450紫外可见光分光光度计和IRprestige-21傅里叶红外光谱仪(日本岛津);LB培养基、营养琼脂购自上海生工;柠檬酸、、4-氨基苯基-α-D-吡喃甘露糖苷(简写为A-D-mannopyanoside)、(1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐)70(EDC)、奎宁均购自上海阿拉丁生化科技股份有限公司,分析纯;乙二胺、N-羟基琥珀酰亚胺(NHS)等购自成都科龙化工试剂厂,分析纯;其他试剂均为分析纯;实验用水为二次蒸馏水;实验是在常温常压下进行。磷酸盐缓冲溶液(PBS)配制:精确称取0.24gKH2PO4,1.44gNa2HPO4,8gNaCl,0.2gKCl溶于去离子水中,用0.1moL/L的NaOH调节pH至7.4.75大肠杆菌DH5a/沙门氏菌S.123443标本:菌种均由第三军医大学检验系提供。在LB培养基中培养37℃培养1214h;将原菌液在8000rpm,离心3min,去除上清液后重悬于PBS缓冲液中,重复离心23次,最后悬浮在PBS缓冲液中。-2-
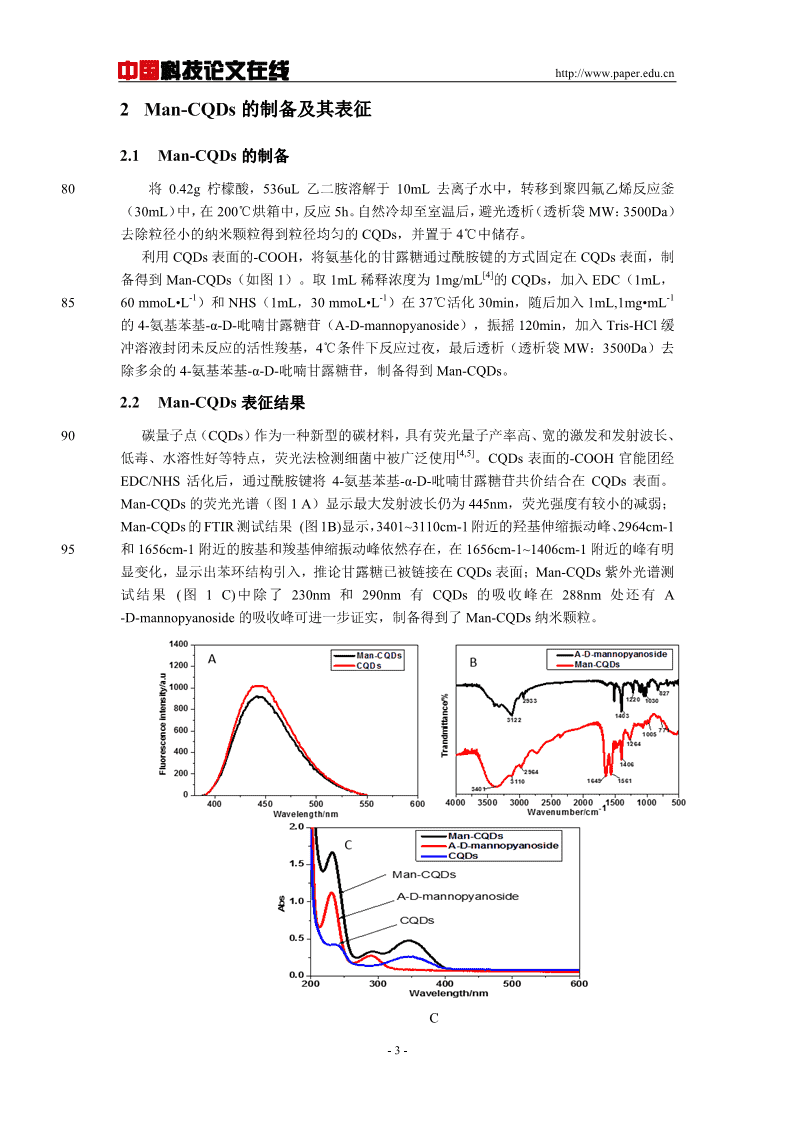
中国科技论文在线http://www.paper.edu.cn2Man-CQDs的制备及其表征2.1Man-CQDs的制备80将0.42g柠檬酸,536uL乙二胺溶解于10mL去离子水中,转移到聚四氟乙烯反应釜(30mL)中,在200℃烘箱中,反应5h。自然冷却至室温后,避光透析(透析袋MW:3500Da)去除粒径小的纳米颗粒得到粒径均匀的CQDs,并置于4℃中储存。利用CQDs表面的-COOH,将氨基化的甘露糖通过酰胺键的方式固定在CQDs表面,制[4]备得到Man-CQDs(如图1)。取1mL稀释浓度为1mg/mL的CQDs,加入EDC(1mL,-1-1-18560mmoL•L)和NHS(1mL,30mmoL•L)在37℃活化30min,随后加入1mL,1mg•mL的4-氨基苯基-α-D-吡喃甘露糖苷(A-D-mannopyanoside),振摇120min,加入Tris-HCl缓冲溶液封闭未反应的活性羧基,4℃条件下反应过夜,最后透析(透析袋MW:3500Da)去除多余的4-氨基苯基-α-D-吡喃甘露糖苷,制备得到Man-CQDs。2.2Man-CQDs表征结果90碳量子点(CQDs)作为一种新型的碳材料,具有荧光量子产率高、宽的激发和发射波长、[4,5]低毒、水溶性好等特点,荧光法检测细菌中被广泛使用。CQDs表面的-COOH官能团经EDC/NHS活化后,通过酰胺键将4-氨基苯基-α-D-吡喃甘露糖苷共价结合在CQDs表面。Man-CQDs的荧光光谱(图1A)显示最大发射波长仍为445nm,荧光强度有较小的减弱;Man-CQDs的FTIR测试结果(图1B)显示,3401~3110cm-1附近的羟基伸缩振动峰、2964cm-195和1656cm-1附近的胺基和羧基伸缩振动峰依然存在,在1656cm-1~1406cm-1附近的峰有明显变化,显示出苯环结构引入,推论甘露糖已被链接在CQDs表面;Man-CQDs紫外光谱测试结果(图1C)中除了230nm和290nm有CQDs的吸收峰在288nm处还有A-D-mannopyanoside的吸收峰可进一步证实,制备得到了Man-CQDs纳米颗粒。C-3-
中国科技论文在线http://www.paper.edu.cn100图1Man-CQDs的表征结果图:(A)CQDs和Man-CQDs的荧光光谱图;(B)Man-CQDs的红外光谱图;(C)A-D-mannopyanoside、CQDs和Man-CQDs的紫外光谱图;Fig.1CharacterizationresultsofMan-CQDs;(A)FluorescencespectraofCQDsandMan-CQDs;(B)FITRspectraofMan-CQDs;(C)UV/visspectraofMan-CQDs,A-D-mannopyanosideandCQDs1053Man-Fe3O4的制备及其表征3.1Man-Fe3O4的制备-1取60μL,1mg•mL的COOH-Fe3O4于玻璃瓶中,外加磁力富集去除上清液后,加入-1-1300μLEDC(200mmoL•L)和300μLNHS(50mmoL•L)的混合溶液,振摇反应30min,-1活化磁珠表面的羧基。加入300μL(1mg•mL)4-氨基苯基α-D-吡喃甘露糖苷,避光振摇11060min。加入300μL1%牛血清白蛋白溶液,避光振荡2h,封闭未结合的活性羧基,避免非特异性吸附。最后,在外加磁力的作用下,将多余未反应完的4-氨基苯基α-D-吡喃甘露糖-1苷去掉,用200μL7.4PBS缓冲液洗涤3次,最终重悬至300μL,得到约为0.2mg•mL的Man-Fe3O4溶液,保存于4℃条件下,备用。3.2Man-Fe3O4的表征结果115基于Fe3O4磁性纳米粒子表面的羧基,在EDC/NHS活化后,将修饰有氨基的甘露糖通过酰胺键将甘露糖固定在Fe3O4表面,制备得到Man-Fe3O4。利用UV-vis和FITR对进行结构表征。由于Fe3O4纳米粒子在水溶液中是非均相体系,测试过程出现沉降,导致UV-vis测试基线下降。Man-Fe3O4纳米探针的紫外测试结果显示在289nm处,出现了氨基化甘露糖的吸收峰,说明甘露糖已经成功接枝在Fe3O4纳米粒子的表面(图2A)。Fe3O4纳米粒子的-1-1120红外光谱测试结果显示1625cm的C=O吸收峰和3120cm处的-OH的特征峰,主要来自Fe3O4纳米粒子表面的-COOH(图2B)。Man-Fe3O4纳米探针的红外光谱测试结果显示,3395-1-1cm和3335cm的特征吸收峰分别是羧基中-OH的伸缩振动峰和酰胺键中N-H的伸缩振动-1-1-1峰;2940cm处是甘露糖分子结构中C-H特征吸收峰;1500cm和1585cm是氨基化甘露-1-1糖结构中苯环的特征峰;970cm~1200cm之间一系列吸收峰主要来自苯环的C=C指纹-1125吸收峰;830cm是苯环对位有取代基C-H指纹吸收峰(图3C)。因此根据紫外光谱和红外光谱测试结果显示氨基化甘露糖成功修饰在Fe3O4磁性纳米粒子表面,制备得到了Man-Fe3O4纳米探针。-4-
中国科技论文在线http://www.paper.edu.cn图2Man-Fe3O4的表征结果:A.Man-Fe3O4纳米粒子的紫外光谱图;B.Fe3O4纳米粒子的红外光谱图;130C.Man-Fe3O4纳米粒子的红外光谱图Fig2CharacterizationresultsofMan-Fe3O4:A.TheUVspectrogramofMan-Fe3O4;B.TheIRspectrogramofFe3O4;C.TheIRspectrogramofMan-Fe3O44Man-Fe3O4和Man-CQDs双标记模式选择性识别标记沙门氏菌1354.1合成样本的制备及其沙门氏菌的检测4.1.1合成样本的制备8-1在7个4mL的离心管中加入1mL,10cfu·mL的大肠杆菌DH5a溶液中,然后依次在7-16-16-15-17个离心管中加入不同浓度(10cfu·mL,10cfu·mL,5×10cfu·mL,10cfu·mL,4×5-14-15-110cfu·mL,10cfu·mL,3×10cfu·mL)的沙门氏菌溶液,制备得到含有不同浓度沙门氏140菌的混菌溶液。4.1.2沙门氏菌定量检测-1在新制的合成样本中分别加入200uL的Man-Fe3O4(1mg·mL),室温下孵育60min,外加磁力,去除上清液,底部沉淀物用PBS缓冲液洗23次后,加入200uL的Man-CQDs-1(0.162mg·mL)室温下孵育60min,外加磁力,去除上清液,底部沉淀物用pH=7.4PBS145缓冲液洗23次后,重悬定容3mL。利用荧光光谱仪测试重悬液的荧光信号。4.2合成样本中沙门氏菌检测结果分析在合成样本中加入Man-Fe3O4结合后,通过外加磁力将未标记的细菌和干扰物质去除,重悬后加入Man-CQDs进行荧光标记,通过外加磁力将多余的标记试剂去除后重悬进行荧光150光谱测试。荧光测试结果显示,采用Man-Fe3O4和Man-CQDs能够定量检测混合菌液中的沙门氏菌,并且沙门氏菌的浓度的对数与相对荧光值存在良好的线性关系,线性方程IFL=217.-5-
中国科技论文在线http://www.paper.edu.cn247-13-12Log(c)-758.8(R=0.9578),线性范围为10-10cfu•mL,检测限为5×10cfu•mL。该方法以甘露糖为识别元件,采用双标记模式,实现了沙门氏菌的定量检测,相较于抗体,适配体等识别元件,检测的灵敏度还有待提高,但糖分子本身具有无毒和价格低廉的特点,仍然是[6,7]155值得进一步的研究。8008007007007-160010cfu·mL600500500/a.u400400IFL/a.u300IFL3-13005×10cfu·mL20020010010000400450500550600λ/nm3.54.04.55.05.56.06.57.07.5Log(c)图3A.系列浓度的沙门氏菌加入到大肠杆菌DH5a中Fe3O4-Man和Man-CQDs标记后的荧光测试图;B.系列浓度沙门氏菌浓度的对数与Fe3O4-Man和Man-CQDs标记后的荧光强度的线性拟合Fig.3A.ThefluorescencespectrumofvariousconcentrationofS.typhimuriumwhichaddedintoE.coli160DH5alabeledMan-Fe3O4andMan-CQDs;B.ThelinearfittingofthefluorescenceintensityofbacterialabeledMan-Fe3O4andMan-CQDsandlogarithmofbacteriaofvariousconcentration5结论本文基于磁性纳米探针和荧光纳米探针双标记模式实现了混合菌液中沙门氏菌的定量检测。通过在混合菌液中加入磁性纳米探针捕获沙门氏菌,在外加磁场作用下,分离得到被165捕获的沙门氏菌,再加入荧光纳米探针对其进行荧光标记,采用荧光光谱仪对标记的细菌进行荧光信号测试,实现了沙门氏菌的定量检测。实验制备得到了磁性Man-Fe3O4纳米探针,利用紫外光谱和红外光谱对其进行了结构表征,结果显示甘露糖成功地修饰在Fe3O4纳米粒子表面。基于Man-Fe3O4和Man-CQDs纳米探针双标记模式对大肠杆菌DH5a和沙门氏菌的混合菌液中的沙门氏菌进行了检测,结果显示沙门氏菌的浓度的对数与对应荧光值存在良好247-1170的线性关系,线性方程为IFL=11.59Log(c)-709.8(R=0.9874),线性范围为10-10cfu•mL,3-1检测限为5×10cfu•mL。该方法充分利用磁性纳米探针和荧光纳米探针的磁捕获和高效率荧光标记的特性,实现了复杂样本中快速识别捕获目标菌并实现了荧光标记的过程,避免了检测前对样本复杂的处理过程,实现了快速、高选择性和高灵敏度的细菌检测的目标。[参考文献](References)175[1]PeterJV,KristaRW.NanomaterialEnabledBiosensorsforPathogenMonitoring-AReview[J].EnvironSciTechnol,2010,44(3656-69.[2]PramanikA,JonesS,PedrazaF,etal.Fluorescent,MagneticMultifunctionalCarbonDotsforSelectiveSeparation,Identification,andEradicationofDrug-ResistantSuperbugs[J].ACSOmega,2017,2(2):554-62.[3]DoganÜ,KasapE,CetinD,etal.Rapiddetectionofbacteriabasedonhomogenousimmunoassayusing180chitosanmodifiedquantumdots[J].SensorsandActuatorsB:Chemical.2016,233:369-78.[4]BhushanB,KumarSU,GopinathP.Multifunctionalcarbondotsasefficientfluorescentnanotagsfortrackingcellsthroughsuccessivegenerations[J].JournalofMaterialsChemistryB,2016,4(28):4862-71.[5]ZhuS,MengQ,WangL,etal.HighlyPhotoluminescentCarbonDotsforMulticolorPatterning,Sensors,andBioimaging[J].AngewandteChemie-InternationalEdition.2013,52(14):3953-7.-6-
中国科技论文在线http://www.paper.edu.cn185[6]LuoPG,WangH,GuL,etal.SelectiveInteractionsofSugar-FunctionalizedSingle-WalledCarbonNanotubeswithBacillusSpores[J].ACSNano.2009,3(12):3909-16.[7]MukhopadhyayB,MartinsMB,KaramanskaR,etal.Bacterialdetectionusingcarbohydrate-functionalisedCdSquantumdots:amodelstudyexploitingE.colirecognitionofmannosides[J].TetrahedronLetters.2009,50(8):886-9.190-7-'
您可能关注的文档
- 单轴压缩条件下含瓦斯煤样力学性质研究.pdf
- 双斜盘串联式液压变压器流场特性分析.pdf
- 双曲积的渐近上曲率.pdf
- 双氰胺改性角蛋白填料的制备与应用.pdf
- 双链RNA结合蛋白TRBP、PRKRA在miRNA成熟过程中的调控作用.pdf
- 变革型导师风格对研究生经验开放性的影响机制研究.pdf
- 同伴压力对消费者减排行为的影响分析.pdf
- 噬菌体展示筛选与狂犬病毒P互作的宿主蛋白.pdf
- 国内科学学的学术群体与研究热点分析.pdf
- 基于QAR数据的飞行环境及驾驶操作定量评价模型.pdf
- 基于SOI结构的光波导表面光滑化机理.pdf
- 基于Web的PM2.5监测预警系统的设计.pdf
- 基于WEB的三维树木监管系统设计与实现.pdf
- 基于两级插值的图像矩阵补全.pdf
- 基于动态体压分布的汽车座椅振动舒适度预测.pdf
- 基于卷积神经网络的路面病害检测技术.pdf
- 基于平方根无迹卡尔曼滤波的机器人无标定视觉伺服.pdf
- 基于微波退火技术制备的高性能短沟道金属源漏Ge pMOSFET.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明