- 400.99 KB
- 2022-04-22 13:42:58 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中国科技论文在线http://www.paper.edu.cn冰片基咔咯衍生物的合成、表征及其抗癌活#性研究**喻笑笑,康熙元,郭颖昕,房仙颖,徐海军5(南京林业大学化学工程学院,江苏生物质能源与化学品重点实验室,南京,210037)摘要:使用吡咯和冰片基芳醛为原料,设计并合成了2个无金属冰片基咔咯衍生物3和6,使用核磁共振氢谱、质谱、元素分析及紫外-可见吸收光谱对它们进行了结构表征,并使用MTT法研究了它们对肝癌细胞的抗癌活性,初步研究结果表明,化合物3比化合物6显示出更强的抗癌活性,在生物医学上可能具有潜在的应用前景。10关键词:咔咯;冰片;合成;抗癌活性中图分类号:O621.3Synthesis,CharacterizationandAnticancerActivityofCorroleDerivativeswithBorneolYuXiao-Xiao,KanXi-Yuan,GuoYing-Xin,FangXian-Ying,XuHai-Jun15(CollegeofChemicalEngineering,JiangsuKeyLabofBiomass-basedGreenFuelsandChemicals,NanjingForestryUniversity,Nanjing210037)Abstract:Twocorrolederivatives3and6withborneolhavebeendesignedandsynthesized,andtheirstructureswerecharacterizedby1HNMR,MS,elementalanalysisandUv-visspectra.Theanti-canceractivityofthecorrolederivativesfortheHepG2cellwerealso20investigated.Theresultsshowedthatthecorrole3hasbetteranti-canceractivitythan6andpotentialapplicationinbio-medicine.Keywords:Corrole;Borneol;Carbazole;Anti-cancerActivity0引言25咔咯(Corrole)是由四个吡咯相连而形成的具有18个π电子共轭体系的四吡咯大[1]环化合物,在分子结构上和卟啉有一定的相似性,但比卟啉少一20位碳。咔咯能稳定结合较高氧化态的金属离子,因而它们具有独特的光化学、电化学、光物理和光生物性[2-4]质,在功能材料、光电催化、生物医药等领域有着广泛的应用前景。咔咯化合物具有特殊的电子吸收和荧光特性,而且对某些生物组织有特殊的亲和性和选择性,可以在一30定条件下聚集在体内发生病变的组织部位,并可用作癌肿瘤的检测试剂和光动力冶疗[5-7](PDT)的光敏剂。例如,5,15-二吡啶基-10-(五氟苯基)咔咯不仅能够与DNA紧密结合,并具有高单线态氧量子产率,在光照下能够有效抑制Hela细胞的生长及优良的[8]抗癌活性;另外,具有高单线态氧量子产率的meso-三(五氟苯基)咔咯能够在光照[9]下通过细胞微管损伤有效地抑制Hela细胞的生长。咔咯化合物在抗癌药物及PDT光35敏剂领域已展现出巨大的应用前景。基金项目:教育部高等学校博士学科点专项基金(20133204120009);江苏省生物质绿色燃料与化学品重点实验室开放基金(JSBGFC12002)。作者简介:喻笑笑(1991-),男,硕士研究生,精细有机合成通信联系人:徐海军(1978-),男,教授,功能有机化合物的设计、合成及性能研究.E-mail:xuhaijun_jx@163.com-1-
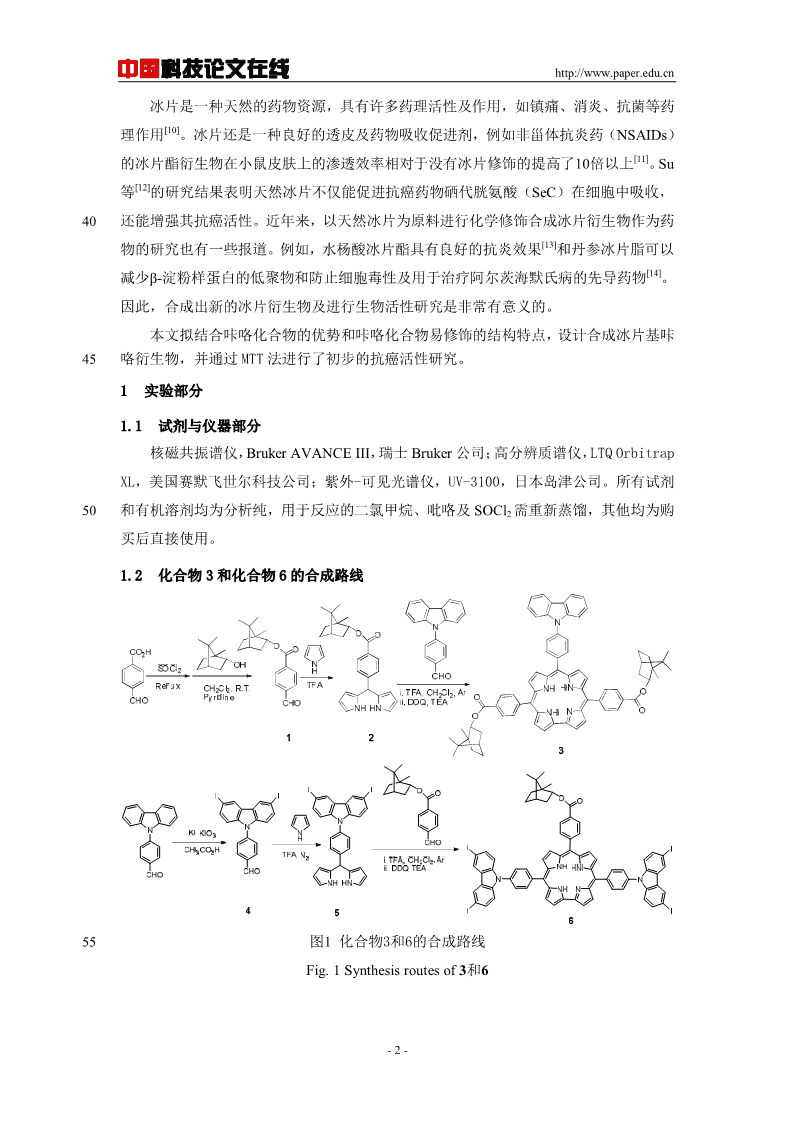
中国科技论文在线http://www.paper.edu.cn冰片是一种天然的药物资源,具有许多药理活性及作用,如镇痛、消炎、抗菌等药[10]理作用。冰片还是一种良好的透皮及药物吸收促进剂,例如非甾体抗炎药(NSAIDs)[11]的冰片酯衍生物在小鼠皮肤上的渗透效率相对于没有冰片修饰的提高了10倍以上。Su[12]等的研究结果表明天然冰片不仅能促进抗癌药物硒代胱氨酸(SeC)在细胞中吸收,40还能增强其抗癌活性。近年来,以天然冰片为原料进行化学修饰合成冰片衍生物作为药[13]物的研究也有一些报道。例如,水杨酸冰片酯具有良好的抗炎效果和丹参冰片脂可以[14]减少β-淀粉样蛋白的低聚物和防止细胞毒性及用于治疗阿尔茨海默氏病的先导药物。因此,合成出新的冰片衍生物及进行生物活性研究是非常有意义的。本文拟结合咔咯化合物的优势和咔咯化合物易修饰的结构特点,设计合成冰片基咔45咯衍生物,并通过MTT法进行了初步的抗癌活性研究。1实验部分1.1试剂与仪器部分核磁共振谱仪,BrukerAVANCEIII,瑞士Bruker公司;高分辨质谱仪,LTQOrbitrapXL,美国赛默飞世尔科技公司;紫外-可见光谱仪,UV-3100,日本岛津公司。所有试剂50和有机溶剂均为分析纯,用于反应的二氯甲烷、吡咯及SOCl2需重新蒸馏,其他均为购买后直接使用。1.2化合物3和化合物6的合成路线55图1化合物3和6的合成路线Fig.1Synthesisroutesof3和6-2-
中国科技论文在线http://www.paper.edu.cn1.3化合物3和化合物6的合成1.3.1对甲酸冰片酯苯甲醛(1)的合成在100mL圆底烧瓶中,加入对甲酰基苯甲酸(1.58g,10.00mmoL)和10mL新蒸馏60的二氯亚砜,磁力搅拌,加热到82℃回流反应10h,接着,升高温度至110℃左右,蒸馏除去过量的未反应的二氯亚砜,得到白色固体物质未经进一步提纯,直接用于下一步反应,随后,向其中依次加入(-)-冰片(1.62g,10.00mmoL)和吡啶(1.20mL,13.00mmoL)及15mL二氯甲烷,在冰水浴条件下,磁力搅拌反应1h后,移出冰浴继续室温反应12h。向反应混合物中,加入50mL二氯甲烷稀释,用饱和碳酸氢钠洗至中性,分离出有65机相再用30mL水洗多次,再用饱和氯化钠溶液洗,无水硫酸镁干燥后,真空旋蒸除去有机溶剂,得到淡黄色油状液体。粗产物经硅胶柱层析分离提纯,洗脱液为二氯甲烷/1石油醚=1:1,得白色固体。产率:59.6%。HNMR(600MHz,CDCl3)δ10.11(s,1H),8.21(d,J=8.4Hz,2H),7.96(d,J=7.8Hz,2H),5.16-5.13(m,1H),2.53-2.47(m,1H),2.14-2.09(m,1H),1.86-1.80(m,1H),1.76(t,J=4.8Hz,1H),1.47-1.41(m,1H),1.35-701.30(m,1H),1.13(dd,J=3.0,13.8Hz,1H),0.98(s,3H),0.93(s,6H)。1.3.25-4-苯甲酸冰片酯基二吡咯甲烷(2)的合成在25mL三口圆底烧瓶中,加入4-甲酰基苯甲酸冰片酯(1.15g,4.00mmol)和新蒸馏的吡咯(7mL,100.00mmol),避光及氩气保护条件下,逐滴注射入三氟乙酸(29μL,0.41mmol),室温条件下,磁力搅拌反应过夜。待反应完毕后,加入200mL二氯甲烷稀释,75再用250mLNaOH水溶液(10.20g),分两次洗涤分层,取有机相,再用水洗两次,收集有机相,无水Na2SO4干燥,真空旋蒸除去二氯甲烷(40℃)及多余吡咯(66℃),后经硅胶1柱层析分离提纯,洗脱剂为二氯甲烷,得白色固体。HNMR(600MHz,CDCl3)δ8.00(d,J=7.8Hz,4H),7.29(d,J=6.6Hz,2H),6.72(s,2H),6.16(d,J=3.0Hz,2H),5.90(s,2H),5.53(s,1H),5.10-5.08(m,1H),2.49-2.45(m,1H),2.12-2.08(m,1H),1.85-1.78(m,1H),801.74-1.71(m,1H),1.41-1.38(m,1H),1.30-1.25(m,1H),1.09(dd,J=3.0,13.8Hz,1H),0.96(s,3H),0.90(s,6H)。1.3.35,15-二-(4-甲酸冰片酯苯基)-10-(4-(9-咔唑基)苯基)咔咯(3)的合成将5-4-甲酸冰片酯苯基二吡咯甲烷(1.18g,2.80mmol)和4-(9-咔唑基)苯甲醛(0.26g,0.94mmol)加入500mL三口烧瓶,并加入干燥处理的二氯甲烷(70mL)进行溶解。氩85气保护下,逐滴加入三氟乙酸(0.002mL),在室温及避光条件下,磁力搅拌反应4h后,加入DDQ(0.86g,3.80mmol),撤除氩气氧化0.5h,反应物减压旋蒸除去有机溶剂,残留物进行硅胶柱层析分离,洗脱剂为二氯甲烷/石油醚=7:3,后经甲醇-氯仿重结晶后,1得暗紫色固体,产率:7.2%。HNMR(600MHz,CDCl3)δ8.98-8.83(m,4H),8.75(s,2H),-3-
中国科技论文在线http://www.paper.edu.cn8.58-8.51(m,11H),8.25(d,J=6.6Hz,2H),8.05-7.98(m,2H),7.88-7.84(m,2H),7.58-907.55(m,3H),7.44-7.42(m,2H),5.31-5.29(m,2H),2.67-2.61(m,2H),2.35-2.32(m,2H),1.92-1.88(m,2H),1.84(t,J=4.2Hz,2H),1.51-1.45(m,4H),1.31-1.26(m,2H),1.07(s,12H),0.99(s,6H);元素分析按C71H65N5O4,计值(%):C81.04,H6.23,N6.66;实验值-5-1-1(%):C80.97,H6.29,N6.74.UV-vis(CH2Cl2):λmax(nm)(ε×10Lmolcm):431(0.692),545(0.088),593(0.101),655(0.131)。951.3.43,6-二碘-9-(4-甲酰苯基)咔唑(4)的合成在250mL的单口瓶中,加入9-(4-甲酰苯基)咔唑(5.00g,18.43mmol)及125mL的乙酸磁力搅拌并加热回流,待其完全溶解后,将反应混合物冷却至80℃。向其中加入KI(4.13g,24.83mmol)、KIO3(3.00g,14.00mmol),该反应体系温度维持在80℃,继续磁力搅拌反应5h。待反应完毕后,用足量5%NaHSO3水溶液淬灭,以除去多余的I2、100KIO3,二氯甲烷萃取,分液漏斗分离,有机层经无水Na2SO4干燥,有机相减压旋蒸去1除有机溶剂,残留物通过无水四氢呋喃重结晶,得褐色固体,得率84.1%。HNMR(600MHz,CDCl3)δ10.13(s,1H),8.41(s,2H),8.13(d,J=7.2Hz,2H),7.72(t,J=9.0Hz,4H),7.22(d,J=8.4Hz,2H)。1.3.55-(4-(3,6-二碘-9-咔唑)苯基)二吡咯甲烷(5)的合成105在250mL的三口瓶中,加入100mL干燥处理的二氯甲烷和新蒸馏的50mL吡咯(704.00mmol)。避光及氩气保护条件下,逐滴加入三氟乙酸(0.21mL,0.28mmol),磁力搅拌数分钟,待三氟乙酸完全溶于溶液中后,缓慢滴加溶于10mL二氯甲烷的3,6-二碘-9-(4-甲酰苯基)咔唑(0.96g,1.84mmol)溶液,待滴加完后再继续磁力搅拌反应1h,反应结束后,加入足量饱和NaOH溶液淬灭,二氯甲烷萃取,分离出有机层,无水Na2SO4110干燥,再分别减压旋蒸除去二氯甲烷和多余的吡咯,残留物使用硅胶柱层析分离提纯,1二氯甲烷作为洗脱液,快速柱层析,得橙黄色固体,收率87.6%。HNMR(600MHz,CDCl3)δ8.38(d,J=1.8Hz,2H),8.04(s,2H),7.65(d,J=9.0Hz,2H),7.45-7.41(m,4H),7.16(d,J=8.4Hz,2H),6.78(s,2H),6.22(s,2H),5.99(s,2H),5.60(s,1H)。1.3.65,15-二-(4-(3,6-二碘-9-咔唑基)苯基)-10-(4-甲酸冰片酯苯基)咔咯(6)的合成115将(4-(3,6-二碘-9-咔唑基)苯基)二吡咯甲烷(1.79g,2.80mmol)和对甲酸冰片酯苯甲醛(0.38g,0.94mmol)加入500mL三口烧瓶,并加入干燥处理的二氯甲烷(70mL)进行溶解。氩气保护下,逐滴加入三氟乙酸(0.002mL),在室温及避光条件下,磁力搅拌反应4h后,加入DDQ(0.86g,3.80mmol),撤除氩气氧化0.5h,反应物减压旋蒸除去有机溶剂,残留物进行硅胶柱层析分离提纯,洗脱剂为二氯甲烷/石油醚=3:2,后经甲1120醇-氯仿重结晶后,得到暗紫色固体,产率:5.4%。HNMR(600MHz,CDCl3)δ9.08(s,4-4-
中国科技论文在线http://www.paper.edu.cnH),8.78(d,J=11.4Hz,2H),8.68-8.46(m,8H),8.34-8.16(m,6H),8.06(d,J=3.6Hz,4H),7.76(d,J=3.6Hz,4H),7.63(d,J=5.4Hz,4H),5.34-5.31(m,1H),2.64-2.61(m,1H),2.34-2.31(m,1H),1.92-1.87(m,1H),1.85(t,J=4.2Hz,1H),1.45-1.42(m,2H),1.31-1.29(m,1H),1.06(s,6H),0.99(s,3H);元素分析按C72H52I4N6O2,计值(%):C56.12,H-5-11253.40,N5.45;实验值(%):C56.21,H3.35,N5.51.UV-vis(CH2Cl2):λmax(nm)(ε×10Lmol-1cm):436(1.421),552(0.112),590(0.101),647(0.131)。1.4抗癌活性测试MTT测试是目前测定化合物体外抗癌活性最简单有效的方法之一。对冰片、化合130物3和6进行MTT测试,测定其对肝癌细胞(HepG2)的抗癌活性,并对其结果进行分析。具体实验过程如下:(1)接种肝癌细胞:0.25%胰蛋白酶消化,使肝癌细胞脱离,形成单细胞,加入培养3液配成单个细胞悬液,以每孔3×10左右个肝癌细胞接种到96孔培养板上,每孔体积100μL;135(2)培养肝癌细胞:在37℃,5%CO2及95%饱和湿度的条件下,培养6天,待细胞贴壁时,开始加药;(3)加入目标化合物:依次加入1、10、100μM浓度的目标化合物,每一浓度设三副孔(以避免偶然误差),依次加入完毕后,继续在培养箱中培养;(4)MTT显色:目标化合物与肝癌细胞共培养68h后,每孔加入20μL4mg/mL的140MTT溶液,继续放置在培养箱中孵育4h,接着,吸除孔内上层清液,每孔加入200μLDMSO,振荡5-10min,以使甲臜完全溶于DMSO中;(5)测OD:选择540nm波长,在酶标仪上测定各孔的OD值,并记录下结果;(6)根据下面公式(1),对数据进行分析处理,计算出对肿瘤细胞增殖的抑制率,并冰片、化合物3和6的㧕制率与浓度的关系柱状图。实验组OD值抗癌活性=1-×100%对照组OD值(1)1452结果与讨论2.1合成与表征如图1所示,以对甲酰基苯甲酸和冰片为起始原料,通过酯化反应得到对甲酸冰片酯苯甲醛(1),再与吡咯在三氟乙酸的催化作用下得到二吡咯衍生物(2),然后与4-(9H-150咔唑-9-基)苯甲醛在三氟乙酸的催化剂作用下缩合并经DDQ氧化得到咔咯化合物(3);对于化合物(6)的合成,是以4-(9H-咔唑-9-基)苯甲醛为原料对咔唑的3,6-位进行碘-5-
中国科技论文在线http://www.paper.edu.cn化,再在三氟乙酸的催化下与吡咯反应得到含碘代咔唑的二吡咯衍生物,接着三氟乙酸的催化下与对甲酸冰片酯苯甲醛发生缩合反应并经DDQ氧化得到化合物(6),另外还合成了咔唑基上3,6位为叔丁基或溴代的此类咔咯化合物,但因不稳定,在用柱层析155分离纯化过程中会发生分解,因而未能得到纯的物质。化合物3和6的结构分别通过了核磁共振氢谱进行了表征,核磁波谱上化学位移在7-10都是芳环及吡咯环结构上H的信号峰,化学位移5.3左右的为与酯基氧原子碳上的H的特征峰,化学位移在0.9-3是冰片基H的特征峰。因此表明合成的化合物3和6为目标化合物冰片基咔咯。2.2紫外-可见吸收光谱160新型含冰片基咔咯衍生物3、6的紫外-可见吸收光谱如图2和3所示。0.81.6431nm436nm1.4)0.6-1)1.2-1cm-1cm1.0-10.4LmolLmol0.8((-5-50.6ε×10ε×100.20.4647nm655nm545nm593nm0.2590nm552nm0.00.0300400500600700800300400500600700800Wavelength(nm)Wavelength(nm)图2化合物3的紫外-可见光谱图3化合物6的紫外-可见光谱Fig.2TheUV-visspectraofthecompound3Fig.3TheUV-visspectraofthecompound6165从图2和3中可以看出,化合物3和6分别都有一个很强的Soret带吸收峰及其三个较弱的Q带吸收峰,其Soret吸收带分别出现在436nm、431nm处是由于咔咯环的a1u(π)-eg(π*)的S0→S2所产生的允许跃迁,而550-650nm区域的三个较弱的Q带则是由于170咔咯环的a2u(π)-eg(π*)的S0→S1所产生的允许跃迁,符合咔咯类化合物的紫外-可见吸收光谱特征。另外,化合物6相对于化合物3具有更强的吸收及波长更长的吸收波长,这可能是由于含有更多给电子能力的咔唑基导致了HOMO与LUMO能级减小及跃迁机率增大所致。-6-
中国科技论文在线http://www.paper.edu.cn2.3MTT测试175图4化合物3和6的抗癌活性与浓度的关系Fig.4Relationshipofanticanceractivityandconcentrationofthecompounds3and6采用MTT法测定化合物3、6及冰片对肝癌细胞(HepG2)的抗癌活性,其结果如图4所示。从图可知,所有化合物都显示一定的抗癌活性,并随着浓度的增加,其抗癌活180性也随之增强;但咔咯基冰片化合物抗癌活性明显强于冰片化合物。另外,化合物3的抗癌活性明显要强于6。然而,化合物3和6对肝癌细胞(HepG2)抑制率并不是很理想,对其他癌细胞的抗癌活性研究还在进行中。3结论本文以冰片和吡咯为原料,设计合成了2个含冰片基及咔唑基的咔咯衍生物,利用185核磁共振波谱、元素分析、质谱及紫外-可见吸收光谱对其结构进行了表征,证实了所合成化合物为目标产物;并对其生物活性进行了研究,初步的抗癌活性表明,化合物3对肝癌细胞HepG2具有较好的抗癌生物活性,进一步的研究正在进行中。致谢190本研究课题得到教育部博士点基金资助(20133204120009)。[参考文献](References)[1]林文生,朱卫华,路桂芬等.咔咯锰、铁和钴配合物的合成与应用研究进展[J].应用化工,2011,40(2):319-323-7-
中国科技论文在线http://www.paper.edu.cn195[2]朱卫华,刘铁龙,李敏智等.两种取代咔咯的合成与表征[J].光谱实验室,2013,30(4):1562-1566[3]BarataJFB,NevesMGPMS,FaustinoMAF.StrategiesforCorroleFunctionalizationChem.Rev.2017,117:3192−3253[4]LiuHY,MahmoodaMHR,QiuSX,etal.Recentdevelopmentsinmanganesecorrole200chemistryCoord.Chem.Rev.2013,257:1306-1333[5]游丽莉,沈涵,史蕾等.新型Corrole光敏剂的光物理特性[J].中国科学:物理学力学天文学,2010,40:224-230[6]王家敏,史蕾,刘海洋.咔咯及其金属配合物与DNA的作用和抗肿瘤活性[J].化学进展,2015,27(6):7556-762.205[7]TeoRD,HwangJY,TerminiJ,etal.FightingCancerwithCorrolesChem.Rev.2017,117:2711−2729[8]LiangZH,LiuHY,ZhouR,etal.J.MembraneBiol.2016,249:419-428[9]BarataJFB,ZamarronA,NevesMGPMS,etal.Photodynamiceffectsinducedbymeso-tris(pentafluorophenyl)corroleanditscyclodextrinconjugatesoncytoskeletal210componentsofHeLacellsEur.J.Med.Chem.,2015,92:135-144[10]国家药典委员会.中华人民共和国药典(一部)[M].北京化学工业出版社,2010:41[11]LinJF,NiKF,ZhangY,etal.SynthesisandEvaluationofTransdermalPermeation,PharmacologicalActivityofBornylNSAIDEstersLettersinDrugDesign&Discovery,2015,21511:72-77[12]SuJY,LaiHQ,ChenJP,etal.NaturalBorneol,aMonoterpenoidCompound,PotentiatesSelenocystine-InducedApoptosisinHumanHepatocellularCarcinomaCellsbyEnhancementofCellularUptakeandActivationofROS-MediatedDNADamagePlosOne2013,8(5):e63502220[13]VasconcelosRM,LeiteFC,LeiteJA,etal.Synthesis,acutetoxicityandanti-inflammatoryeffectofbornylsalicylate,asalicylicacidderivative.Immunopharmacolgyandimmunotoxicology2012,34:1028-1038.[14]HanM,LiuY,ZhangB,etal.Salvianicborneolesterreducesbeta-amyloidoligomersandpreventscytotoxicity.PharmaceuticalBiology,2011,49:1008-1013225-8-'
您可能关注的文档
- 一种三氟甲基取代的叔丁基联蒽类多功能蓝光材料及OLED性能研究.pdf
- 一种免标记检测聚腺苷二磷酸核糖聚合酶-1活性的新方法.pdf
- 一种基于鱼眼全景拍摄的畸变车牌校正新方法.pdf
- 不同瓦斯压力下煤岩单轴压缩力学性质及声发射特性研究.pdf
- 二进制程序漏洞挖掘关键技术研究综述.pdf
- 交通事件下拥堵网络化蔓延的框架模型与算法.pdf
- 亲水支架细胞培养的染色方法.pdf
- 低温条件下活性污泥呼吸图谱特征变化.pdf
- 光控智能界面构建及其在生物中的应用.pdf
- 利用InSAR Stacking技术监测雷州半岛沉降.pdf
- 单轴压缩条件下含瓦斯煤样力学性质研究.pdf
- 双斜盘串联式液压变压器流场特性分析.pdf
- 双曲积的渐近上曲率.pdf
- 双氰胺改性角蛋白填料的制备与应用.pdf
- 双链RNA结合蛋白TRBP、PRKRA在miRNA成熟过程中的调控作用.pdf
- 变革型导师风格对研究生经验开放性的影响机制研究.pdf
- 同伴压力对消费者减排行为的影响分析.pdf
- 噬菌体展示筛选与狂犬病毒P互作的宿主蛋白.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明