- 773.58 KB
- 2022-04-22 13:43:34 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中国科技论文在线http://www.paper.edu.cn#光敏感型水凝胶的研究进展**廖悦,徐子扬,刘文广(天津大学材料科学与工程学院,天津,300350)5摘要:由于可实现远程、精准控制以及刺激因素的调控灵活方便等独特优势,光敏感型水凝胶取得了快速进展。近年来,人们发展了很多光敏感型水凝胶体系,根据光敏型基团的光致反应机理不同,主要可以分为光异构型水凝胶、光裂解型水凝胶和光二聚型水凝胶。这些光敏感型水凝胶可以在细胞培养、脱附、可控释放等方面得到应用。本文综述了近年来光敏感型水凝胶的研究进展以及在生物医学方面的应用,并对其未来的发展方向进行了展望。10关键词:光敏感;水凝胶;生物医学应用中图分类号:0648.17RecentadvanceinphotosensitivehydrogelsLIAOYue,XUZiyang,LIUWenguang15(SchoolofMaterialsScienceandEngineering,TianjinUniversity,Tianjin300350)Abstract:Rapidprogresshasbeenmadeinphosensitivehydrogelsrecentlyduetotheirspecificadvantagessuchasremotesensing,precisecontrollingandflexibleadjustmentofthestimulatingfactors.Lotsofphotosensitivehydrogelsystemshavebeendevelopedandcouldbegroupedintothreemaincategoriesaccordingtothephotoinducedmechanismofphotosensitivegroup:photoisomerized20hydrogels,lightcleavablehydrogelsandlightsensitivedimerizedhydrogels.Andthesehydrogelshavebeenbeusedincontrollingcelladhesion/detachmentandcontrolledreleaseofcell.Inthisarticle,recentprogressinphotosensitivehydrgelsandtheirbimedicalapplicationswerereviewedandfuturedevelopmentdirectionwasoutlooked.Keywords:photosensitivity;hydrogels;biomedicalapplications250引言光敏感型水凝胶,是一类可以响应光信号而发生物理性质或化学性质变化的智能型水凝胶。此类水凝胶的聚合物网络内部通常包含一个光感受器(通常是具有光致变色能力的发色团)和一个功能基团,当光照时,光信号首先由光感受器中的发色团捕获,然后通过发色团30的异构化、裂解或二聚反应将它转变成化学信号,这个化学信号经过一个化学回路被转移至[1]功能基团,从而影响和改变了水凝胶的结构和性能。与其他刺激因素相比,光具有快速、高效、节能、安全的优势,能够在时间和空间上实现对水凝胶进行远程、精准控制,这使得[2-4]光敏型水凝胶得到了迅速的发展。光敏型水凝胶的响应行为与光敏型基团的选择有关,而根据光敏型基团的光致反应机理不同,光敏型水凝胶可以分为三类:光异构型水凝胶、光[5]35裂解型水凝胶以及光二聚型水凝胶。1光异构型水凝胶光异构型水凝胶是聚合物分子链上含有多个光异构型基团的水凝胶。常见的光异构型基团主要包括偶氮苯(azobenzene)和螺吡喃(spiropyran)等。这些基团均能在紫外、可见光基金项目:高等学校博士学科点专项科研基金的资助(20130032110006)作者简介:廖悦(1991-),女,硕士研究生,主要研究方向:生物医用高分子材料通信联系人:刘文广(1968-),男,教授/博导,主要研究方向:生物医用高分子材料.E-mail:wgliu@tju.edu.cn-1-
中国科技论文在线http://www.paper.edu.cn40照射下发生可逆的异构化反应,造成水凝胶网络亲疏水性的转变。1.1基于偶氮苯基团的光异构型水凝胶偶氮苯基团的光致反应机理是其内部的N=N键发生了可逆的顺反异构化过程。当受到紫外光辐照时,偶氮苯基团会经历从反式结构到顺式结构的异构化过程,而在照射可见光或升温之后,又能恢复到反式结构。这是由于偶氮苯基团在紫外区有一个π-π*强吸收峰,而[6]45在可见区有一个n-π*弱吸收峰,通常反式结构比顺式结构更稳定,能量差约为50kJ/mol。此外,偶氮苯基团的顺反异构使得分子极性、分子尺寸、空间位阻乃至电性能等发生变化,造成水凝胶体系的形状、体积、溶胀性质及一些功能上的改变,甚至会引起凝胶-溶胶转变[7,8]。[9]Anseth等根据上述性质设计了一种包含偶氮苯基团的PEG基水凝胶,它利用不同波50长的光照刺激下偶氮苯基团的异构化,实现了水凝胶体系在刚性和柔性之间的可逆转变,该材料可以通过光照调控自身弹性模量,从而实时控制细胞的粘附形态和生长状况,在智能体外细胞培养基质方面具有潜在的应用价值。1.2基于螺吡喃的光异构型水凝胶螺吡喃(SP)是一种常见的具有光致变色性质的光敏型基团。在紫外光照射下,SP杂55环上的C-O螺环键发生断裂并形成一个面内高度共轭的发色团,该发色团在可见区有着强烈的吸收峰,于是,SP就转变为它的异构体部花青(merocyanine,MC),这个开环结构的MC又可通过可见光刺激或加热恢复至闭环结构的SP。其中,MC带有两性离子,相对亲水;SP呈中性,不带电,相对疏水。将螺吡喃基团引入到水凝胶体系中,可利用光照调控水凝[10,11]胶的溶胀行为。此外,紫外光照射后,水凝胶呈现出紫色;而在照射白光之后,又能变60回无色。含有螺吡喃基团的光敏型水凝胶具有比偶氮苯基水凝胶更大程度的亲水-疏水平衡[6,12]转变和更为优势的光致变色性质,因此在光异构型水凝胶集体中占有重要的一席之地。[13]本课题组以低聚乙二醇甲基丙烯酸酯(OEGMA)、2-乙烯基-4,6-二氨基-1,3,5-三嗪(VDT)和合成的具有螺吡喃结构的小分子SPAA为单体,聚乙二醇双丙烯酸酯(PEGDA)为交联剂,采用紫外光引发自由基共聚反应制备出光敏型的P(OEGMA-co-VDT-co-SPAA)65水凝胶(简称POVSP)。在POVSP水凝胶基体表面接种和培养小鼠成纤维细胞(L929),当细胞粘附、伸展并呈现一个良好的状态时,利用365nm波长的紫外光对其表面进行辐照,可使体系内部的SP转化成MC结构,水凝胶的亲水性得到提高,实现L929细胞从POVSP水凝胶表面的脱附。MTT试验表明,这种光刺激法能实现L929细胞的无损脱附。此外,使用光罩对水凝胶表面局部区域进行遮挡,有效控制了细胞的选择性脱附,更具70自主性和灵活性,使这种光敏型水凝胶的优势得到了更好的发挥。尤其重要的是,Liu等根据二氨基三嗪(diaminotriazine)间的自氢键作用原理,将PVDT/pDNA复合微粒锚固到POVSP水凝胶表面,实现了介导基因在非洲绿猴肾细胞(COS-7)中的反向转染,并通过紫外光照射,致使这种基因修饰的细胞从水凝胶表面自动且无损地脱附(图1)。之后,课[14]题组继续探索并发展了这类光敏型材料,以丙烯酰胺(AAm)单体替代OEGMA,结果75表明:合成的PAVSP水凝胶具有更高的细胞粘附率及脱附率,具有更优异的细胞相容性,进一步利用纤连蛋白修饰和“三明治”式转染方法,使基因转染效率得到显著提升,为细胞的培养、脱附和基因转染技术提供了一个有效的体外平台。-2-
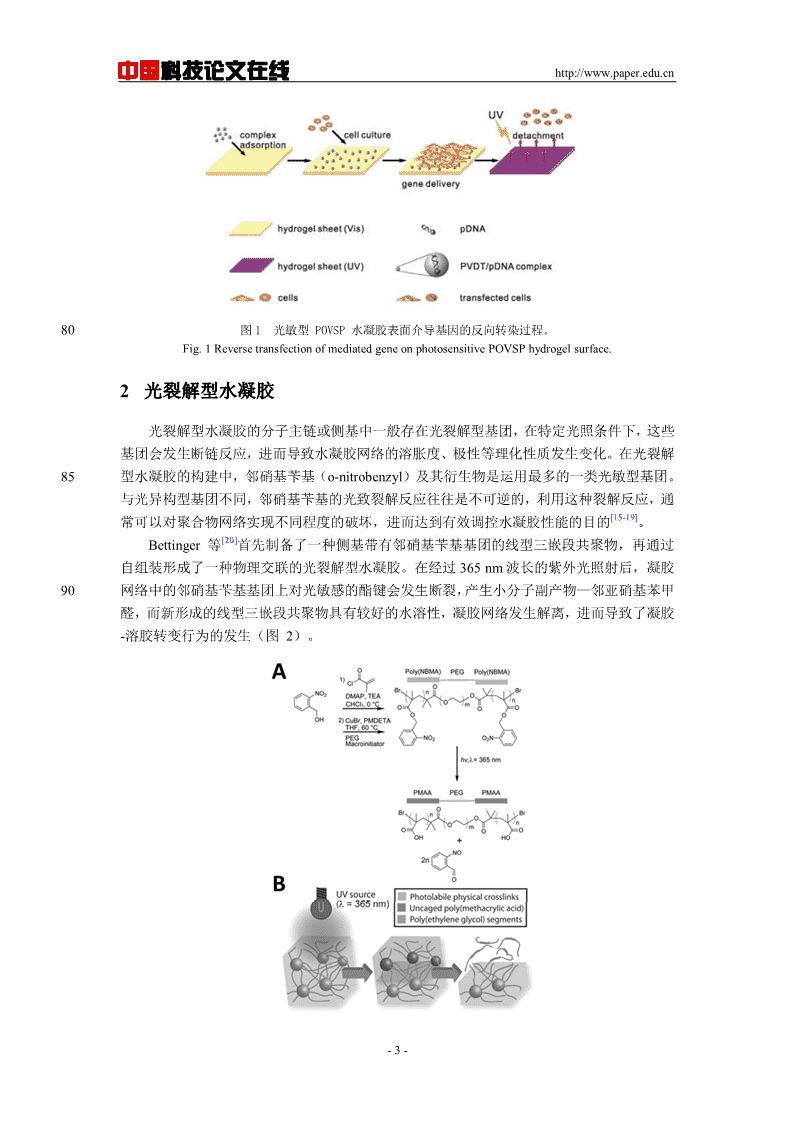
中国科技论文在线http://www.paper.edu.cn80图1光敏型POVSP水凝胶表面介导基因的反向转染过程。Fig.1ReversetransfectionofmediatedgeneonphotosensitivePOVSPhydrogelsurface.2光裂解型水凝胶光裂解型水凝胶的分子主链或侧基中一般存在光裂解型基团,在特定光照条件下,这些基团会发生断链反应,进而导致水凝胶网络的溶胀度、极性等理化性质发生变化。在光裂解85型水凝胶的构建中,邻硝基苄基(o-nitrobenzyl)及其衍生物是运用最多的一类光敏型基团。与光异构型基团不同,邻硝基苄基的光致裂解反应往往是不可逆的,利用这种裂解反应,通[15-19]常可以对聚合物网络实现不同程度的破坏,进而达到有效调控水凝胶性能的目的。[20]Bettinger等首先制备了一种侧基带有邻硝基苄基基团的线型三嵌段共聚物,再通过自组装形成了一种物理交联的光裂解型水凝胶。在经过365nm波长的紫外光照射后,凝胶90网络中的邻硝基苄基基团上对光敏感的酯键会发生断裂,产生小分子副产物—邻亚硝基苯甲醛,而新形成的线型三嵌段共聚物具有较好的水溶性,凝胶网络发生解离,进而导致了凝胶-溶胶转变行为的发生(图2)。-3-
中国科技论文在线http://www.paper.edu.cn图2光裂解型水凝胶的制备和光致分解过程示意图。(A)Poly(NBMA)-b-PEG-b-poly(NBMA)三嵌段共聚95物的制备与光刺激脱保护。(B)共聚物网络中物理交联的解离示意图。Fig.2Preparationandphotodecompositionofphoto-cleavedhydrogel.(A)Synthesisandphotodeprotectionofpoly(NBMA)-b-PEG-b-poly(NBMA)triblockcopolymers.(B)Schematicillustrationofdissociationofphysicalcross-linkswithincopolymernetworks.光裂解型水凝胶不仅具有与细胞外基质相似的特性,有利于细胞的生长与繁殖,而且可100以通过远程遥控光照实时控制水凝胶的降解程度,从而实现对细胞的连续性或阶段性释放,因而可以作为支架材料用于细胞的装载和释放。[21]Kasko等将一系列含有邻硝基苄基基团的不同光敏型交联剂引入到水凝胶体系中,并考察了它们在相同光照条件下降解速率。基于上述研究,他们设计了不同体系构成的水凝胶整体,并定量研究了同一细胞群在其中的偏置释放。此外,他们将两类细胞(绿色荧光蛋白105表达的人的间充质干细胞,GFP-expressinghMSCs,和红色荧光蛋白表达的人的间充质干细胞,RFP-expressinghMSCs)分别封装在具有不同降解速率的两种水凝胶中,组成一种新颖的双重细胞支架模型,并利用同一光源进行照射,实现了两种细胞可控的多重精准释放(图3)。这种光裂解型水凝胶对于组织工程和再生医学领域有着十分重大的意义,尤其是对不能通过单一细胞群进行修复的复杂组织,上述水凝胶的构建打破了常规思路,为解决这一科110学难题找到了突破口。图3两种细胞的偏置释放水凝胶模型(A),两种凝胶之间的界面(B)及所封装细胞的释放数量随光照时间的关系图(C)。Fig.3Modelforwavelength-biasedreleaseoftwoencapsulatedcells(A),interfaceoftwogels(B)and115relationshipbetweenreleaseamountofencapsulatedcellsandlighttime(C).此外,光裂解型水凝胶还可以用于细胞的分离与筛选,这一过程在细胞学研究中,对于[22]降低干细胞、肿瘤细胞样品的异质性十分必要。Matsui等报道了一种链中含有光裂解型邻硝基苄基单元、链端为N-羟基丁二酰亚胺酯基的四臂聚乙二醇(NHS-PC-4armPEG)与带有丰富氨基的明胶(Gelatin)混合反应形成的化学交联的水凝胶,它能够在365nm波长的120紫外光照射下发生降解。如若使用计算机控制光照系统,局部照射能达到的降解区域最小精度约为20μm,能够实现对3D水凝胶环境中封装的细胞进行单个或多个目标细胞的分选(图4),分选所得的细胞移入另一个培养基继续培养,通过细胞分裂生长得到纯化的细胞群。值得强调的是,不论是细胞封装、紫外照射过程,还是水凝胶的降解产物,对细胞造成-4-
中国科技论文在线http://www.paper.edu.cn的毒害均可忽略不计,经历了这一分选过程的细胞生长状况良好。125图4光裂解型水凝胶中用以模拟细胞分选的光学微珠分选示意图。(A)较大的圆形区域;(B)单个微珠;(C)多个微珠。Fig.4Schematicdiagramofopticalbeadsortingforsimulatingcellsortinginphoto-cleavedhydrogels.(A)alargecirclearea,(B)asinglemicrobeadand(C)multiplemicrobeads.130此外,三苯甲烷(triphenylmethane)衍生物也可以作为一种光裂解型基团,它在光照下解离为离子对,并形成带有明显颜色的三苯甲基阳离子,加热时又能与周围环境中的阴离子[23]重新结合,恢复至先前的状态,具有可逆性。因此,三苯甲烷基水凝胶能够利用光照反复调控水凝胶的性质。3光二聚型水凝胶135体系中含有光二聚型基团的水凝胶称为光二聚型水凝胶。在一定光照条件下,光二聚型基团之间的两两反应形成的二聚物为水凝胶提供了可逆的交联点,通过转换光照条件,这些交联点又能发生解交联,因此,光二聚型基团能够用于引发成胶,控制凝胶-溶胶转变以及水凝胶的交联密度、溶胀度等。光二聚型基团通常有香豆素(coumarin)、肉桂酸(cinnamicacid)、蒽(anthracene)等。以香豆素基团为例,使用波长大于300nm的光照时,通过[2πs+2πs]140环加成反应形成环丁烷的二聚体,充当交联点;当使用波长小于260nm的光照时,二聚体[24]中的环丁烷会以对称的方式发生断裂,发生解交联,重新形成两个香豆素基团。[25]Anseth等设计、合成、制备了一类新型的香豆素基光二聚型水凝胶,这种水凝胶能够在水相中通过铜催化点击化学(copper-catalyzedclickchemistry)反应快速高效地形成,且聚合物网络的形成速率可以很好地控制。由于豆香素基团的存在,该水凝胶在365nm的紫-5-
中国科技论文在线http://www.paper.edu.cn145外光或405nm的可见光照射下,会发生可逆的光降解过程(图5)。此外,这种水凝胶还可以作为双光子吸收材料,当照射波长达到860nm时,材料表面会发生微米级尺度的刻蚀,该性能可以在时间和空间上实现对细胞微环境的调控,有望在组织工程领域得到应用。图5香豆素基水凝胶聚合物网络的形成和降解过程示意图。150Fig.5Schematicdiagramofformationanddegradationofcoumarinbasedhydrogelpolymernetworks.4展望由于具有无需额外试剂,可实现远程、精准控制以及刺激因素的调控灵活方便等独特优势,光敏感型水凝胶受到了众多研究人员的关注,并得到了迅速的发展。近年来,光敏感型水凝胶在生物材料,尤其是细胞培养、释放、筛选、脱附等方面取得了突破性进展,利用光155信号影响水凝胶的理化性质,进而实现对细胞为环境的实时调控,赋予了其在组织工程领域的潜在应用价值,有望作为一种功能型组织工程支架,影响细胞的行为,进而实现预期的组织修复效果。致谢感谢高等学校博士学科点专项科研基金的资助(20130032110006)。160[参考文献](References)[1]PeppasNA,KhareAR.Preparation,structureanddiffusionalbehaviorofhydrogelsincontrolledrelease[J].AdvancedDrugDeliveryReviews,1993,11(4):1-35.[2]TakashimaY,HatanakaS,OtsuboM,NakahataM,KakutaT,HashidzumeA,YamaguchiH,HaradaA.165Expansion-contractionofphotoresponsiveartificialmuscleregulatedbyhost-guestinteractions[J].NatureCommunications,2012,3(4):1270.[3]MosiewiczKA,KolbL,vanderVliesAJ,MartinoMM,LienemannPS,HubbellJA,EhrbarM,LutolfMP.Insitucellmanipulationthroughenzymatichydrogelphotopatterning[J].NatureMaterials,2013,12(11):1072-1078.170[4]ShinDS,YouJ,RahimianA,VuT,SiltanenC,EhsanipourA,StybayevaG,SutcliffeJ,RevzinA.Photodegradablehydrogelsforcapture,detection,andreleaseoflivecells[J].AngewanteChemicalInternationalEdition,2014,53(31):8221-8224.[5]TomatsuI,PengK,KrosA.Photoresponsivehydrogelsforbiomedicalapplications[J].AdvancedDrugDeliveryReviews,2011,63(14-15):1257-1266.175[6]TomatsuI,PengK,KrosA.Photoresponsivehydrogelsforbiomedicalapplications[J].AdvancedDrugDeliveryReviews,2011,63(14-15):1257-1266.[7]ZhaoYL,StoddartJF.Azobenzene-basedlight-responsivehydrogelsystem[J].Langmuir,2009,25(15):8442-8446.[8]WangD,WagnerM,ButtHJ,WuS.Supramolecularhydrogelsconstructedbyred-light-responsivehost-guest-6-
中国科技论文在线http://www.paper.edu.cn180interactionsforphoto-controlledproteinreleaseindeeptissue[J].SoftMatter,2015,11(38):7656-7662.[9]RosalesAM,MabryKM,NehlsEM,AnsethKS.Photoresponsiveelasticpropertiesofazobenzene-containingpoly(ethylene-glycol)-basedhydrogels[J].Biomacromolecules,2015,16(3):798-806.[10]SatohT,SumaruK,TakagiT,KanamoriT.Fast-reversiblelight-drivenhydrogelsconsistingofspirobenzopyran-functionalizedpoly(N-isopropylacrylamide)[J].SoftMatter,2011,7(18):8030-8034.185[11]StumpelJE,ZiółkowskiB,FloreaL,DiamondD,BroerDJ,SchenningAPHJ.Photoswitchableratchetsurfacetopographiesbasedonself-protonatingspiropyran-NIPAAMhydrogels[J].ACSAppliedMaterials&Interfaces,2014,6:7268-7274.[12]RosarioR,GustD,HayesM,JahnkeF,SpringerJ,GarciaAA.Photo-modulatedwettabilitychangesonspiropyran-coatedsurfaces[J].Langmuir,2002,18(21):8062-8069.190[13]WangN,ZhangJ,SunL,WangP,LiuW.Gene-modifiedcelldetachmentonphotoresponsivehydrogelsstrengthenedthroughhydrogenbonding[J].ActaBiomaterialia,2014,10(6):2529-2538.[14]WangN,LiY,ZhangY,LiaoY,LiuW.High-strengthphotoresponsivehydrogelsenablesurface-mediatedgenedeliveryandlight-inducedreversiblecelladhesion/detachment[J].Langmuir,2014,30(39):11823-11832.[15]TibbittMW,KloxinAM,SawickiLA,AnsethKS.Mechanicalpropertiesanddegradationofchainand195step-polymerizedphotodegradablehydrogels[J].Macromolecules,2013,46(7):2785-2792.[16]KloxinAM,TibbittMW,KaskoAM,FairbairnJA,AnsethKS.Tunablehydrogelsforexternalmanipulationofcellularmicroenvironmentsthroughcontrolledphotodegradation[J].AdvancedMaterials,2010,22(1):61-66.[17]KirschnerCM,AnsethKS.Insitucontrolofcellsubstratemicrotopographiesusingphotolabilehydrogels[J].200Small,2013,9(4):578-584.[18]McKinnonDD,BrownTE,KyburzKA,KiyotakeE,AnsethKS.Designandcharacterizationofasyntheticallyaccessible,photodegradablehydrogelforuser-directedformationofneuralnetworks[J].Biomacromolecules,2014,15(7):2808-2816.[19]DeForestCA,TirrellDA.Aphotoreversibleprotein-patterningapproachforguidingstemcellfatein205three-dimensionalgels[J].NatureMaterials,2015,14(5):523-531.[20]ZhuC,BettingerCJ.Light-induceddisintegrationofrobustphysicallycross-linkedpolymernetworks[J].MacromolecularRapidCommunications,2013,34(18):1446-1451.[21]GriffinDR,KaskoAM.Photodegradablemacromersandhydrogelsforlivecellencapsulationandrelease[J].JournalofAmericanChemicalSociety,2012,134(31):13103-13107.210[22]TamuraM,YanagawaF,SugiuraS,TakagiT,SumaruK,MatsuiH,KanamoriT.Opticalcellseparationfromthree-dimensionalenvironmentinphotodegradablehydrogelsforpureculturetechniques[J].ScientificReports,2014,4:4793.[23]QiuY,ParkK.Environment-sensitivehydrogelsfordrugdelivery[J].AdvancedDrugDeliveryReviews,2001,53(3):49-60.215[24]TrenorSR,ShultzAR,LoveBJ,LongTE.Coumarinsinpolymers:fromlightharvestingtophoto-cross-linkabletissuescaffolds[J].ChemicalReviews,2004,104(6):3059-3077.[25]AzagarsamyMA,McKinnonDD,AlgeDL,AnsethKS.Coumarin-basedphotodegradablehydrogel:design,synthesis,gelation,anddegradationkinetics[J].ACSMacroLetters,2014,3(6):515-519.-7-'
您可能关注的文档
- 三种萤火虫的线粒体基因组测序和18种甲虫的系统发育分析.pdf
- 三维颈动脉超声图像中斑块的纹理特征分析.pdf
- 不同Wx等位组合对杂交稻天优3611品质的影响.pdf
- 不同分辨率DEM与坡度关系分析.pdf
- 不同强度与时间高压静电辐射处理对麦长管蚜生长发育与繁殖的影响.pdf
- 个性特征对洪灾后创伤后应激障碍慢性化的影响.pdf
- 临夏学龄少数民族儿童患龋情况及相关因素调查分析.pdf
- 从“湿热瘀结”论治子宫内膜异位症.pdf
- 优化新生脉散方对心衰大鼠心功能及NT-proBNP水平影响的实验研究简报.pdf
- 关于《敖氏伤寒金镜录》的作者及版本流传的探讨.pdf
- 利用水文模型研究GPS站坐标时间序列.pdf
- 利用番茄红素提高细胞重编程效率的研究.pdf
- 利用高密度基因组芯片估计绵羊SNP之间的重组率和有效群体大小.pdf
- 制备温度对BiFeO3薄膜结构及性能的影响.pdf
- 单件生产系统的动态调度方法.pdf
- 单羰基姜黄素类似物的抗肿瘤靶点发现.pdf
- 卵巢癌起源理论与浆液性卵巢癌的输卵管起源新观点.pdf
- 卷接机斜置轴承分离装置设计与仿真.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明