- 395.31 KB
- 2022-04-22 13:43:41 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中国科技论文在线http://www.paper.edu.cn#单羰基姜黄素类似物的抗肿瘤靶点发现*李颖博,周德敏(北京大学药学院,北京100191)5摘要:目的:研究和发现单羰基姜黄素类化合物的抗肿瘤靶点。方法:通过反向对接预测化合物潜在作用靶点。利用MTT法检测化合物对前列腺癌细胞的抑制增殖能力。利用表面等离子体共振方法检测化合物与靶蛋白的结合能力。结果:单羰基姜黄素类化合物显著抑制肿瘤细胞增殖,活性优于姜黄素。通过反向对接预测提示该类化合物的作用靶点可能是CDK2。10表面等离子体共振检测结果显示,化合物与CDK2结离常数KD值与其抗肿瘤细胞增殖活性密切相关。结论:CDK2是此类单羰基姜黄素类似物的抗肿瘤潜在靶点。关键词:单羰基姜黄素类似物;抗肿瘤;靶点;CDK2中图分类号:Q5115Identificationofapotentialanti-cancertargetofmono-carbonylcurcuminanaloguesLIYingbo,ZHOUDemin(SchoolofPharmaceuticalSciences,PekingUniversity,Beijing100191)Abstract:Objective:Toidentifythepotentialanticancertargetsofmono-carbonylanaloguesof20curcumin.Methods:MTTassaywasusedtoevaluatetheanti-canceractivity.Insilicoapproachewasusedtopredictthepotentialtargets.Surfaceplasmonresponace(SPR)wasusedtoevaluatetheineractionofcompoundsandprotein.Results:Itisshowedthatthesecurcuminanaloguesdisplayedinvitroanti-canceractivitycomparableandevenhigherthanthatofcurcumin.ByPharmMappermapping,weidentifiedCDK2asapotentialtargetofthesecompounds.FurtherSPRexperiments25identifiedthatmono-carbonylcurcuminanaloguesbindtightlytohumanCDK2.Inaddition,theKDvaluesoftargetcompoundsobtainedintheSPRexperimentsshowedniceconsistencywiththedockingdataandtheinvitroanti-cancerresults.Conclusion:Thesemono-carbonylanaloguesofcurcuminarepotentinhibitorsofCDK2.Keywords:mono-carbonylanaloguesofcurcumin;anticancer;target;CDK2300引言姜黄素是从姜科植物根茎中提取的一类天然活性化合物,姜黄作为传统中药的应用已有两千多年的历史。姜黄素类化合物具有广泛的药理活性,包括抗炎、抗抑郁、心血管保护等35作用。其中,姜黄素的抗肿瘤作用尤其受到科学家的关注。研究显示,姜黄素具有抗肿瘤谱广泛、多靶点、能够逆转肿瘤多药耐药、毒性极低等优点。然而,姜黄素结构中的β-二酮[1,2]基团使其表现出结构不稳定以及体内代谢快的特点,严重影响了其临床应用。本研究设计并合成了一系列单羰基姜黄素类似物,这些化合物的药代动力学性质得到了极大改善,且一些化合物抗肿瘤增殖作用优于姜黄素。40在设计合成的基础上,我们借助反向分子对接的方法,以该类单羰基姜黄素类似物为探针,利用PharmMapperServer,在已知结构的靶点数据库中寻找可能与之结合的生物大分子,并通过数据库文献检索,预测该类化合物的可能作用靶点。在此基础上,利用表面等离子体共振方法(surfaceplasmonresponace,SPR)检测了化合物与大分子之间的结合能力,通过分基金项目:高等学校博士学科点专项科研基金(20130001120034)作者简介:李颖博(1983-),女,助理研究员,化学生物学.E-mail:liyb@bjmu.edu.cn-1-
中国科技论文在线http://www.paper.edu.cn析比较靶点结合力与抗肿瘤活性间的相关性,我们发现该类单羰基姜黄素类似物的抗肿瘤作45用靶标可能为cyclindependentkinase2(CDK2)。1材料与方法1.1通过PharmMapperServer对单羰基姜黄素类似物的潜在靶点进行预测PharmMapper数据库(http://59.78.96.61/pharmmapper/)是利用药效团匹配方法进行小分[3,4]子作用靶点预测的数据库。我们利用该数据库对单羰基姜黄素类似物进行反向分子对接50分析。将化合物以Mol2文件形式提交数据库,对小分子化合物进行优化,生成多种构象,选择全体人蛋白靶标库,最大构象数值选择300。PharmMappersever对配体小分子与其数据库中药效团自动匹配。1.2MTT法检测化合物对细胞活力的影响3前列腺癌细胞株PC-3于含10%胎牛血清,1%双抗的F12K培养基中常规培养。将5×1055细胞接种于96孔板中,贴壁后分别给予不同浓度的化合物,培养72h后加入MTT溶液,继续培养4h,弃去液体,每孔加入150μlDMSO,振荡使结晶物充分溶解后,在酶标仪以620nm吸收光处检测各孔吸光值。化和物IC50利用GraphPadPrism5软件计算。1.3表面等离子体共振方法(surfaceplasmonresonance,SPR)检测化合物与靶蛋白结合力60在BiacoreT200system(GEHealthcare,Sweden)上对化合物与人CDK2蛋白的结合能力进行检测。重组人CDK2蛋白购置于Novoprotein公司。将重组CDK2耦联于CM5芯片,耦联缓冲液为10mM硼酸钠(pH7.75)。化合物溶于含5%DMSO的PBS-P缓冲液。结合过程包括120-180s样品注射进样(60μl/min),300s结离和冲洗。采用Biacoreevaluationsoftware(T200version1.0)进行数据分析。652结果2.1单羰基姜黄素类似物具有抗肿瘤增殖作用我们设计合成了5个单羰基姜黄素类似物,C1和C3分别为姜黄素和双去甲氧基姜黄素,化合物结构式如图1所示。-2-
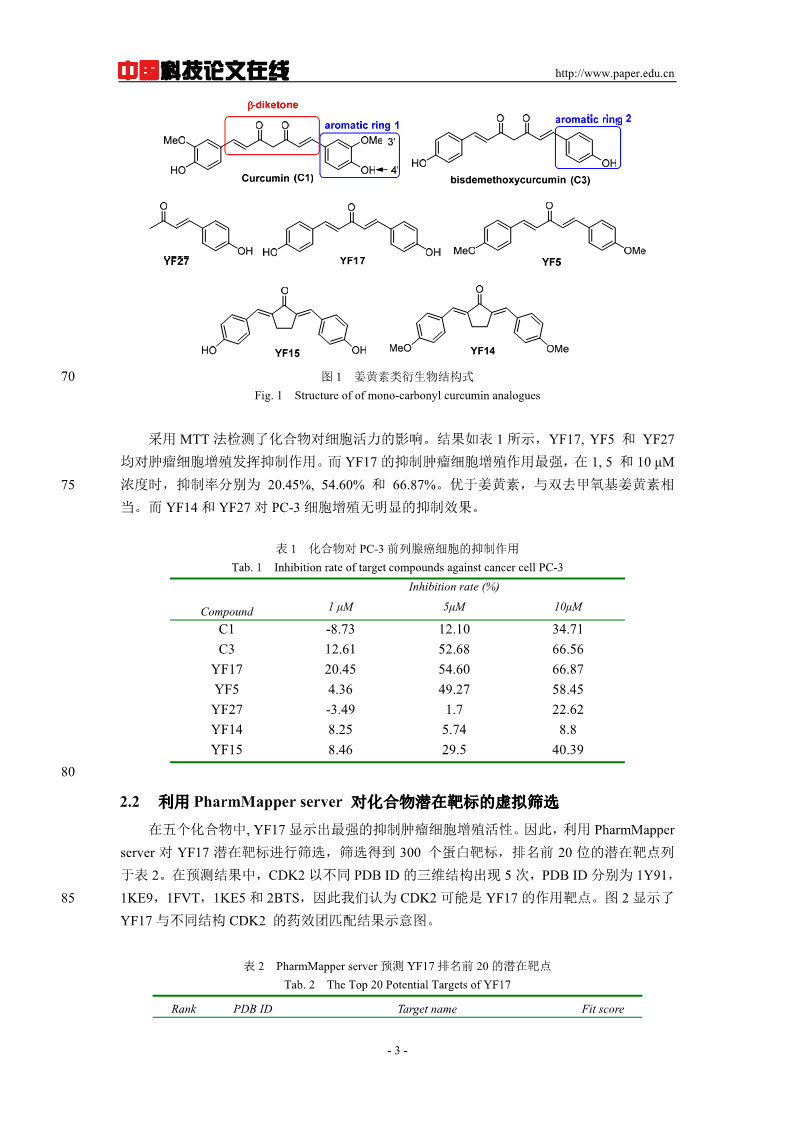
中国科技论文在线http://www.paper.edu.cn70图1姜黄素类衍生物结构式Fig.1Structureofofmono-carbonylcurcuminanalogues采用MTT法检测了化合物对细胞活力的影响。结果如表1所示,YF17,YF5和YF27均对肿瘤细胞增殖发挥抑制作用。而YF17的抑制肿瘤细胞增殖作用最强,在1,5和10μM75浓度时,抑制率分别为20.45%,54.60%和66.87%。优于姜黄素,与双去甲氧基姜黄素相当。而YF14和YF27对PC-3细胞增殖无明显的抑制效果。表1化合物对PC-3前列腺癌细胞的抑制作用Tab.1InhibitionrateoftargetcompoundsagainstcancercellPC-3Inhibitionrate(%)1μM5μM10μMCompoundC1-8.7312.1034.71C312.6152.6866.56YF1720.4554.6066.87YF54.3649.2758.45YF27-3.491.722.62YF148.255.748.8YF158.4629.540.39802.2利用PharmMapperserver对化合物潜在靶标的虚拟筛选在五个化合物中,YF17显示出最强的抑制肿瘤细胞增殖活性。因此,利用PharmMapperserver对YF17潜在靶标进行筛选,筛选得到300个蛋白靶标,排名前20位的潜在靶点列于表2。在预测结果中,CDK2以不同PDBID的三维结构出现5次,PDBID分别为1Y91,851KE9,1FVT,1KE5和2BTS,因此我们认为CDK2可能是YF17的作用靶点。图2显示了YF17与不同结构CDK2的药效团匹配结果示意图。表2PharmMapperserver预测YF17排名前20的潜在靶点Tab.2TheTop20PotentialTargetsofYF17RankPDBIDTargetnameFitscore-3-
中国科技论文在线http://www.paper.edu.cn12PE13-phosphoinositide-dependentproteinkinase4.524121PMUMitogen-activatedproteinkinase103.86932FGIBasicfibroblastgrowthfactorreceptor13.86442JDScAMP-dependentproteinkinasecatalytic3.863subunitalpha53LJRGlutathioneS-transferasetheta-23.84561P60Deoxycytidinekinase3.83971CBSCellularretinoicacid-bindingprotein23.83482DUXAldosereductase3.752917GSGlutathioneS-transferaseP3.737101Y91Celldivisionproteinkinase23.724112PE23-phosphoinositide-dependentproteinkinase3.651121ZZLMitogen-activatedproteinkinase143.61131KE9Celldivisionproteinkinase23.574141PGTGlutathioneS-transferaseP3.545151FVTCelldivisionproteinkinase23.508161KE5Celldivisionproteinkinase23.469171NMSCaspase-33.383182BTSCelldivisionproteinkinase23.375191XH4cAMP-dependentproteinkinasecatalytic3.338subunitalpha201XH5cAMP-dependentproteinkinasecatalytic3.258subunitalpha90注:CDK2用粗体标注图2YF17与靶蛋白CDK2药效图叠合图Fig.2TheindividualpharmacophoremodelsofYF17bindingwithCDK295-4-
中国科技论文在线http://www.paper.edu.cn2.3利用SPR法对化合物与CDK2结合能力进行检测表面等离子体共振方法SPR是一种检测生物分子间相互作用的光学检测技术,其原理是利用生物分子间结合产生的光学耦合参数变化,进行分子相互作用的信息检测。因其灵敏[5]性高、简便快捷,近年来被广泛用于生命科学、医药检测、药物筛选等领域。本研究利用100SPR法对虚拟预测的靶点进行了进一步验证。通过检测不同浓度化合物C1,C3,YF5,YF17和YF27与人重组CDK2蛋白的动态结合-结离曲线,拟合计算出化合物与CDK2结离常数KD值,KD值越大,引起最大效应所需药物浓度越多,则化合物与CDK2的亲和力越小。结果如图3所示,C1,C3,YF5,YF17和YF27的KD值分别为15.73,5.617,16.39,2.997和23.7μM。结合MTT结果分析,化合物的KD值与对肿瘤细胞抑制率成负性相关,即抑制率105高的化合物的KD值低,而抑制率低的化合物的KD值高。如抗肿瘤活性最强的YF17与CDK2结合力最高,而抗肿瘤活性最差的YF27与CDK2结合力最差。这一结果进一步确证了此类单羰基姜黄素类似物通过与CDK2结合,发挥抗肿瘤增殖作用。图3SPR法检测化合物与CDK2结合。110Fig.3IdentificationofbindingbetweencompoundstohumanCDK2bySPRassay.HumanCDK2wasimmobilizedonaCM5chipandtargetcompoundsinvariousconcentrationscirculatedonthechip.TheirKDvalueswerelabeledinthecorrespondingcurves.3讨论姜黄素结构中的β-二酮基团是造成其结构不稳定,体内代谢快的重要原因,通过改造115姜黄素结构中的β-二酮基团,科学家设计并合成了多个类型的姜黄素衍生物,以改善其药代动力学性质。其中把β-二酮结构改为具有单羰基结构的单羰基姜黄素类似物是其中较好的一类改造策略,此类化合物既保留了姜黄素的药理活性,结构稳定性又得到提高。研究显示,姜黄素在pH7.2的PBS溶液中的t1/2仅为10min,而改造后的单羰基姜黄素类似物在pH7.4的缓冲溶液中溶解后,经72h仍可检测出。体内实验也表明,单羰基姜黄素类似物[6]120的药动学性质得到了极大改善,血浆峰值浓度是姜黄素的10倍,半衰期是姜黄素的2倍。同时,单羰基姜黄素类似物保留了良好的抗肿瘤活性,在多种肿瘤细胞株和移植瘤小鼠模型[7,8]中显示出与姜黄素类似,甚至更高的活性。我们的研究结果也显示,在前列腺癌细胞株-5-
中国科技论文在线http://www.paper.edu.cnPC-3上,单羰基姜黄素类似物Y17的抗肿瘤增殖活性优于姜黄素。为深入探索单羰基姜黄素类似物的抗肿瘤作用机制,本研究中通过PharmMapperserver,125利用药效团匹配方法对单羰基姜黄素类似物进行反向分子对接分析,预测其可能作用靶标。结果提示YF17的作用靶点可能为CDK2。CDK2是细胞周期进程中的关键蛋白,以CDK2[9]为靶点设计的抑制剂已显示出良好的抗肿瘤活性。通过SPR方法检测了化合物与人重组CDK2蛋白的动态结合-结离曲线,分析化合物与CDK2结离常数KD值,结果显示了化合物的KD值与其对肿瘤细胞抑制率密切相关,抑制率高的化合物的KD值低,而抑制率低的化130合物的KD值高,进一步揭示了此类单羰基姜黄素类似物通过与CDK2结合发挥抗肿瘤增殖作用的可能性。本研究首次提出CDK2为单羰基姜黄素类似物的潜在抗肿瘤靶点,为姜黄素类化合物的药物设计和结构优化提供支持。4结论本文通过反向分子对接分析预测,抗肿瘤活性检测,结合SPR验证化合物与蛋白相互135作用,初步确证了CDK2是单羰基姜黄素类似物的抗肿瘤作用潜在靶点。这是首次对单羰基姜黄素类似物与CDK2相互作用的报道。本研究将为姜黄素类化合物的进一步结构优化和结构改造提供支持。[参考文献](References)[1]ParkW,AminAR,ChenZG,ShinDM.Newperspectivesofcurcuminincancerprevention[J].CancerPrev140Res(Phila),2013,6(5):387-400.[2]GuptaSC,KismaliG,AggarwalBB.Curcumin,acomponentofturmeric:fromfarmtopharmacy[J].Biofactors,2013,39(1):2-13.[3]LiuX,OuyangS,YuB,LiuY,HuangK,GongJ,ZhengS,LiZ,LiH,JiangH.PharmMapperserver:awebserverforpotentialdrugtargetidentificationusingpharmacophoremappingapproach[J].NucleicAcidsRes,14538(WebServerissue):W609-14.[4]ChitralaKN,YeguvapalliS.Computationalpredictionandanalysisofbreastcancertargetsfor6-methyl-1,3,8-trichlorodibenzofuran[J].PLoSOne,2014,9(11):e109185.[5]KurodaK,KatoM,MimaJ,UedaM.Systemsforthedetectionandanalysisofprotein-proteininteractions[J].ApplMicrobiolBiotechnol,2006,71(2):127-136.150[6]LiangG,ShaoL,WangY,ZhaoC,ChuY,XiaoJ,ZhaoY,LiX,YangS.Explorationandsynthesisofcurcuminanalogueswithimprovedstructuralstabilitybothinvitroandinvivoascytotoxicagents[J].BioorgMedChem.2009,17(6):2623-2631.[7]RobinsonTP,EhlersT,HubbardIVRB,BaiX,ArbiserJL,GoldsmithDJ,BowenJP.Design,synthesis,andbiologicalevaluationofangiogenesisinhibitors:aromaticenoneanddienoneanaloguesofcurcumin[J].Bioorg155MedChemLett,2003,13(1):115-117.[8]LeowPC,BahetyP,BoonCP,LeeCY,TanKL,YangT,EePL.FunctionalizedcurcuminanalogsaspotentmodulatorsoftheWnt/β-cateninsignalingpathway[J].EurJMedChem,2014,71:67-80.[9]DeAzevedoWFJr,Mueller-DieckmannHJ,Schulze-GahmenU,WorlandPJ,SausvilleE,KimSH.StructuralbasisforspecificityandpotencyofaflavonoidinhibitorofhumanCDK2,acellcyclekinase[J].ProcNatlAcad160SciUSA,1996,93(7):2735-2740.-6-'
您可能关注的文档
- 从“湿热瘀结”论治子宫内膜异位症.pdf
- 优化新生脉散方对心衰大鼠心功能及NT-proBNP水平影响的实验研究简报.pdf
- 光敏感型水凝胶的研究进展.pdf
- 关于《敖氏伤寒金镜录》的作者及版本流传的探讨.pdf
- 利用水文模型研究GPS站坐标时间序列.pdf
- 利用番茄红素提高细胞重编程效率的研究.pdf
- 利用高密度基因组芯片估计绵羊SNP之间的重组率和有效群体大小.pdf
- 制备温度对BiFeO3薄膜结构及性能的影响.pdf
- 单件生产系统的动态调度方法.pdf
- 卵巢癌起源理论与浆液性卵巢癌的输卵管起源新观点.pdf
- 卷接机斜置轴承分离装置设计与仿真.pdf
- 参芪解郁方对产后抑郁大鼠TregTh17平衡的干预作用研究.pdf
- 双酪氨酸诱导小鼠肠道氧化应激及炎症反应.pdf
- 双链DNA可能的几种局部拓扑结构.pdf
- 含油异丁烷的燃爆实验研究.pdf
- 吸热表面热辐射特性对太阳能腔式吸热器热效率的影响.pdf
- 四种发光甲虫的转录组测序和系统发育分析.pdf
- 四轮轮毂电机驱动电动汽车高效制动能量回收策略研究.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明