- 373.33 KB
- 2022-04-22 13:32:23 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中国科技论文在线http://www.paper.edu.cn#偶氮苯基镁自由基化合物的反应性研究*任文山,谷得发(西南大学化学化工学院,重庆400715)5摘要:最近报道的偶氮苯镁自由基金属化合物1是一个非常有用的低价镁合成子,它可以作为单电子转移试剂活化很多无机和有机小分子。本文将在前面的工作基础上,进一步探索该化合物的反应性。研究发现氮苯镁自由基化合物1能被溴化银氧化生成溴化物2。更重要的是,该化合物还可以与苯甲醛反应生成环状金属镁配合物3,这是首次发现偶氮苯镁自由基化合物1可被用作双电子还原剂。金属镁化合物2和3都通过了红外、元素分析以及X-射10线单晶衍射的检测。关键词:有机化学;偶氮苯镁;低价镁合成子;反应性中图分类号:O627.21ReactivityofaMagnesiumComplexwithanAzobenzenyl15AnionRadicalligandRenWenshan,GuDefa(CollegeofChemistryandChemicalEngineering,SouthwestUniversity,Chongqing400715)Abstract:Azobenzenylanionradicalcomplexofmagnesium1isanusfullow-valentmagnesiumsynthon,whichcanserveasagoodsingle-electronreductantasshownbythereactivitywithseveral20smallmolecules.Herein,itsreactivitywillbefurtherexplored.Treatmentcomplex1withAgBrgivesthebormcompound2.Furthermore,itisfirstlyfoundthatcompound1canbeusedasatwo-electronreductantbyreactionwithbenzaldehydeleadingtotheheterocycliccomplex3.Thecomplexes2and3hasbeencharacterizedbyinfraredspectroscopy,elementalanalysis,andsingle-crystalX-raydiffraction.)25Keywords:Organicchemistry;Azobenzenylmagnesiumcomplex;low-valentmagnesiumsynthon;Reactivity0引言在过去的几十年里,低价镁金属化合物备受化学家们的关注,它们经常作为还原剂用于30各类有机反应中。例如,Mg/MgX2(X=Br或者I)混合物可作为单电子还原剂用于很多不[1-3][4-6]饱和化合物的还原反应中。另外,Jones及其合作者在2007年报道的首例一价金属镁化合物具有溶解性好,较传统还原剂如金属钠、钾等更安全的特点,已相继被用于各类合[5,6][5-8]成反应中,并且常常成功的实现了一些用传统还原剂难以实现的反应。因此,开发新型的低价镁化合物,并研究它们的反应性是很有价值的工作。35氧化还原活性配体为低价镁化合物的制备提供了一条新的有效途径。目前虽然已有不少[9][10-12]含氧化还原活性配体如Ar-BIAN和DAD等的金属镁化合物报道。但是这些研究主要侧重于配合物的合成和结构方面,对于化合物的反应性则很少涉及。最近,我们合成了首例偶氮苯镁自由基金属化合物,并研究了它的反应性,结果表明该化合物是非常有用的“低价[13]镁合成子”,在反应中通常作为单电子转移试剂,可以用于制备一些通过常规方法很难合基金项目:高等学校博士学科点专项科研基金(新教师类)(20130182120011)作者简介:任文山(1983-),男,副教授、硕导,金属有机化学.E-mail:rws603@swu.edu.cn-1-
中国科技论文在线http://www.paper.edu.cn40成的金属镁配合物。这些结果激发了我们对该化合物反应性继续探索的兴趣。本文将在前面工作的基础上,进一步探索偶氮苯镁自由基金属化合物1对AgBr和苯甲醛的反应性。1实验部分1.1仪器与试剂45核磁谱是在Bruker-600型核磁共振仪器上完成,红外光谱测试通过Bio-RadFTS-185FT/IR红外光谱仪完成,单晶测试通过SupernovaE双微焦斑单晶衍射仪完成,元素分析通过VarioEL元素分析仪完成。所有试剂除特别注明外,均为市售A.R.级或C.R.级商品。正己烷、环己烷、苯、甲苯、四氢呋喃用金属钠与二苯甲酮回流除水后蒸出备用。1.2原料的制备[13]50原料偶氮苯镁自由基金属化合物1参照文献方法制备。市售苯甲醛用氢化钙处理后蒸出备用。1.3金属镁化合物的制备1.3.1有机金属镁配合物[HC(C(Me)N-2,6-iPr2C6H3)2]MgBr(THF)(2)的制备室温下,向[HC(C(Me)N-2,6-iPr2C6H3)2]Mg(PhNNPh)(THF)(1;0.7g,1mmol)的THF55(10mL)溶液中加入AgBr(0.19g,1mmol),搅拌1h,过滤,将滤液浓缩至6mL,并在室温下挥发两天获得2的无色晶体,产率:0.52g(87%)。(实测值:C,66.81;H,8.26N,4.75.1C33H49N2MgBrO的理论值:C,66.73;H,8.32;N,4.72%).HNMR(600MHz,C6D6):7.19-7.17(m,6H,Ar-H),4.86(s,1H,HC{C(CH3)NAr}2),3.60(brs,4H,THF),3.29(m,4H,CHMe2),1.68(s,6H,HC{C(CH3)NAr}2),1.38(d,12H,J=6.6Hz,CH(CH3)2),1.32(brs,4H,THF),1.23(d,6012H,J=6.6Hz,CH(CH3)2)ppm.IR(KBr):ν=2957(m),2924(m),2864(m),1619(m),1548(s),1460(m),1379(m),1320(m),1275(m),1173(m),1105(m),1057(m),1016(m),933(m),-1761(s)cm。1.3.2有机金属镁配合物{(THF)2Mg[OCH(Ph)(N2Ph2)]}2•2THF(3•2THF)的制备室温下,向[HC(C(Me)N-2,6-iPr2C6H3)2]Mg(PhNNPh)(THF)(1;0.7g,1mmol)的THF65(10mL)溶液中滴加PhCHO(0.106g,1mmol)的THF(5mL)溶液,并在室温下反应3oh,过滤,将滤液浓缩至5mL,向体系中滴加几滴正己烷后在-20C下放置两天获得3•2THF的无色晶体,产率:65%(0.34g)。(实测值:C,70.54;H,7.53;N,5.41.C62H80N4O8Mg2的理论值:C,70.39;H,7.62;N,5.30%).IR(KBr):ν=2962(m),2927(m),2863(m),1600(m),1549-1(m),1447(m),1384(m),1324(m),1260(s),1092(s),1021(s),932(m),873(m),800(s)cm。由70于3•2THF在氘代苯,氘代吡啶,氘代四氢呋喃中溶解度都非常差,无法进行核磁表征。-2-
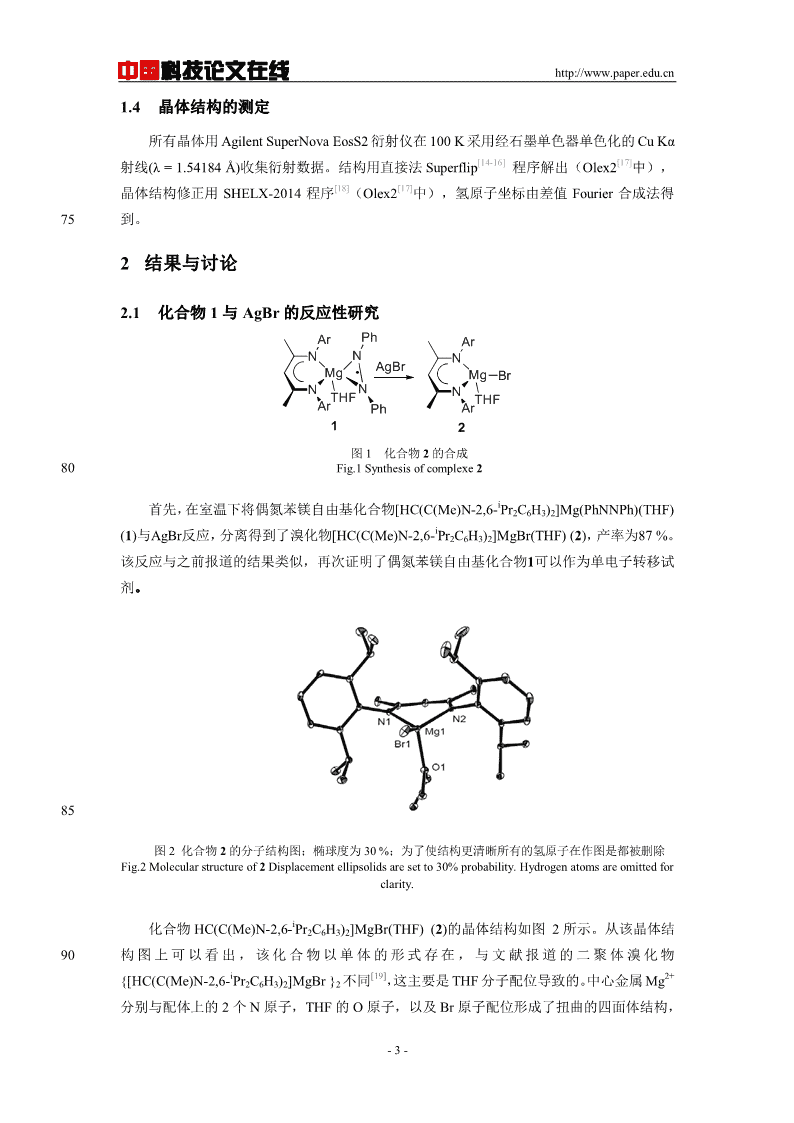
中国科技论文在线http://www.paper.edu.cn1.4晶体结构的测定所有晶体用AgilentSuperNovaEosS2衍射仪在100K采用经石墨单色器单色化的CuKα[14-16][17]射线(λ=1.54184Å)收集衍射数据。结构用直接法Superflip程序解出(Olex2中),[18][17]晶体结构修正用SHELX-2014程序(Olex2中),氢原子坐标由差值Fourier合成法得75到。2结果与讨论2.1化合物1与AgBr的反应性研究ArPhArNNNAgBrMgMgBrNNNTHFTHFArPhAr12图1化合物2的合成80Fig.1Synthesisofcomplexe2i首先,在室温下将偶氮苯镁自由基化合物[HC(C(Me)N-2,6-Pr2C6H3)2]Mg(PhNNPh)(THF)i(1)与AgBr反应,分离得到了溴化物[HC(C(Me)N-2,6-Pr2C6H3)2]MgBr(THF)(2),产率为87%。该反应与之前报道的结果类似,再次证明了偶氮苯镁自由基化合物1可以作为单电子转移试剂。85图2化合物2的分子结构图;椭球度为30%;为了使结构更清晰所有的氢原子在作图是都被删除Fig.2Molecularstructureof2Displacementellipsolidsaresetto30%probability.Hydrogenatomsareomittedforclarity.i化合物HC(C(Me)N-2,6-Pr2C6H3)2]MgBr(THF)(2)的晶体结构如图2所示。从该晶体结90构图上可以看出,该化合物以单体的形式存在,与文献报道的二聚体溴化物i[19]2+{[HC(C(Me)N-2,6-Pr2C6H3)2]MgBr}2不同,这主要是THF分子配位导致的。中心金属Mg分别与配体上的2个N原子,THF的O原子,以及Br原子配位形成了扭曲的四面体结构,-3-
中国科技论文在线http://www.paper.edu.cn2+oo因为这四个配位原子与中心金属Zn之间构成的键角范围为93.76(11)到119.19(9),与理[19]想的正四面体结构不同。Mg(1)-Br(1)的键长为2.4213(11)Å比文献报道的二聚体溴化物i95{[HC(C(Me)N-2,6-Pr2C6H3)2]MgBr}2(2.5282(7)Å)略短。2.2化合物1与PhCHO反应性研究图3化合物3的合成Fig.3Synthesisofcomplexes3100随后我们研究了化合物1对苯甲醛的反应性。有趣的是,将1当量的PhCHO加入到化合物1的THF溶液中后,发现PhCHO插入到镁和偶氮苯之间形成一个五元杂环物i-{(THF)2Mg[OCH(Ph)(N2Ph2)]}2(9)(图3),在这个过程中[HC(C(Me)N-2,6-Pr2C6H3)2]配体被消[20-21]i-除。根据之前的报道,一价阴离子[HC(C(Me)N-2,6-Pr2C6H3)2]配体在一定条件下也可以作为单电子还原剂。因此,我们推测该反应的具体过程是:首先偶氮苯自由基上的单电子转·105移到苯甲醛的“C=O”上,生成五元杂环MgN(Ph)N(Ph)CO,然后配体i−i·−[HC(C(Me)N-2,6-Pr2C6H3)2]被氧化,并以自由基的形式离去[HC(C(Me)N-2,6-Pr2C6H3)2],同时生成产物3。不幸的是,该过程所产生的中间体很难被捕捉到。这个反应结果与以前报道的结果不同,偶氮苯镁自由基化合物首次被发现可以作为双电子还原剂。110图4化合物3的分子结构图;椭球度为30%;为了使结构更清晰所有的氢原子在作图是都被删除Fig.4Molecularstructureof3.Displacementellipsolidsaresetto30%probability.Hydrogenatomsareomittedforclarity.2+化合物{(THF)2Mg[OCH(Ph)(N2Ph2)]}2(3)晶体结构如图4所示。中心金属Mg和一分子2-[OCH(Ph)(N2Ph2)]中的一个O原子一个N原子分别形成两个σ键,与另一分子-4-
中国科技论文在线http://www.paper.edu.cn2-115[OCH(Ph)(N2Ph2)]中的O形成一个σ配位键,与THF中的两个O配位形成一个扭曲的四方锥。2-2+两个[OCH(Ph)(N2Ph2)]配体中的两个O原子同中心Mg构成一个棱形结构。Mg(1)-Mg(1i)之i间的距离为3.0529(13)Å比{[HC(C(Me)N-2,6-Pr2C6H3)2]Mg}2(2.8457(8)Å)中的Mg-Mg键长[4]要长(2.8457(8)Å)。Mg(1)-O(1)(1.9734(16)和1.9935(16)Å)的键长与化合物[(EDBP-MeTs)Mg(nBu)](1.980(3),1.968(2),2.010(3)and2.013(3)Å)和[22]120[(EDBP-MeTs)Mg(μ-OBn)]2(1.925(2)and1.946(2)Å)中Mg-O的键长相似。Mg(1)-N(1)的键ii长为2.0896(19)Å,比[HC(C(Me)N-2,6-Pr2C6H3)2]Mg(NPr2)(1.938(2)Å)和i[22][HC(C(Me)N-2,6-Pr2C6H3)2]Mg[N(SiMe3)2](1.961(2)Å)中的Mg-N键长要长。表1化合物2和3的晶体测定参数Tab.1Crystaldataandexperimentalparametersforcompounds2and3Compound23•2THFchemicalformula0.5(C33H49BrMgN2O)C54H52Mg2N4O6,2(C4H8O)formulaweight296.981045.82crystalsize(mm)0.15×0.14×0.140.20x0.20x0.15radiation1.541841.54184crystalsystemorthorhombicmonoclinicspacegroupIba2P121/c1a(Å)15.5121(2)10.8196(4)b(Å)25.3630(3)12.6849(4)c(Å)16.72839(20)20.0833(6)α(°)9090β(°)9095.098(3)γ(°)90903V(Å)6581.53(14)2745.43(16)Z1623ρ(calc)(g/cm)1.1991.263F(000)25281108-1absorp.coeff.(mm)2.0740.871θrange(deg)5.224to71.5514.127to71.917reflnscollected16209(Rint=0.0329)15446/(Rint=0.0259)indep.reflns56035270Refnsobs.[I>2σ(I)]54774477data/restr/paras5603/1/3535270/1/357GOF1.0391.019R1/wR2[I>2σ(I)]0.0306/0.07850.0573/0.1533R1/wR2(alldata)0.0314/0.07930.0669/0.16163largpeakandhole(e/Å)0.794/-0.6610.648/-0.465CCDC15458611253结论本文在前面的研究工作基础上进一步探索了偶氮苯镁自由基化合物iHC(C(Me)N-2,6-Pr2C6H3)2]Mg(PhNNPh)(THF)(1)的反应性。发现当它与AgBr反应时,与前面报道的结果类似,表现出单电子还原性。但当它与PhCHO的反应时,首次被发现具有双-5-
中国科技论文在线http://www.paper.edu.cn130电子还原性。[参考文献](References)[1]RauschMD,McEwenWE,KleinbergJ.ReductionsInvolvingUnipositiveMagnesium[J].ChemicalReviews,1957,57(3):417-437.135[2]KöppeR,HenkeP,SchnöckelH.MgClandMg2Cl2:FromTheoreticalandThermodynamicConsiderationstoSpectroscopyandChemistryofSpecieswithMgMgBonds[J].AngewandteChemieInternationalEdition,2008,47(45):8740-8744.[3]ThumCCL,KhairallahGN,O"HairRAJ.Gas‐PhaseFormationoftheGomberg-BachmannMagnesiumKetyl[J].AngewandteChemieInternationalEdition,2008,47(47):9118-9121.140[4]GreenSP,JonesC,StaschA.Stablemagnesium(I)compoundswithMg-Mgbonds[J].Science,2007,318(5857):1754-1757.[5]JonesC,StaschA.StableMolecularMagnesium(I)Dimers:AFundamentallyAppealingYetSyntheticallyVersatileCompoundClass[M]//Alkaline-EarthMetalCompounds.SpringerBerlinHeidelberg,2013:73-101.[6]StaschA,JonesC.Stabledimericmagnesium(I)compounds:fromchemicallandmarkstoversatilereagents[J].145DaltonTransactions,2011,40(21):5659-5672.[7]BoutlandAJ,PernikI,StaschA,etal.Magnesium(I)DimersBearingTripodalDiimine-EnolateLigands:ProficientReagentsfortheControlledReductiveActivationofCO2andSO2[J].Chemistry-AEuropeanJournal,2015,21(44):15749-15758.[8]BoutlandAJ,DangeD,StaschA,etal.Two‐CoordinateMagnesium(I)DimersStabilizedbySuperBulky150AmidoLigands[J].AngewandteChemieInternationalEdition,2016,55(32):9239-9243.[9]HillNJ,Vargas-BacaI,CowleyAH.Recentdevelopmentsinthecoordinationchemistryofbis(imino)acenaphthene(BIAN)ligandswiths-andp-blockelements[J].DaltonTransactions,2009(2):240-253.[10]HillNJ,Vargas-BacaI,CowleyAH.Recentdevelopmentsinthecoordinationchemistryofbis(imino)acenaphthene(BIAN)ligandswiths-andp-blockelements[J].DaltonTransactions,2009(2):240-253.155[11]LiuY,YangP,YuJ,etal.Sodiumandmagnesiumcomplexeswithdianionicα-diimineligands[J].Organometallics,2008,27(22):5830-5835.[12]GaoJ,LiuY,ZhaoY,etal.SynthesesandStructuresofMagnesiumComplexeswithReducedα-DiimineLigands[J].Organometallics,2011,30(22):6071-6077.[13]RenW,GuD.AnAzobenzenylAnionRadicalComplexofMagnesium:Synthesis,Structure,andReactivity160Studies[J].InorganicChemistry,2016,55(22):11962-11970.[14]PalatinusL,ChapuisG.Superflip-acomputerprogramforthesolutionofcrystalstructuresbychargeflippinginarbitrarydimensions[J].JournalofAppliedCrystallography,2007,40(4):786-790.[15]PalatinusL,vanderLeeA.SymmetrydeterminationfollowingstructuresolutioninP1[J].JournalofAppliedCrystallography,2008,41(6):975-984.165[16]PalatinusL,PrathapaSJ,SmaalenS.EDMA:acomputerprogramfortopologicalanalysisofdiscreteelectrondensities[J].JournalofAppliedCrystallography,2012,45(3):575-580.[17]DolomanovOV,BourhisLJ,GildeaRJ,etal.OLEX2:acompletestructuresolution,refinementandanalysisprogram[J].JournalofAppliedCrystallography,2009,42(2):339-341.[18]SheldrickGM.AshorthistoryofSHELX[J].ActaCrystallographicaSectionA:Foundationsof170Crystallography,2008,64(1):112-122.[19]DoveAP,GibsonVC,HormnirunP,etal.Lowcoordinatemagnesiumchemistrysupportedbyabulkyβ-diketiminateligand[J].DaltonTransactions,2003(15):3088-3097.[20]KhusniyarovMM,BillE,WeyhermüllerT,etal.HiddenNoninnocence:TheoreticalandExperimentalEvidenceforRedoxActivityofaβ‐Diketiminate(1−)Ligand[J].AngewandteChemieInternationalEdition,1752011,50(7):1652-1655.[21]CampC,ArnoldJ.Onthenon-innocenceof"Nacnacs":ligand-basedreactivityinβ-diketiminatesupportedcoordinationcompounds[J].DaltonTransactions,2016,45(37):14462-14498.[22]WuJ,ChenYZ,HungWC,etal.Preparation,characterization,andcatalyticstudiesofmagnesiumphenoxides:highlyactiveinitiatorsforring-openingpolymerizationofL-lactide[J].Organometallics,2008,27(19):1804970-4978.-6-'
您可能关注的文档
- 让生命充满爱”校园演讲听后感.doc
- 记华新实验小学“五要素合格课展示周”活动.doc
- 基于罗丹明酰肼的铜离子荧光探针及其生物成像应用.pdf
- 玉米-大豆间作和施氮对红壤旱地作物碳氮吸收的影响.pdf
- 趋化因子及其受体与肠道炎症的研究进展.pdf
- 龙眼果肉多糖对巨噬细胞活化作用的研究.pdf
- Tim-3Galectin-9途径在肝脏区域免疫调节中的作用.pdf
- 一种低成本雷电定位预警系统的研究.pdf
- 作为Rho激酶抑制剂的六氢氮杂卓氧基苯甲酰胺类化合物的合成.pdf
- 利用直接重编程诱导心肌细胞体外培育心肌组织.pdf
- 双金属xNiyCo催化剂在二氧化碳重整甲烷反应中的催化性能:制备方法及载体孔结构的影响.pdf
- 叶酸偶联的荧光聚合物纳米探针的制备及细胞成像.pdf
- 基于图的流形排序的多层级融合显著性目标检测.pdf
- 基于季节调整的CPI与PPI传导关系研究.pdf
- 基于线反电动势估算的无刷直流电机无传感器控制策略.pdf
- 提升超导磁浮密封输运系统悬浮间距的方法.pdf
- 敲降KLF4表达增强肝癌细胞Bel-7402对奥沙利铂的敏感性.pdf
- 机械专业英语教学改革背景分析及对策.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明