- 510.80 KB
- 2022-04-22 13:44:35 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
'中国科技论文在线http://www.paper.edu.cn阿霉素涂层输尿管支架的制备及药物释放#行为的研究**马晓飞,肖艳,郎美东5(华东理工大学材料科学与工程学院,上海200237)摘要:本文采用开环共聚方式,以异辛酸亚锡为催化剂制备了PLCL5050共聚物,并通过核磁、凝胶渗透色谱表征共聚物的结构,差式扫描量热法、万能力学试验机表征共聚物的热力学和力学性能。采用溶液浸渍法制备了阿霉素涂层输尿管支架,并通过环氧乙烷灭菌方式进行灭菌。研究了阿霉素涂层支架在人工尿液中药物释放行为,探讨了载药量和环氧乙烷灭菌10处理对阿霉素药物释放行为的影响。结果表明,载药量的增加会降低药物的释放速度,而环氧乙烷灭菌会使阿霉素释放速度加快。关键词:阿霉素;输尿管支架;涂层;环氧乙烷;灭菌中图分类号:N5515PreparationandInVitroDrugReleaseofDoxorubicin-coatedUreteralStentsMaXiaofei,XiaoYan,LangMeidong(SchoolofMaterialsScienceandTechnology,EastChinaUniversityofScienceandTechnology,Shanghai200237)20Abstract:Poly(L-lactide-co-ɛ-caprolactone)(PLCL5050)copolymerwassynthesizedsuccessfullyviaring-openingpolymerization(ROP)usingstannousisocaprylateasthecatalyst.1H-NMR,13C-NMRandGPCwereappliedtocharacterizethestructureofthecopolymer.ThethermalandmechanicalpropertiesofPLCL5050weremeasuredbyDSCandtensiletests.PLCL5050ascarriersfordoxorubicinhydrochloride(DOX)wascoatedonureteralstentsbythedippingmethod.Both25non-sterileandethyleneoxid(EtO)sterilizedstentswereusedforloadingDOX.Tosimulateabodyenvironment,thereleaseprofilesofDOX-coatedureteralstentswasevaluatedinartificialurine,theeffectofthedrugdoesandsterilizationwereinvestigated.Theresultsindicatedthatthereleaserateofdoxorubicindecreasedwithincreasingdrugloading,whilethedrugreleaserateincreasedwhenthestentsweresterilizedbyEtO.30Keywords:doxorubicin;ureteralstent;coating;ethyleneoxide;sterilization0引言[1]近些年来,输尿管肿瘤发病率日趋增多,多以恶性病理,同时引发输尿管梗塞、肾衰[2]竭等疾病。目前临床上,对于输尿管肿瘤的治疗多存在于手术切除后,辅以化疗治疗。但[3]35是传统的化疗方式存在易扩散、选择性差、伴有明显的毒副作用等缺点。因此采用定向治疗输尿管肿瘤的方法是目前的一个重要研究方向。随着微创手术的发展,输尿管支架管已成为泌尿系统疾病中必备的器械,主要用于恶性输尿管肿瘤、输尿管结石等引发输尿管梗塞等泌尿系统疾病术后引流尿液和输尿管壁修补缺[4]损。随着药物洗脱支架在心血管狭窄定向治疗中的成功应用,药物洗脱输尿管支架也得到[5-6]40了一定的发展。药物涂层或药物洗脱输尿管支架以可降解聚合物作为药物的载体,当支架植入输尿管后,所携带的药物随着聚合物的降解而洗脱,或者以扩散的方式定向局部发挥基金项目:高等学校博士学科点专项科研基金(20130074110007)作者简介:马晓飞(1991-),女,硕士研究生,主要研究方向:可降解医用材料通信联系人:郎美东(1966-),男,教授,主要研究方向:生物材料.E-mail:mdlang@ecust.edu.cn-1-
中国科技论文在线http://www.paper.edu.cn[7]作用,治疗输尿管疾病。三氯生洗脱输尿管支架能够有效的缓解输尿管支架并发症;酮咯[8][9]酸洗脱输尿管支架可以有效的缓解术后的疼痛;Liatsikos等将紫杉醇洗脱支架和裸金属支架植入猪输尿管内,通过对比发现紫杉醇洗脱支架能够抑制肿瘤组织增生,延长引流的时45间。目前聚乳酸、聚己内酯、聚乙醇酸及其共聚物广泛的用作药物洗脱支架的涂层聚合物。[10]Multanen等以聚己内酯和聚乳酸共聚物作为载体,制备了氧氟沙星涂层支架,通过药物[11]的持续释减少细菌的粘附。丛晓明等以聚乳酸-聚乙醇酸为载体,发明了一种用于预防输尿管狭窄的输尿管支架,通过释放紫杉醇抑制疤痕细胞增生,避免输尿管狭窄或再狭窄。50本研究期望以聚乳酸聚己内酯共聚物PLCL5050为涂层药物载体,阿霉素盐酸盐为抗肿瘤模型药物,制备一种用于肿瘤定向治疗的输尿管支架。采用溶液浸渍的方法制备了高低载药浓度的两组阿霉素涂层输尿管支架,并通过环氧乙烷灭菌方式进行灭菌。此外,详细研究了阿霉素涂层支架在人工尿液中药物释放行为,探讨了载药量和环氧乙烷灭菌处理对阿霉素药物释放行为的影响。551实验部分1.1原料及试剂阿霉素盐酸盐(DOX•HCL)购于北京中硕科技有限公司,纯度98%。聚氨酯输尿管支架管购于张家港市沙工医疗器械科技发展有限公司。ε-己内酯(ε-CL)购于Aldrich,CaH2干燥72小时后减压蒸馏得到干燥的ε-CL己内酯。L-丙交酯(L-LA)由中国科学院长春应用60化学研究所提供,甲苯干燥重结晶三次。异辛酸亚锡(Sn(Oct)2)购于Sigma。其他试剂均购于上海凌峰化学试剂有限公司,分析纯产品。1.2聚丙交酯己内酯共聚物(PLCL5050)的合成在氩气的保护下,将ε-己内酯和L-丙交酯两种单体迅速加入到反应茄瓶中,置于45°C的油浴抽真空4h。在氩气的保护下,通过微量注射器滴加异辛酸亚锡甲苯溶液(单体质量65的千分之0.5)至反应体系中,换气三次。将反应茄瓶置于140°C的油浴中反应24h。反应结束后,待体系冷却至室温,加入适量的二氯甲烷溶解,冰甲醇沉降。将产物真空干燥至恒重。1.3阿霉素涂层输尿管支架的制备将盐酸阿霉素和聚丙交酯聚己内酯共聚物分别溶解于二甲基亚砜和四氢呋喃溶液中,溶70解均匀后,将盐酸阿霉素溶液逐滴滴加到PLCL共聚物溶液中形成聚合物药物溶液。将购买的聚氨酯输尿管支架裁剪成30mm,两端固定放入上述聚合物药物溶液中浸渍后取出,通风橱干燥24h。重复浸渍过程四次,通风橱干燥24h后置于45°C烘箱干燥72h,真空干燥至恒重。将制备的载药涂层输尿管支架中的一半采用环氧乙烷50°C灭菌2小时(上海市复旦大[12]学附属医院中山医院)。载药量通过聚合物药物溶液中药物与聚合物的比重进行计算。75阿霉素涂层输尿管支架的表面形貌通过SEM(JSM-6360LV;日本)测得,样品喷金处理,加速电压15kV。-2-
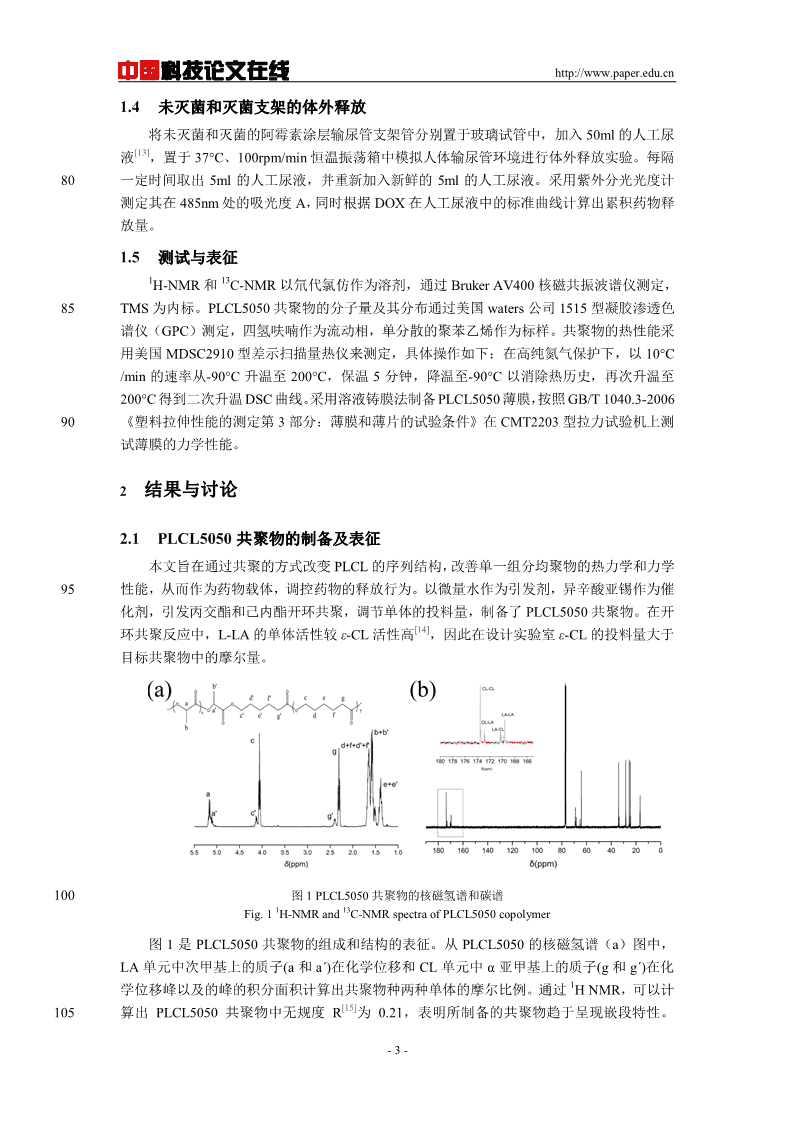
中国科技论文在线http://www.paper.edu.cn1.4未灭菌和灭菌支架的体外释放将未灭菌和灭菌的阿霉素涂层输尿管支架管分别置于玻璃试管中,加入50ml的人工尿[13]液,置于37°C、100rpm/min恒温振荡箱中模拟人体输尿管环境进行体外释放实验。每隔80一定时间取出5ml的人工尿液,并重新加入新鲜的5ml的人工尿液。采用紫外分光光度计测定其在485nm处的吸光度A,同时根据DOX在人工尿液中的标准曲线计算出累积药物释放量。1.5测试与表征113H-NMR和C-NMR以氘代氯仿作为溶剂,通过BrukerAV400核磁共振波谱仪测定,85TMS为内标。PLCL5050共聚物的分子量及其分布通过美国waters公司1515型凝胶渗透色谱仪(GPC)测定,四氢呋喃作为流动相,单分散的聚苯乙烯作为标样。共聚物的热性能采用美国MDSC2910型差示扫描量热仪来测定,具体操作如下:在高纯氮气保护下,以10°C/min的速率从-90°C升温至200°C,保温5分钟,降温至-90°C以消除热历史,再次升温至200°C得到二次升温DSC曲线。采用溶液铸膜法制备PLCL5050薄膜,按照GB/T1040.3-200690《塑料拉伸性能的测定第3部分:薄膜和薄片的试验条件》在CMT2203型拉力试验机上测试薄膜的力学性能。2结果与讨论2.1PLCL5050共聚物的制备及表征本文旨在通过共聚的方式改变PLCL的序列结构,改善单一组分均聚物的热力学和力学95性能,从而作为药物载体,调控药物的释放行为。以微量水作为引发剂,异辛酸亚锡作为催化剂,引发丙交酯和己内酯开环共聚,调节单体的投料量,制备了PLCL5050共聚物。在开[14]环共聚反应中,L-LA的单体活性较ε-CL活性高,因此在设计实验室ε-CL的投料量大于目标共聚物中的摩尔量。100图1PLCL5050共聚物的核磁氢谱和碳谱113Fig.1H-NMRandC-NMRspectraofPLCL5050copolymer图1是PLCL5050共聚物的组成和结构的表征。从PLCL5050的核磁氢谱(a)图中,LA单元中次甲基上的质子(a和a´)在化学位移和CL单元中α亚甲基上的质子(g和g´)在化1学位移峰以及的峰的积分面积计算出共聚物种两种单体的摩尔比例。通过HNMR,可以计[15]105算出PLCL5050共聚物中无规度R为0.21,表明所制备的共聚物趋于呈现嵌段特性。-3-
中国科技论文在线http://www.paper.edu.cn13PLCL5050共聚物的序列分布通过CNMR中酯基上的C的出峰进行表征。如图1(b)在160~180ppm之间出现四个峰,为173.49,172.90,170.26和169.60,分别对应CL-CL,[16]CL-LA,LA-CL和LA-LA的序列,这表明CL和LA在共聚物中是无规分布的。GPC测定的聚合物的分子量及分布总结在表1中,聚合物呈现单分散,分布相对较宽,这也证明聚110合物制备成功,组分单一。表1PLCL5050共聚物的性能表征Table1CharacteristicsofpreparedcopolymerinthisstudydE%MolarratioabcdMnbbccΔHmTs(MPa)CopolymersPDIRTg/℃Tm/℃(KDa)(J/g)(MPa)%LA%CL36.38;PLCL505050501231.710.21-47.204.42514.55.43118.48aTheactualfeedratiointheexperiment.b1CalculatedbyHNMRspectrafromtherelativeintensityofthemethineofPLLAat5.15ppmandtheε115methylenesignalofε-PCLat4.1ppm.cDeterminedbyGPC(Waters1515,USA).d1lLAandlCLaretheLAandCLnumberaveragesequencelengthsobtainedfromHNMR.ThesevaluesarecomparedtotheBernoullianrandomnumber-averagesequencelengths(lLA=1/CLandlCL=1/LA),obtainingtherandomnesscharactervalue(R).e120Obtainedfromthestress−straincurve.聚合物的组成和结构影响着其相应的热力学和力学性能。图2(a)是PLCL5050共聚物的二次升温DSC曲线,PLCL5050的Tg为-47.20℃,结果显示共聚物呈现两个Tm,介于PCL(60℃)和PLLA(189℃)的熔点之间。这也表明PLCL5050共聚物呈现了PCL和PLLA均聚物的特性,该共聚物为具有一定有序结构的无规共聚物。从熔融焓上看,共聚物125PLCL5050的ΔHm为4.425J/g,远远小于PCL和PLLA单一均聚物的熔融焓,这表明当共聚体系中两者的单体比例相等时,能够很好破坏CL和LA的结晶性。图2(b)是PLCL5050共聚物的拉伸曲线。从图中可以看出,PLCL5050共聚物在拉伸强度14.5MPa,断裂伸长率1854%,弹性模量E为5.43Mpa,呈现了强而韧的特性。130图2PLCL5050共聚物的DSC和应力-应变曲线Fig.2DSCandtensilestress-straincurvesofthePLCL5050copolymer2.2阿霉素涂层输尿管支架的表征实验中按照表2的配方配制了一定浓度的药物聚合物溶液,采用溶液浸渍法,通过改变药物聚合物药物溶液中药物的含量,制备了低载药量(14%(w/w))和高载药量(28%(w/w))-4-
中国科技论文在线http://www.paper.edu.cn135两组阿霉素涂层输尿管支架,低载药量支架(DOX-L)载药602µg,高载药量支架(DOX-H)[12]载药1346µg。不同支架的载药量的微小差异可能是由于裁剪的支架长度存在微小的不同。表2阿霉素涂层支架的性能参数Table2Thepropertiesofthestentcoatingsusedinthestudy(n=6)AbbreviationsPolymerDOX•HCLTHF/DMSODrugload/stentDOX-LPLCL5050,150mg21mg2ml/1.5ml602±67µgDOX-HPLCL5050,150mg42mg2ml/1.5ml1346±112µgFree/42mg2ml/1.5ml437±78µgControl//2ml/1.5ml/图3是通过SEM测得的Free对照组DOX支架(1a)和DOX-H药物涂层支架表面形140貌(1b)。从1a中可以明显看出大量的阿霉素药物呈球形分布于支架表面,而加了聚合物作为阿霉素载体的涂层支架,表面光滑,均一,这也说明阿霉素药物和聚合物相容性较好,能够被聚合物所包裹。图3不含聚合物和含聚合物阿霉素涂层支架的SEM表面形貌145Fig.3TheSEMimagesofDOXloadedureteralsentswith/withoutPLCL5050copolymer2.3未灭菌阿霉素涂层支架的体外释放PLCL5050共聚物作为阿霉素药物的载体,制备阿霉素涂层输尿管支架。通过阿霉素药物的洗脱,来达到定向治疗肿瘤的目的。150图4未灭菌阿霉素涂层支架的药物释放行为(UDOX-L:未灭菌处理的低载药量支架;UDOX-H:未灭菌处理的高载药量支架)Fig.4ThedoxorubicinreleaseprofilesofunsterilizedDOX-coatedureteralstents-5-
中国科技论文在线http://www.paper.edu.cn图4是未灭菌处理的低载药量和高载药量的阿霉素涂层支架的药物释放曲线。从释放趋势来看,所有的药物涂层支架释放趋势一致,在释放的起始阶段,低载药量和高载药量的支155架都发生了明显的突释。这一现象主要是因为裸露在支架涂层的表面未被包埋在聚合物中的阿霉素或者说是离涂层表面比较近的阿霉素,当一接触到释放介质时便能够很快的释放出来[17]。在突释之后,低载药量和高载药量的阿霉素涂层支架释放速度平缓,在60天之后,释放速度有所增加。从载药量上可以看出,载药量增加,药物的释放速率减慢。DOX-L组的阿霉素的释放速率明显快于DOX-H组。在120天时,DOX-L组释放了61%的药物,而DOX-H160组仅释放了46%。药物与药物之间的作用力能够影响和改变载药系统的物理化学性能,从[18-19]而影响药物的释放行为。2.4灭菌阿霉素涂层支架的体外释放输尿管支架作为泌尿外科广泛应用的引流产品,在使用前均需要经过灭菌处理。本文采用了环氧乙烷对高载药量的阿霉素涂层输尿管支架进行灭菌处理,研究了环氧乙烷灭菌对阿165霉素涂层支架药物释放行为的影响。文献报道灭菌会改变聚合物的分子量,组成和结构,影[20-21]响材料的性能。聚合物分子量、分布等都影响着其结晶性、力学性能及降解性能,也会影响到药物的释放性能。因此在研究灭菌后药物支架释放行为前研究了环氧乙烷对PLCL5050共聚物的影响。170图5PLCL5050共聚物灭菌处理前后GPC对比(SPLCL5050:灭菌处理的PLCL5050;UPLCL5050:未灭菌处理的PLCL5050)Fig.5GPCprofilesofPLCL5050copolymerbefore/aftersterilization175图5是涂层聚合物PLCL5050灭菌前后的GPC对比。从图中可以看出,灭菌后的PLCL5050的流出时间发生了偏移,分子量和分布发生变化。经过灭菌处理PLCL5050共聚物的分子量从123KDa变为112KDa,分子量分布从1.71变为1.74。这说明在灭菌过程中聚合物的主链发生断裂,使得分子量降低,分布变宽。-6-
中国科技论文在线http://www.paper.edu.cn180图6灭菌与未灭菌阿霉素涂层支架的药物释放行为对比(SDOX-H:灭菌处理的高载药量支架;UDOX-H:未灭菌处理的高载药量支架)Fig.6ThedoxorubicinreleaseprofilesofDOX-Hbefore/aftersterilization图6是阿霉素涂层支架灭菌前后的药物释放行为。从释放曲线的趋势来看,在释放的起始阶段,环氧乙烷灭菌处理后的药物支架灭菌也存在一个明显的突释。在10天之后,SDOX-H185组药物释放速率开始加快,在40天之后,释放速度显著增加,在整个实验阶段,药物的释放速率都明显快于未进行灭菌处理的UDOX-H组。在120天时,SDOX-H累计释放阿霉素65%,比UDOX-H多释放了19%的药物。结果表明环氧乙烷灭菌处理破坏了药物涂层聚合物的结构,从而影响了药物的释放行为。3结论190(1)通过溶液浸渍法制备了低载药量和高载药量的阿霉素涂层输尿管支架,药物涂层表面光滑均一。(2)研究了载药量对药物涂层支架药物释放行为的影响,载药量越高,药物的释放速率越慢,释放周期越长。(3)研究了环氧乙烷灭菌对药物涂层支架药物释放行为的影响,环氧乙烷灭菌处理后的195阿霉素涂层输尿管支架药物释放速率加快。致谢本论文获得了高等学校博士学科点专项科研基金(20130074110007)的资助。[参考文献](References)200[1]王晓.输尿管肿瘤的超声诊断进展[J].上海医学影像,2010,19(2):149-152.[2]赵勇,李涛.恶性肿瘤引起输尿管梗阻的外科治疗进展[J].中华腔镜泌尿外科杂志,2015,9(2):146-150.[3]董广星,陈旭.靶向药物阿霉素抗肿瘤研究新进展[J].天津药学,2003,15(2):60-63.[4]井新中,王梦江,李娅鑫,赵文杰.泌尿系统疾病治疗中输尿管支架的临床应用[J].中国医疗前沿,2013,8(11):54.205[5]LiatsikosE,KallidonisP,StolzenburgJU,KarnabatidisD.Ureteralstents:past,presentandfuture[J].Expert-7-
中国科技论文在线http://www.paper.edu.cnRev.Med.Devices,2009,6(3):313-324.[6]ChewBH,DuvdevaniM,DenstedtJD.Newdevelopmentsinureteralstentdesign,materialsandcoatings[J].ExpertRev.Med.Devices,2006,3(3):395-403.[7]Mendez-ProbstCE,GoneauLW,MacDonaldKW,NottL,SeneyS,ElwoodCN,LangeD,ChewBH,210DenstedtJD,CadieuxPA.Theuseoftriclosanelutingstentseffectivelyreducesureteralstentsymptoms:aprospectiverandomizedtrial[J].BJUInt,2012,110(5):749-754.[8]KrambeckAE,WalshRS,DenstedtJD,PremingerGM,LiJ,EvansJC,LingemanJE,LexingtonG.Anoveldrugelutingureteralstent:aprospective,randomized,multicenterclinicaltrialtoevaluatethesafetyandeffectivenessofaketorolacloadedureteralstent[J].JUrol,2010,183(3):1037-1042.215[9]LiatsikosEN,KarnabatidisD,KagadisGC,RokkasK,ConstantinidesC,ChristeasN,FlarisN,VoudoukisT,ScopaCD,PerimenisP,FilosKS,NikiforidisGC,StolzenburgJU,SiablisD.Applicationofpaclitaxel-elutin--gmetalmeshstentswithinthepigureter:anexperimentalstudy[J].EurUrol,2007,51(1):217-223.[10]MultanenM,TaljaM,HallanvuoS,SiitonenA,VälimaaT,TammelaTLJ,SeppäläJ,TörmäläP.Bacterialadherencetoofloxacin-blendedpolylactone-coatedself-reinforcedl-lacticacidpolymerurologicalstents[J].BJU220Int,2000,86(9):966-969.[11]从小明,顾晓箭.预防输尿管狭窄的支架及制备方法:中国,104001222A[P].2014-08-27.[12]MikkonenJ,UurtoI,IsotaloT,KotsarA,TammelaTL,TaljaM,SaleniusJP,TormalaP,KellomakiM.Drug-elutingbioabsorbablestents-aninvitrostudy[J].ActaBiomater,2009,5(8):2894-2900.[13]NowatzkiPJ,KoepselRR,StoodleyP,MinK,HarperA,MurataH,DonfackJ,HortelanoER,EhrlichGD,225RussellAJ.Salicylicacid-releasingpolyurethaneacrylatepolymersasanti-biofilmurologicalcathetercoatings[J].ActaBiomater,2012,8(5):1869-1880.[14]FernandezJ,EtxeberriaA,SarasuaJR.Synthesis,structureandpropertiesofpoly(L-lactide-co-epsilon-caprolactone)statisticalcopolymers[J].JMechBehavBiomedMater,2012,9:100-112.[15]FernándezJ,EtxeberriaA,SarasuaJR.Effectsofrepeatunitsequencedistributionandresidualcatalyston230thermaldegradationofpoly(l-lactide/ε-caprolactone)statisticalcopolymers[J].PolymDegradStabil,2013,98(7):1293-1299.[16]FernándezJ,EtxeberriaA,SarasuaJR.Invitrodegradationofpoly(lactide/δ-valerolactone)copolymers[J].PolymDegradStabil,2015,112:104-116.[17]PanCJ,TangJJ,WengYJ,WangJ,HuangN.Preparationandinvitroreleaseprofilesofdrug-eluting235controlledbiodegradablepolymercoatingstents[J].ColloidSurfB-Biointerfaces,2009,73(2):199-206.[18]FredenbergS,WahlgrenM,ReslowM,AxelssonA.Themechanismsofdrugreleaseinpoly(lactic-co-glycolicacid)-baseddrugdeliverysystems-areview[J].IntJPharm,2011,415(1-2):34-52.[19]HuT,YangJ,CuiK,RaoQ,YinT,TanL,ZhangY,LiZ,WangG.ControlledSlow-ReleaseDrug-ElutingStentsforthePreventionofCoronaryRestenosis:RecentProgressandFutureProspects[J].ACSApplied240Materials&Interfaces,2015,7(22):11695-11712.[20]WeirNA,BuchananFJ,OrrJF,FarrarDF.Influenceofprocessingandsterilisationonpropertiesofpoly-ϵ-caprolactone[J].Plastics,RubberandComposites,2003,32(6):265-270.[21]WeirNA,BuchananFJ,OrrJF,FarrarDF,BoydA.Processing,annealingandsterilisationofpoly-L-lactide[J].Biomaterials,2004,25(18):3939-3949.245-8-'
您可能关注的文档
- 苯达松在三种典型土壤中的吸附与淋溶.pdf
- 螺杆式双级冷凝器空气源热泵供暖系统模拟研究.pdf
- 表面改性强化微粉煤脱硫试验研究.pdf
- 论公共服务供给侧改革的价值目标.pdf
- 论实验动物腧穴的发展阶段.pdf
- 轴向并联式轴向磁场磁通切换混合永磁记忆电机的电磁特性研究.pdf
- 金属纳米圆盘-纳米球间隙模式表面等离激元共振特性研究.pdf
- 钴镍氢氧化物的制备及其电催化析氧性能研究.pdf
- 银包金等离子体纳米棒对激射性能的提高.pdf
- 零件加工一致性评价技术.pdf
- 面向众核负载聚集模式的Cache一致性协议研究综述.pdf
- 预补偿型反向训练模式下的01式跳空技术.pdf
- 高分辨率透射电镜碳烟图像量化分析方法研究.pdf
- 高压缩比天然气发动机爆震模拟及燃烧室优化.pdf
- 黄淮海平原区夏玉米倒伏特点及化控抗倒技术研究进展.pdf
- 黄芪甲苷对高胰岛素环境下肾小球系膜细胞的保护作用及其机制.pdf
- 黄连素激活TGR5、调节S1P2MAPK信号通路,抵抗高糖诱导的GMC中炎症纤维化成分的表达.pdf
- 黑加仑采收机的设计与试验.pdf
相关文档
- 施工规范CECS140-2002给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程
- 施工规范CECS141-2002给水排水工程埋地钢管管道结构设计规程
- 施工规范CECS142-2002给水排水工程埋地铸铁管管道结构设计规程
- 施工规范CECS143-2002给水排水工程埋地预制混凝土圆形管管道结构设计规程
- 施工规范CECS145-2002给水排水工程埋地矩形管管道结构设计规程
- 施工规范CECS190-2005给水排水工程埋地玻璃纤维增强塑料夹砂管管道结构设计规程
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程(含条文说明)
- cecs 141:2002 给水排水工程埋地钢管管道结构设计规程 条文说明
- cecs 140:2002 给水排水工程埋地管芯缠丝预应力混凝土管和预应力钢筒混凝土管管道结构设计规程 条文说明
- cecs 142:2002 给水排水工程埋地铸铁管管道结构设计规程 条文说明